I legami chimici sono fondamentali per comprendere come gli atomi... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
3,249
•
Aggiornato May 21, 2026
•
marle
@marlee_
I legami chimici sono fondamentali per comprendere come gli atomi... Mostra di più






Gli atomi formano legami per raggiungere la stabilità energetica. Quando due atomi si uniscono, l'energia potenziale del sistema diminuisce, rendendo la formazione del legame vantaggiosa dal punto di vista energetico.
La formazione di legami chimici è un processo che libera energia. Per rompere questi stessi legami, dobbiamo fornire energia al sistema. L'energia di legame indica quanta energia è necessaria per separare gli atomi legati: più è grande questo valore, più forte è il legame.
Secondo la regola dell'ottetto, gli atomi sono particolarmente stabili quando hanno otto elettroni nel loro livello energetico più esterno. Per raggiungere questa configurazione, gli atomi possono cedere, acquistare o condividere elettroni. La valenza di un atomo rappresenta proprio il numero di elettroni che può mettere in gioco per formare legami.
💡 Il legame ionico si forma quando un metallo cede elettroni a un non metallo. L'attrazione elettrostatica tra gli ioni di carica opposta che si formano è ciò che tiene uniti gli atomi nel composto.
Nel legame ionico, la forza di attrazione aumenta con la carica degli ioni e diminuisce con le loro dimensioni. I metalli dei primi tre gruppi tendono a perdere elettroni e diventare cationi, mentre i non metalli degli ultimi tre gruppi tendono ad acquistarne per diventare anioni.

Il legame metallico è responsabile delle proprietà caratteristiche dei metalli. In questo tipo di legame, gli ioni positivi dei metalli formano un reticolo cristallino mentre gli elettroni di valenza si muovono liberamente, creando una "nube elettronica" che avvolge tutti i cationi.
La forza del legame metallico dipende dalla carica nucleare: aumenta quando cresce la forza con cui il nucleo attrae gli elettroni. Nei metalli di transizione, anche gli elettroni degli orbitali d e f partecipano alla formazione della nuvola elettronica, creando alcune eccezioni nella forza del legame.
Il legame covalente si forma quando due atomi condividono una o più coppie di elettroni. Entrambi gli atomi esercitano una forza di attrazione sui medesimi elettroni, raggiungendo così la configurazione stabile del gas nobile più vicino. Possiamo rappresentare questo tipo di legame con le formule di Lewis.
💡 Quando gli atomi condividono due o tre coppie di elettroni, si formano legami multipli (doppi o tripli), che sono più forti e più corti dei legami semplici.
Nel legame covalente dativo, la coppia di elettroni condivisa proviene da un solo atomo (donatore), mentre l'altro (accettore) la utilizza per completare il proprio ottetto. Questo tipo di legame si rappresenta con una freccia e spiega la formazione dei composti di coordinazione, dove un metallo viene circondato da atomi donatori di elettroni.

La polarità di un legame dipende dalla differenza di elettronegatività tra gli atomi coinvolti. Quando due atomi identici formano un legame, si ha un legame covalente puro. Se invece gli atomi sono diversi, si crea un dipolo elettrico (legame covalente polare).
Possiamo classificare i legami in base alla differenza di elettronegatività (Δe):
Per rappresentare le strutture molecolari usiamo le formule di Lewis, seguendo alcuni passaggi fondamentali: stabilire la disposizione degli atomi, contare gli elettroni di valenza, rappresentare i legami semplici, completare gli ottetti e, se necessario, disegnare i legami multipli.
La teoria VSEPR (Valence Shell Electron Pair Repulsion) ci permette di prevedere la forma delle molecole. Secondo questa teoria, le coppie di elettroni del livello di valenza si respingono e tendono a disporsi il più lontano possibile le une dalle altre.
💡 La geometria di una molecola dipende dal numero totale di coppie elettroniche (sia condivise che non condivise) attorno all'atomo centrale.
Il numero di coppie elettroniche determina la struttura molecolare:

La polarità di una molecola non dipende solo dalla presenza di legami covalenti polari, ma anche dalla sua geometria. Le molecole elementari (formate da atomi uguali) sono sempre non polari, mentre i composti biatomici con atomi diversi sono sempre polari.
Per le molecole poliatomiche, ogni legame covalente polare origina un dipolo elettrico caratterizzato dal suo momento dipolare (μ), misurato in Debye (D). Una molecola è polare quando la somma vettoriale di tutti i momenti dipolari è diversa da zero.
Le molecole sono apolari solo quando l'atomo centrale è legato a gruppi identici e non presenta coppie di elettroni liberi. Alcune molecole complesse possono avere sia parti polari che apolari, caratteristica importante per la loro solubilità.
💡 Il principio "il simile scioglie il simile" spiega perché sostanze polari si sciolgono in solventi polari (come l'acqua) e sostanze apolari in solventi apolari.
La repulsione tra le coppie elettroniche varia in intensità: la repulsione tra due coppie libere è maggiore di quella tra una coppia libera e una condivisa, che a sua volta è maggiore della repulsione tra due coppie condivise. Questo influenza gli angoli di legame reali, che possono differire dai valori ideali previsti dalla teoria VSEPR.
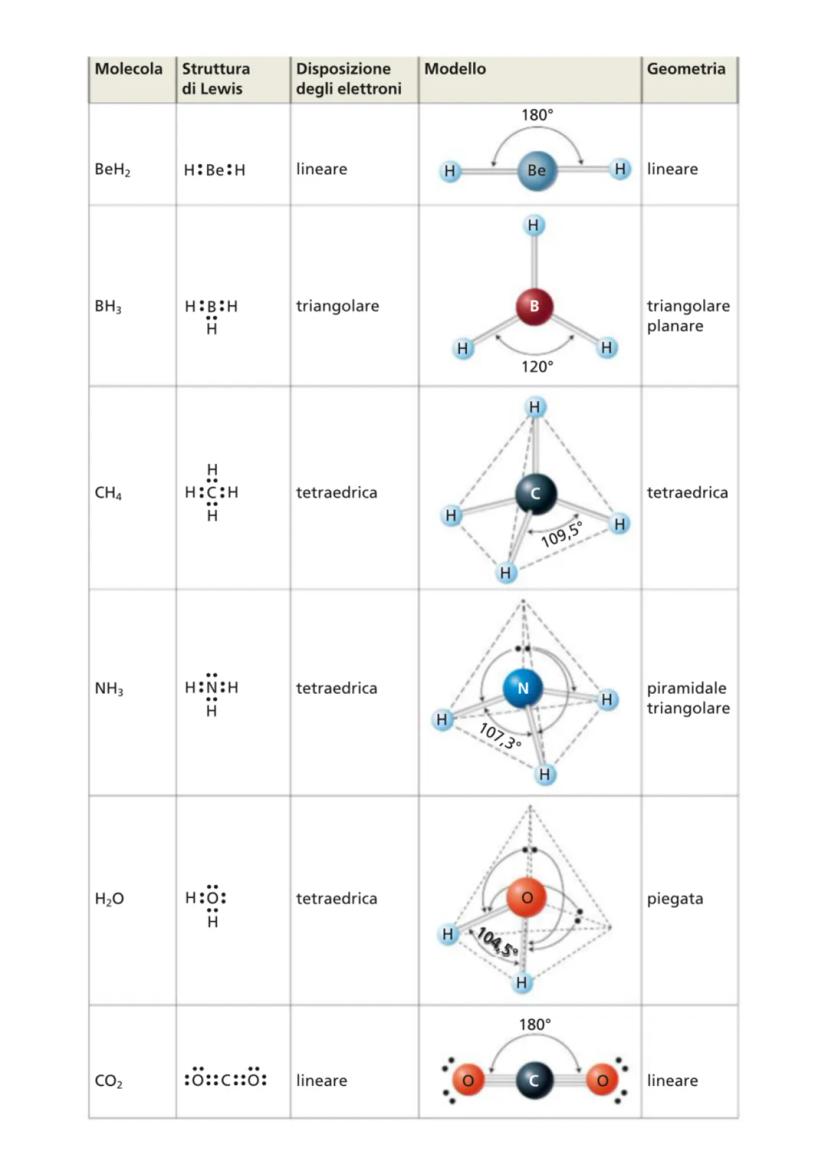
Le molecole assumono forme diverse in base alla disposizione delle coppie elettroniche attorno all'atomo centrale. Ecco alcune geometrie molecolari comuni:
Il berillio diidrato (BeH₂) ha una geometria lineare con angoli di 180° perché Be è circondato da due coppie elettroniche. Anche il monossido di carbonio (CO) presenta questa geometria.
Il borano (BH₃) ha una geometria triangolare planare con angoli di 120° poiché il boro è circondato da tre coppie elettroniche.
Il metano (CH₄) è tetraedrico con angoli di 109,5° perché il carbonio è circondato da quattro coppie elettroniche. Questa è una delle geometrie più comuni in chimica organica.
💡 Quando sono presenti coppie elettroniche libere sull'atomo centrale, la geometria reale della molecola differisce dalla disposizione teorica delle coppie elettroniche.
L'ammoniaca (NH₃) ha una geometria piramidale triangolare con angoli di 107,3° perché l'azoto ha una coppia elettronica libera oltre alle tre coppie condivise con gli idrogeni.
L'acqua (H₂O) ha una geometria piegata (o angolare) con un angolo di 104,5° perché l'ossigeno ha due coppie elettroniche libere oltre alle due coppie condivise con gli idrogeni.

L'acqua è una molecola con legami covalenti polari: l'ossigeno attira gli elettroni di legame, assumendo una carica parziale negativa, mentre gli idrogeni hanno una carica parziale positiva. Questa asimmetria rende l'acqua una molecola polare.
Il legame idrogeno è un'interazione fondamentale tra le molecole d'acqua e spiega molte delle sue proprietà uniche. Nel ghiaccio, i legami idrogeno formano un reticolo cristallino che occupa più spazio rispetto all'acqua liquida, rendendo il ghiaccio meno denso dell'acqua. Questa proprietà è fondamentale per la vita acquatica.
L'elevata tensione superficiale dell'acqua è dovuta all'attrazione tra le molecole: quelle in superficie sono attratte verso l'interno, creando una sorta di "pellicola". Questa proprietà, insieme alla capillarità (la capacità dell'acqua di risalire nei tubi sottili), è essenziale per il trasporto dell'acqua nelle piante.
💡 Senza i legami idrogeno, l'acqua non esisterebbe allo stato liquido alle normali condizioni ambientali: fonderebbe a -100°C e bollirebbe a -91°C!
L'acqua è un eccellente solvente per composti ionici e molecole polari. Può causare la dissociazione ionica di composti come il sale e la ionizzazione di sostanze con legami covalenti polari come HCl. Le soluzioni risultanti, contenenti ioni, sono dette "elettrolitiche" perché conducono elettricità.
L'acqua ha anche un elevato calore specifico e calori latenti di fusione e vaporizzazione . Queste proprietà permettono all'acqua di regolare la temperatura del nostro pianeta e dei nostri corpi, rendendo possibile la vita come la conosciamo.
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
marle
@marlee_
I legami chimici sono fondamentali per comprendere come gli atomi interagiscono e formano composti. Questa interazione permette agli atomi di raggiungere una stabilità energetica che altrimenti non avrebbero come particelle isolate. Comprendere i diversi tipi di legami ci aiuta a... Mostra di più

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Gli atomi formano legami per raggiungere la stabilità energetica. Quando due atomi si uniscono, l'energia potenziale del sistema diminuisce, rendendo la formazione del legame vantaggiosa dal punto di vista energetico.
La formazione di legami chimici è un processo che libera energia. Per rompere questi stessi legami, dobbiamo fornire energia al sistema. L'energia di legame indica quanta energia è necessaria per separare gli atomi legati: più è grande questo valore, più forte è il legame.
Secondo la regola dell'ottetto, gli atomi sono particolarmente stabili quando hanno otto elettroni nel loro livello energetico più esterno. Per raggiungere questa configurazione, gli atomi possono cedere, acquistare o condividere elettroni. La valenza di un atomo rappresenta proprio il numero di elettroni che può mettere in gioco per formare legami.
💡 Il legame ionico si forma quando un metallo cede elettroni a un non metallo. L'attrazione elettrostatica tra gli ioni di carica opposta che si formano è ciò che tiene uniti gli atomi nel composto.
Nel legame ionico, la forza di attrazione aumenta con la carica degli ioni e diminuisce con le loro dimensioni. I metalli dei primi tre gruppi tendono a perdere elettroni e diventare cationi, mentre i non metalli degli ultimi tre gruppi tendono ad acquistarne per diventare anioni.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Il legame metallico è responsabile delle proprietà caratteristiche dei metalli. In questo tipo di legame, gli ioni positivi dei metalli formano un reticolo cristallino mentre gli elettroni di valenza si muovono liberamente, creando una "nube elettronica" che avvolge tutti i cationi.
La forza del legame metallico dipende dalla carica nucleare: aumenta quando cresce la forza con cui il nucleo attrae gli elettroni. Nei metalli di transizione, anche gli elettroni degli orbitali d e f partecipano alla formazione della nuvola elettronica, creando alcune eccezioni nella forza del legame.
Il legame covalente si forma quando due atomi condividono una o più coppie di elettroni. Entrambi gli atomi esercitano una forza di attrazione sui medesimi elettroni, raggiungendo così la configurazione stabile del gas nobile più vicino. Possiamo rappresentare questo tipo di legame con le formule di Lewis.
💡 Quando gli atomi condividono due o tre coppie di elettroni, si formano legami multipli (doppi o tripli), che sono più forti e più corti dei legami semplici.
Nel legame covalente dativo, la coppia di elettroni condivisa proviene da un solo atomo (donatore), mentre l'altro (accettore) la utilizza per completare il proprio ottetto. Questo tipo di legame si rappresenta con una freccia e spiega la formazione dei composti di coordinazione, dove un metallo viene circondato da atomi donatori di elettroni.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La polarità di un legame dipende dalla differenza di elettronegatività tra gli atomi coinvolti. Quando due atomi identici formano un legame, si ha un legame covalente puro. Se invece gli atomi sono diversi, si crea un dipolo elettrico (legame covalente polare).
Possiamo classificare i legami in base alla differenza di elettronegatività (Δe):
Per rappresentare le strutture molecolari usiamo le formule di Lewis, seguendo alcuni passaggi fondamentali: stabilire la disposizione degli atomi, contare gli elettroni di valenza, rappresentare i legami semplici, completare gli ottetti e, se necessario, disegnare i legami multipli.
La teoria VSEPR (Valence Shell Electron Pair Repulsion) ci permette di prevedere la forma delle molecole. Secondo questa teoria, le coppie di elettroni del livello di valenza si respingono e tendono a disporsi il più lontano possibile le une dalle altre.
💡 La geometria di una molecola dipende dal numero totale di coppie elettroniche (sia condivise che non condivise) attorno all'atomo centrale.
Il numero di coppie elettroniche determina la struttura molecolare:

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La polarità di una molecola non dipende solo dalla presenza di legami covalenti polari, ma anche dalla sua geometria. Le molecole elementari (formate da atomi uguali) sono sempre non polari, mentre i composti biatomici con atomi diversi sono sempre polari.
Per le molecole poliatomiche, ogni legame covalente polare origina un dipolo elettrico caratterizzato dal suo momento dipolare (μ), misurato in Debye (D). Una molecola è polare quando la somma vettoriale di tutti i momenti dipolari è diversa da zero.
Le molecole sono apolari solo quando l'atomo centrale è legato a gruppi identici e non presenta coppie di elettroni liberi. Alcune molecole complesse possono avere sia parti polari che apolari, caratteristica importante per la loro solubilità.
💡 Il principio "il simile scioglie il simile" spiega perché sostanze polari si sciolgono in solventi polari (come l'acqua) e sostanze apolari in solventi apolari.
La repulsione tra le coppie elettroniche varia in intensità: la repulsione tra due coppie libere è maggiore di quella tra una coppia libera e una condivisa, che a sua volta è maggiore della repulsione tra due coppie condivise. Questo influenza gli angoli di legame reali, che possono differire dai valori ideali previsti dalla teoria VSEPR.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
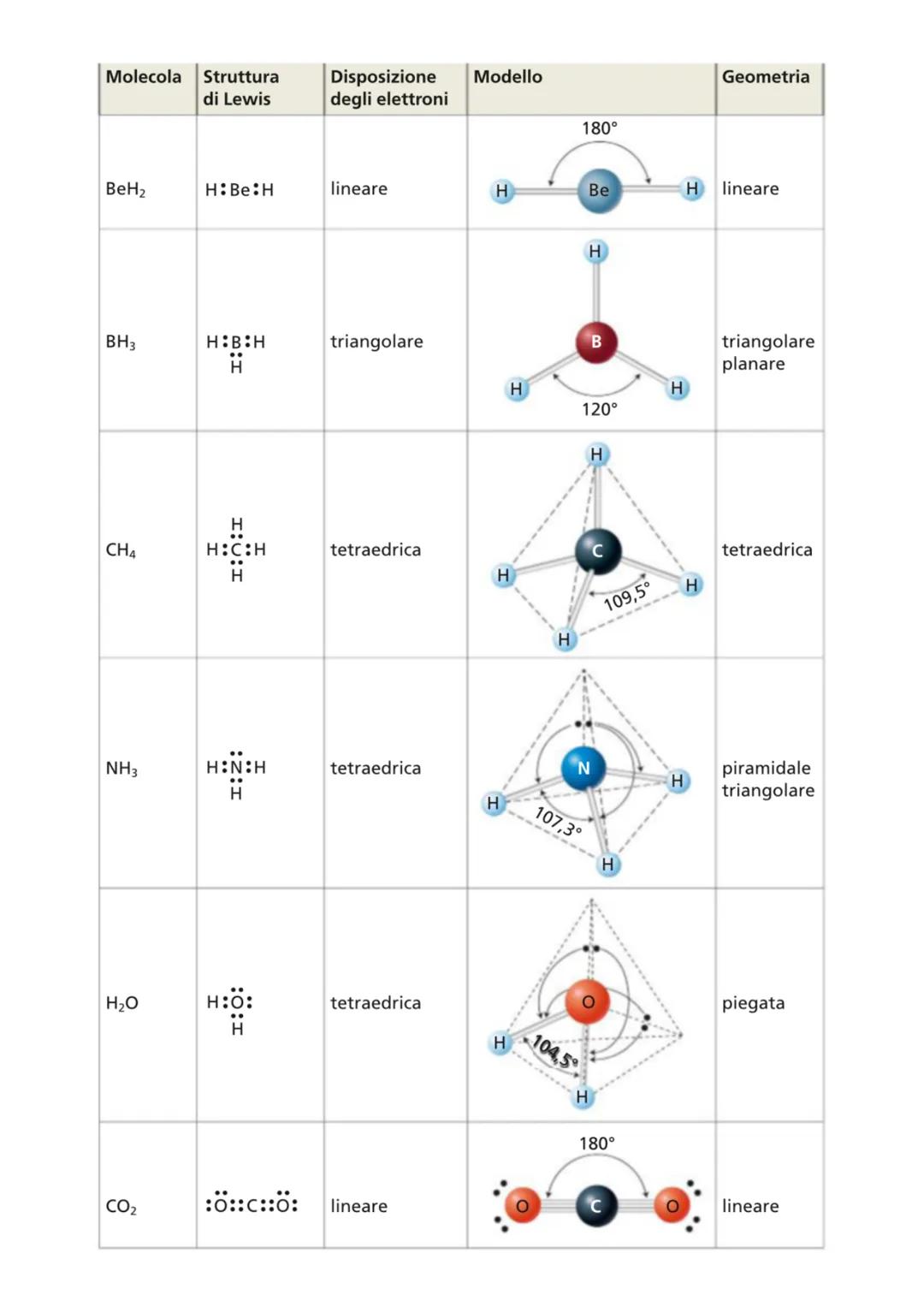
Le molecole assumono forme diverse in base alla disposizione delle coppie elettroniche attorno all'atomo centrale. Ecco alcune geometrie molecolari comuni:
Il berillio diidrato (BeH₂) ha una geometria lineare con angoli di 180° perché Be è circondato da due coppie elettroniche. Anche il monossido di carbonio (CO) presenta questa geometria.
Il borano (BH₃) ha una geometria triangolare planare con angoli di 120° poiché il boro è circondato da tre coppie elettroniche.
Il metano (CH₄) è tetraedrico con angoli di 109,5° perché il carbonio è circondato da quattro coppie elettroniche. Questa è una delle geometrie più comuni in chimica organica.
💡 Quando sono presenti coppie elettroniche libere sull'atomo centrale, la geometria reale della molecola differisce dalla disposizione teorica delle coppie elettroniche.
L'ammoniaca (NH₃) ha una geometria piramidale triangolare con angoli di 107,3° perché l'azoto ha una coppia elettronica libera oltre alle tre coppie condivise con gli idrogeni.
L'acqua (H₂O) ha una geometria piegata (o angolare) con un angolo di 104,5° perché l'ossigeno ha due coppie elettroniche libere oltre alle due coppie condivise con gli idrogeni.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
L'acqua è una molecola con legami covalenti polari: l'ossigeno attira gli elettroni di legame, assumendo una carica parziale negativa, mentre gli idrogeni hanno una carica parziale positiva. Questa asimmetria rende l'acqua una molecola polare.
Il legame idrogeno è un'interazione fondamentale tra le molecole d'acqua e spiega molte delle sue proprietà uniche. Nel ghiaccio, i legami idrogeno formano un reticolo cristallino che occupa più spazio rispetto all'acqua liquida, rendendo il ghiaccio meno denso dell'acqua. Questa proprietà è fondamentale per la vita acquatica.
L'elevata tensione superficiale dell'acqua è dovuta all'attrazione tra le molecole: quelle in superficie sono attratte verso l'interno, creando una sorta di "pellicola". Questa proprietà, insieme alla capillarità (la capacità dell'acqua di risalire nei tubi sottili), è essenziale per il trasporto dell'acqua nelle piante.
💡 Senza i legami idrogeno, l'acqua non esisterebbe allo stato liquido alle normali condizioni ambientali: fonderebbe a -100°C e bollirebbe a -91°C!
L'acqua è un eccellente solvente per composti ionici e molecole polari. Può causare la dissociazione ionica di composti come il sale e la ionizzazione di sostanze con legami covalenti polari come HCl. Le soluzioni risultanti, contenenti ioni, sono dette "elettrolitiche" perché conducono elettricità.
L'acqua ha anche un elevato calore specifico e calori latenti di fusione e vaporizzazione . Queste proprietà permettono all'acqua di regolare la temperatura del nostro pianeta e dei nostri corpi, rendendo possibile la vita come la conosciamo.
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
70
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
Regola ottetto e valenza, legame covalente (polare e apolare), legame ionico, legame metallico, legame dativo, forze dipolo-dipolo, forze di london, legame a idrogeno, ione dipolo, vsepr
legami chimici (cap.11): legame ionico, legame metallico, legame covalente e covalente dativo, la forma delle molecole, la teoria di vespr e molecole polari e a polari
Chimica
Le particelle subatomiche, gli ioni, i cationi e gli isotopi.
Massa atomica, massa molecolare e peso formula, mole, costante di Avogadro, volume molare, equazione di stato dei gas, diffusione e legge di Graham, composizione percentuale, formula minima e molecolare.
1) La vita dipende dall’acqua(1 a 4) 2)Le biomolecole(5-6) 3) I carboidrati(7-8) 4) I lipidi(9-10) 5) Le proteine(11 a 13) 6) Gli acidi nucleici(14)
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS