Preparati a scoprire cosa c'è davvero dentro gli atomi! Quello... Mostra di più
Introduzione agli Atomi e ai Principi della Chimica









La Scoperta delle Particelle Subatomiche
Ti sei mai chiesto cosa succede quando rompi qualcosa di "indivisibile"? Nel 1808 John Dalton pensava che gli atomi fossero davvero indivisibili, come dice il nome stesso. La sua teoria atomica era semplice: materia fatta di atomi piccolissimi e indistruttibili, tutti identici per lo stesso elemento.
Ma tra il XIII e XIX secolo altri scienziati hanno fatto scoperte che hanno mandato in frantumi questa idea! Hanno scoperto che gli atomi contengono particelle subatomiche: elettroni e protoni. Questo significa che gli atomi sono divisibili e hanno una struttura interna complessa.
La teoria di Dalton è stata superata perché ora sappiamo che gli atomi possono avere masse diverse anche se appartengono allo stesso elemento (sono gli isotopi) e hanno una struttura con nucleo e orbite elettroniche studiata da Rutherford e Bohr.
💡 Curiosità: Il nome "atomo" viene dal greco e significa "non tagliabile", ma oggi sappiamo che si può proprio tagliare!

La Natura Elettrica della Materia e la Radioattività
Hai mai strofinato una penna sui capelli e poi attirato pezzetti di carta? Congratulazioni, hai appena creato carica elettrica! Esistono due tipi di cariche: positive (come il vetro strofinato) e negative (come il plexiglass).
La legge di Coulomb ci spiega come funziona l'attrazione e la repulsione: cariche uguali si respingono, cariche opposte si attraggono. La forza dipende dal prodotto delle cariche diviso il quadrato della distanza. È come un'equazione dell'amore elettrico!
Nel XIX secolo gli scienziati hanno scoperto la radioattività: alcuni elementi instabili si trasformano emettendo radiazioni α, β e γ. I raggi α sono poco penetranti, i raggi β sono elettroni molto penetranti, mentre i raggi γ sono radiazioni elettromagnetiche super pericolose.
⚠️ Attenzione: La radioattività può essere pericolosa, ma è anche utile in medicina e per datare fossili antichi!

Elettroni, Protoni e Neutroni: La Famiglia Subatomica
Immagina di dover scoprire cosa c'è dentro una scatola chiusa usando solo degli strumenti strani. Questo è quello che hanno fatto gli scienziati con il tubo catodico! Goldstein, Crookes e Thompson hanno scoperto l'elettrone studiando i raggi catodici: particelle negative che vanno dal catodo all'anodo.
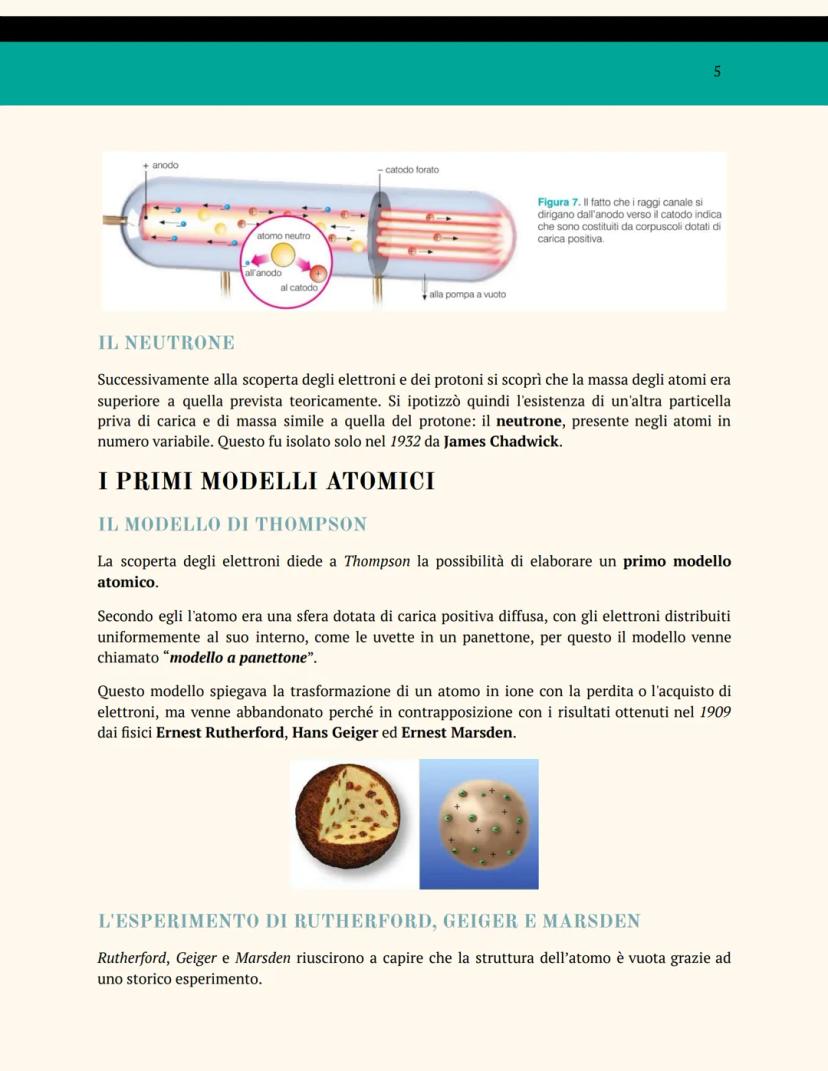
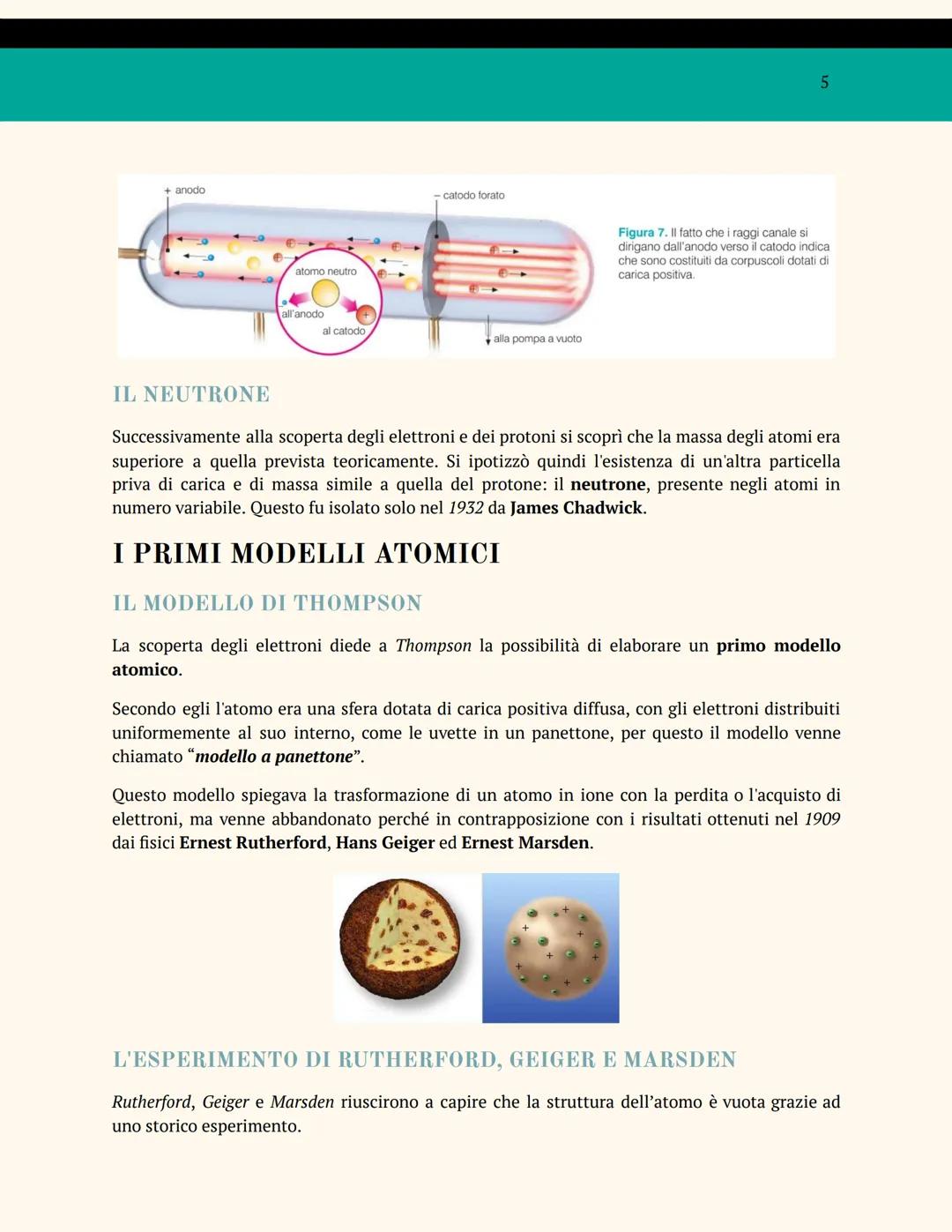
Il protone è stato scoperto sempre con il tubo catodico, ma stavolta con il catodo forato. Goldstein ha visto i raggi canale che andavano in direzione opposta agli elettroni: erano particelle positive più pesanti degli elettroni.
Il neutrone è stato l'ultimo ad essere scoperto nel 1932 da James Chadwick. Gli scienziati si erano accorti che la massa degli atomi era maggiore del previsto, quindi doveva esserci qualcos'altro: una particella senza carica ma con massa simile al protone.
🔬 Fun fact: Il tubo catodico era la tecnologia dietro i vecchi televisori! Guardare la TV significava vedere elettroni che colpivano uno schermo.

I Primi Modelli Atomici
Thompson ha proposto il primo modello atomico dopo aver scoperto gli elettroni: immaginava l'atomo come un panettone! Una sfera positiva con gli elettroni distribuiti dentro come uvette. Carino, ma sbagliato.
Nel 1909 Rutherford, Geiger e Marsden hanno fatto un esperimento geniale: hanno sparato particelle α contro una lamina d'oro sottilissima. La maggior parte passava indisturbata, ma alcune venivano deviate o respinte. Questo significava una cosa incredibile: l'atomo è praticamente vuoto!
Solo una particella su 100.000 veniva deviata, dimostrando che solo una particella su 1000 atomi incontrava qualcosa di solido: il nucleo. È come sparare pallini da ping pong contro una rete da calcio e vedere che ogni tanto uno rimbalza indietro.
🎯 Visualizza: Se un atomo fosse grande come uno stadio, il nucleo sarebbe grande come una biglia al centro del campo!
Il Modello Planetario e le Caratteristiche del Nucleo
Rutherford ha creato il modello planetario: l'atomo come un sistema solare con il nucleo al centro (il Sole) e gli elettroni che orbitano intorno (i pianeti). Il nucleo contiene quasi tutta la massa dell'atomo ed è carico positivamente.
Ma c'era un problema: perché gli elettroni non cadono sul nucleo? Rutherford ha ipotizzato un equilibrio tra due forze: la forza elettrostatica attrattiva che tira l'elettrone verso il nucleo, e la forza centrifuga che lo mantiene in orbita.
Con la scoperta dei neutroni, si è capito che nel nucleo ci sono anche particelle che fanno da "cuscinetto" tra i protoni, evitando che si respingano a vicenda. I neutroni sono come i mediatori di pace del nucleo atomico!
🌟 Ricorda: Il modello planetario è superato ma ancora utile per capire la struttura base dell'atomo!

Numero Atomico, Massa e Isotopi
Il numero atomico Z è come la carta d'identità dell'elemento: indica quanti protoni ci sono nel nucleo. Tutti gli atomi dello stesso elemento hanno lo stesso Z. Il numero di massa A è la somma di protoni e neutroni nel nucleo.
Gli isotopi sono atomi dello stesso elemento (stesso Z) ma con diverso numero di neutroni (diverso A). È come avere fratelli con lo stesso cognome ma peso diverso! L'idrogeno ha tre isotopi: prozio (solo un protone), deuterio , e trizio .
Il carbonio-14 è un isotopo radioattivo famoso perché viene usato per datare i fossili. La massa atomica degli elementi non è mai un numero intero perché è la media pesata di tutti gli isotopi naturali.
📊 Dato interessante: Il carbonio normale rappresenta il 98,9% del carbonio in natura!

Ioni: Quando gli Atomi si Caricano
Quando un atomo perde o guadagna elettroni diventa uno ione. Se perde elettroni diventa un catione (ione positivo) come Ca²⁺ o Na⁺. Se guadagna elettroni diventa un anione (ione negativo) come Cl⁻ o F⁻.
È importante ricordare che il numero di protoni non cambia mai: quello che varia è solo il numero di elettroni. Gli ioni sono fondamentali per capire come si formano i composti chimici e le reazioni.
⚡ Trucco mnemonico: Catione = gatto = positivo (i gatti sono carini e positivi), Anione = arrabbiato = negativo!

La Luce: Onda o Particella?
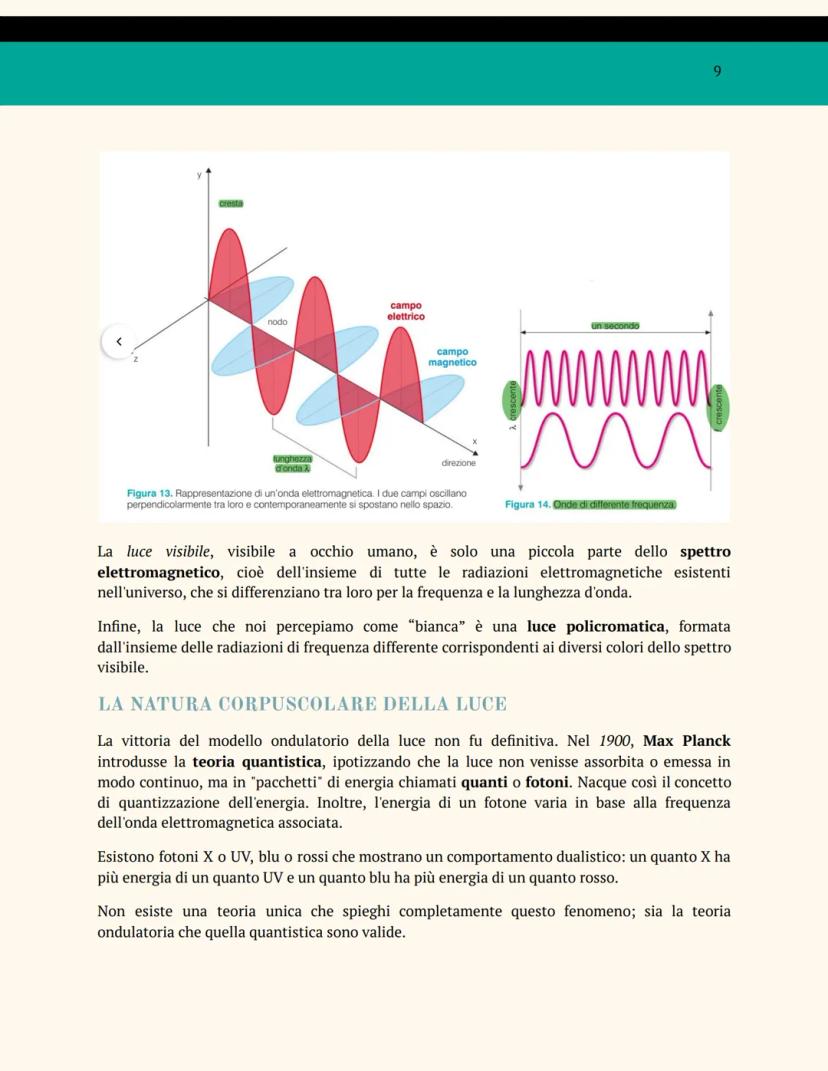
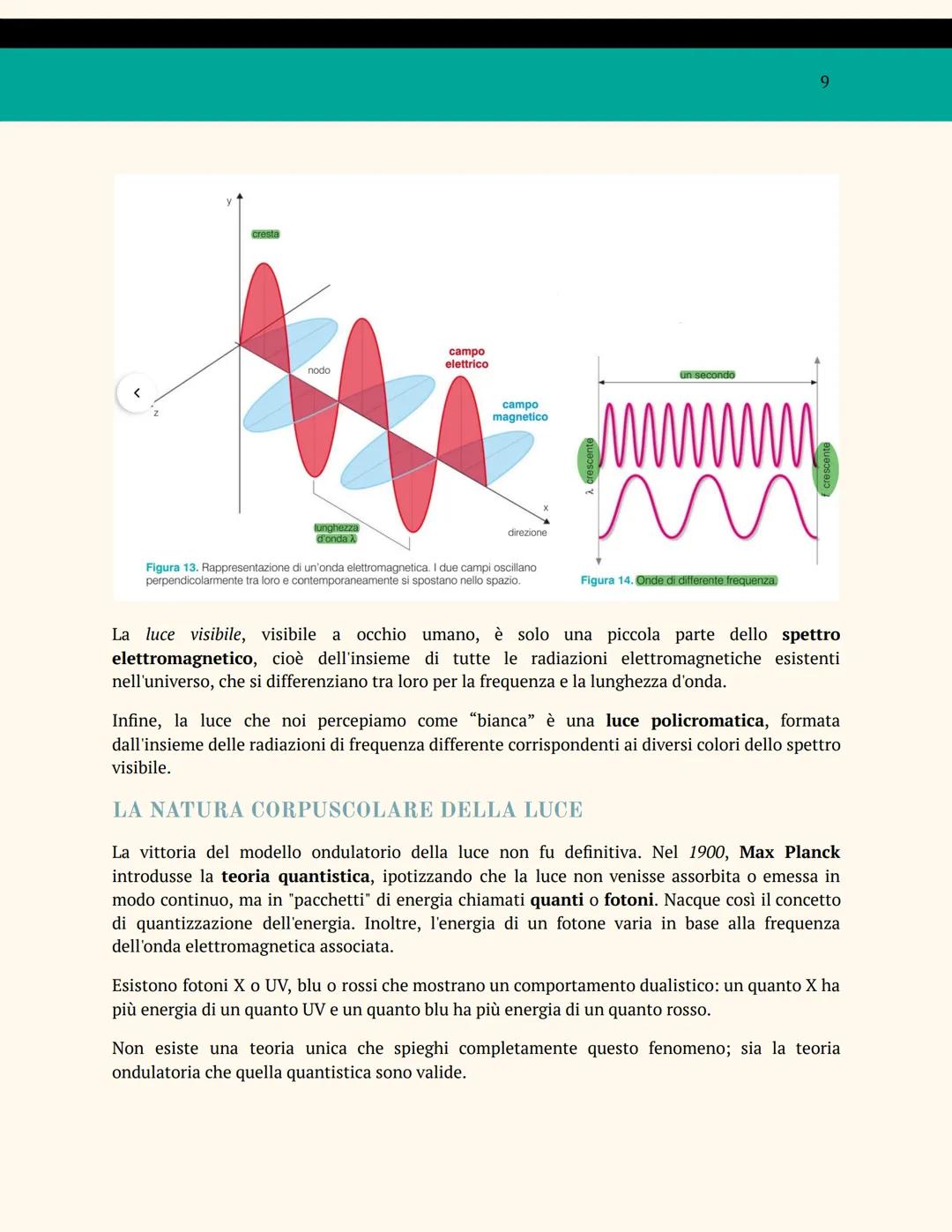
La luce ha una doppia personalità! James Maxwell nel XIX secolo dimostrò che è un'onda elettromagnetica: energia che si propaga senza trasportare materia, con un campo elettrico e uno magnetico che oscillano perpendicolarmente.
Le onde sono caratterizzate da lunghezza d'onda λ (distanza tra due creste), frequenza f (numero di creste al secondo), e velocità di propagazione. La luce visibile è solo una piccola parte dello spettro elettromagnetico.
Nel 1900 Max Planck ha introdotto la teoria quantistica: la luce viene assorbita ed emessa in "pacchetti" chiamati quanti o fotoni. L'energia di ogni fotone dipende dalla frequenza: i fotoni blu hanno più energia di quelli rossi.
🌈 Wow: La luce bianca è in realtà un mix di tutti i colori dello spettro visibile!
Il Dualismo Onda-Particella e il Modello di Bohr
La luce ha un comportamento dualistico: si comporta come onda quando si propaga e come particelle quando interagisce con la materia. Non esiste una teoria unica, entrambe le descrizioni sono valide contemporaneamente!
Il modello di Rutherford aveva un problema: secondo la fisica classica, gli elettroni in movimento dovrebbero perdere energia e cadere sul nucleo. Ma questo non succede! Nel 1913 Niels Bohr ha risolto il mistero con il modello atomico a strati.
Bohr ha applicato la quantizzazione dell'energia agli atomi: gli elettroni possono stare solo in orbite stazionarie con livelli energetici definiti. Quando assorbono energia "saltano" a livelli superiori, ma poi tornano giù emettendo luce specifica.
🪜 Metafora perfetta: L'elettrone si comporta come una biglia su delle scale: può stare solo sui gradini, non a metà strada!

Dal Modello di Bohr agli Orbitali
Nel modello di Bohr, ogni transizione discendente dell'elettrone emette un quanto di energia specifico, creando gli spettri a righe caratteristici di ogni elemento. È come se ogni elemento avesse la sua firma luminosa!
Arnold Sommerfeld ha perfezionato il modello aggiungendo orbite ellittiche oltre a quelle circolari. Però il modello di Bohr funzionava bene solo per l'idrogeno: con atomi più complessi le previsioni non erano accurate.
Questo ha portato allo sviluppo della meccanica quantistica moderna, dove si passa dal concetto di orbita (traiettoria definita) a quello di orbitale (zona di probabilità dove trovare l'elettrone).
🎯 Evoluzione: Dalla palla da biliardo di Dalton alla nuvola di probabilità quantistica - che viaggio incredibile!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: 科学 (かがく)
9L’atomo
Descrizione generale dell’atomo e i 4 modelli atomici
Gli orbitali atomici,i numeri quantici,lo spin e la configurazione elettronica.
Appunti sugli orbitali atomici,i numeri quantici,lo spin e la configurazione elettronica.
legami chimici
Legami chimici
atomo
riassunto atomo
CINETICA CHIMICA
Appunti di chimica sulla cinetica di reazione di quarta liceo scientifico - scienze applicate
I metodi di separazione dei miscugli
-chimica-
Teorie atomiche
Le teorie atomiche e la configurazione elettronica
trasformazioni fisiche della materia
gli stati della materia, sistemi omogenei e eterogenei, sostanze pure e miscugli
le trasformazioni fisiche della materia
gli stati fisici della materia
Contenuti più popolari di Chimica
9Nomenclatura
Nomenclatura chimica inorganica
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Le biomolecole
Appunti sulle biomolecole approfonditi: introduzione, carboidrati, lipidi, proteine e acidi nucleici
APPUNTI DNA ED RNA
Tutto il DNA con la duplicazione del DNA. Tutto l’RNA con trascrizione e traduzione
i legami chimici
i legami chimici
Legami chimici pdf
Legami covalenti, ionici e metallici
Le cellule 🧫
Cellula provariote, cellula eucariote animale e cellula eucariote vegetale.
replicazione del DNA
struttura doppia elica DNA, replicazione DNA, complesso di replicazione, DNA polimerasi, telomeri
Il Metabolismo
Appunti del metabolismo che comprendono: metabolismo del glucosio (glicolisi, respirazione cellulare e fermentazione), metabolismo degli zuccheri (Glicogenosintesi, Glicogenolisi), Gluconeogenesi, metabolismo dei lipidi, catabolismo degli amminoacidi
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Introduzione agli Atomi e ai Principi della Chimica
Preparati a scoprire cosa c'è davvero dentro gli atomi! Quello che sembrava indivisibile si è rivelato un universo in miniatura pieno di particelle elettriche, energie quantizzate e strutture complesse che hanno rivoluzionato la nostra comprensione della materia.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
La Scoperta delle Particelle Subatomiche
Ti sei mai chiesto cosa succede quando rompi qualcosa di "indivisibile"? Nel 1808 John Dalton pensava che gli atomi fossero davvero indivisibili, come dice il nome stesso. La sua teoria atomica era semplice: materia fatta di atomi piccolissimi e indistruttibili, tutti identici per lo stesso elemento.
Ma tra il XIII e XIX secolo altri scienziati hanno fatto scoperte che hanno mandato in frantumi questa idea! Hanno scoperto che gli atomi contengono particelle subatomiche: elettroni e protoni. Questo significa che gli atomi sono divisibili e hanno una struttura interna complessa.
La teoria di Dalton è stata superata perché ora sappiamo che gli atomi possono avere masse diverse anche se appartengono allo stesso elemento (sono gli isotopi) e hanno una struttura con nucleo e orbite elettroniche studiata da Rutherford e Bohr.
💡 Curiosità: Il nome "atomo" viene dal greco e significa "non tagliabile", ma oggi sappiamo che si può proprio tagliare!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
La Natura Elettrica della Materia e la Radioattività
Hai mai strofinato una penna sui capelli e poi attirato pezzetti di carta? Congratulazioni, hai appena creato carica elettrica! Esistono due tipi di cariche: positive (come il vetro strofinato) e negative (come il plexiglass).
La legge di Coulomb ci spiega come funziona l'attrazione e la repulsione: cariche uguali si respingono, cariche opposte si attraggono. La forza dipende dal prodotto delle cariche diviso il quadrato della distanza. È come un'equazione dell'amore elettrico!
Nel XIX secolo gli scienziati hanno scoperto la radioattività: alcuni elementi instabili si trasformano emettendo radiazioni α, β e γ. I raggi α sono poco penetranti, i raggi β sono elettroni molto penetranti, mentre i raggi γ sono radiazioni elettromagnetiche super pericolose.
⚠️ Attenzione: La radioattività può essere pericolosa, ma è anche utile in medicina e per datare fossili antichi!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Elettroni, Protoni e Neutroni: La Famiglia Subatomica
Immagina di dover scoprire cosa c'è dentro una scatola chiusa usando solo degli strumenti strani. Questo è quello che hanno fatto gli scienziati con il tubo catodico! Goldstein, Crookes e Thompson hanno scoperto l'elettrone studiando i raggi catodici: particelle negative che vanno dal catodo all'anodo.
Il protone è stato scoperto sempre con il tubo catodico, ma stavolta con il catodo forato. Goldstein ha visto i raggi canale che andavano in direzione opposta agli elettroni: erano particelle positive più pesanti degli elettroni.
Il neutrone è stato l'ultimo ad essere scoperto nel 1932 da James Chadwick. Gli scienziati si erano accorti che la massa degli atomi era maggiore del previsto, quindi doveva esserci qualcos'altro: una particella senza carica ma con massa simile al protone.
🔬 Fun fact: Il tubo catodico era la tecnologia dietro i vecchi televisori! Guardare la TV significava vedere elettroni che colpivano uno schermo.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
I Primi Modelli Atomici
Thompson ha proposto il primo modello atomico dopo aver scoperto gli elettroni: immaginava l'atomo come un panettone! Una sfera positiva con gli elettroni distribuiti dentro come uvette. Carino, ma sbagliato.
Nel 1909 Rutherford, Geiger e Marsden hanno fatto un esperimento geniale: hanno sparato particelle α contro una lamina d'oro sottilissima. La maggior parte passava indisturbata, ma alcune venivano deviate o respinte. Questo significava una cosa incredibile: l'atomo è praticamente vuoto!
Solo una particella su 100.000 veniva deviata, dimostrando che solo una particella su 1000 atomi incontrava qualcosa di solido: il nucleo. È come sparare pallini da ping pong contro una rete da calcio e vedere che ogni tanto uno rimbalza indietro.
🎯 Visualizza: Se un atomo fosse grande come uno stadio, il nucleo sarebbe grande come una biglia al centro del campo!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Il Modello Planetario e le Caratteristiche del Nucleo
Rutherford ha creato il modello planetario: l'atomo come un sistema solare con il nucleo al centro (il Sole) e gli elettroni che orbitano intorno (i pianeti). Il nucleo contiene quasi tutta la massa dell'atomo ed è carico positivamente.
Ma c'era un problema: perché gli elettroni non cadono sul nucleo? Rutherford ha ipotizzato un equilibrio tra due forze: la forza elettrostatica attrattiva che tira l'elettrone verso il nucleo, e la forza centrifuga che lo mantiene in orbita.
Con la scoperta dei neutroni, si è capito che nel nucleo ci sono anche particelle che fanno da "cuscinetto" tra i protoni, evitando che si respingano a vicenda. I neutroni sono come i mediatori di pace del nucleo atomico!
🌟 Ricorda: Il modello planetario è superato ma ancora utile per capire la struttura base dell'atomo!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Numero Atomico, Massa e Isotopi
Il numero atomico Z è come la carta d'identità dell'elemento: indica quanti protoni ci sono nel nucleo. Tutti gli atomi dello stesso elemento hanno lo stesso Z. Il numero di massa A è la somma di protoni e neutroni nel nucleo.
Gli isotopi sono atomi dello stesso elemento (stesso Z) ma con diverso numero di neutroni (diverso A). È come avere fratelli con lo stesso cognome ma peso diverso! L'idrogeno ha tre isotopi: prozio (solo un protone), deuterio , e trizio .
Il carbonio-14 è un isotopo radioattivo famoso perché viene usato per datare i fossili. La massa atomica degli elementi non è mai un numero intero perché è la media pesata di tutti gli isotopi naturali.
📊 Dato interessante: Il carbonio normale rappresenta il 98,9% del carbonio in natura!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Ioni: Quando gli Atomi si Caricano
Quando un atomo perde o guadagna elettroni diventa uno ione. Se perde elettroni diventa un catione (ione positivo) come Ca²⁺ o Na⁺. Se guadagna elettroni diventa un anione (ione negativo) come Cl⁻ o F⁻.
È importante ricordare che il numero di protoni non cambia mai: quello che varia è solo il numero di elettroni. Gli ioni sono fondamentali per capire come si formano i composti chimici e le reazioni.
⚡ Trucco mnemonico: Catione = gatto = positivo (i gatti sono carini e positivi), Anione = arrabbiato = negativo!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
La Luce: Onda o Particella?
La luce ha una doppia personalità! James Maxwell nel XIX secolo dimostrò che è un'onda elettromagnetica: energia che si propaga senza trasportare materia, con un campo elettrico e uno magnetico che oscillano perpendicolarmente.
Le onde sono caratterizzate da lunghezza d'onda λ (distanza tra due creste), frequenza f (numero di creste al secondo), e velocità di propagazione. La luce visibile è solo una piccola parte dello spettro elettromagnetico.
Nel 1900 Max Planck ha introdotto la teoria quantistica: la luce viene assorbita ed emessa in "pacchetti" chiamati quanti o fotoni. L'energia di ogni fotone dipende dalla frequenza: i fotoni blu hanno più energia di quelli rossi.
🌈 Wow: La luce bianca è in realtà un mix di tutti i colori dello spettro visibile!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Il Dualismo Onda-Particella e il Modello di Bohr
La luce ha un comportamento dualistico: si comporta come onda quando si propaga e come particelle quando interagisce con la materia. Non esiste una teoria unica, entrambe le descrizioni sono valide contemporaneamente!
Il modello di Rutherford aveva un problema: secondo la fisica classica, gli elettroni in movimento dovrebbero perdere energia e cadere sul nucleo. Ma questo non succede! Nel 1913 Niels Bohr ha risolto il mistero con il modello atomico a strati.
Bohr ha applicato la quantizzazione dell'energia agli atomi: gli elettroni possono stare solo in orbite stazionarie con livelli energetici definiti. Quando assorbono energia "saltano" a livelli superiori, ma poi tornano giù emettendo luce specifica.
🪜 Metafora perfetta: L'elettrone si comporta come una biglia su delle scale: può stare solo sui gradini, non a metà strada!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Dal Modello di Bohr agli Orbitali
Nel modello di Bohr, ogni transizione discendente dell'elettrone emette un quanto di energia specifico, creando gli spettri a righe caratteristici di ogni elemento. È come se ogni elemento avesse la sua firma luminosa!
Arnold Sommerfeld ha perfezionato il modello aggiungendo orbite ellittiche oltre a quelle circolari. Però il modello di Bohr funzionava bene solo per l'idrogeno: con atomi più complessi le previsioni non erano accurate.
Questo ha portato allo sviluppo della meccanica quantistica moderna, dove si passa dal concetto di orbita (traiettoria definita) a quello di orbitale (zona di probabilità dove trovare l'elettrone).
🎯 Evoluzione: Dalla palla da biliardo di Dalton alla nuvola di probabilità quantistica - che viaggio incredibile!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: 科学 (かがく)
9L’atomo
Descrizione generale dell’atomo e i 4 modelli atomici
Gli orbitali atomici,i numeri quantici,lo spin e la configurazione elettronica.
Appunti sugli orbitali atomici,i numeri quantici,lo spin e la configurazione elettronica.
legami chimici
Legami chimici
atomo
riassunto atomo
CINETICA CHIMICA
Appunti di chimica sulla cinetica di reazione di quarta liceo scientifico - scienze applicate
I metodi di separazione dei miscugli
-chimica-
Teorie atomiche
Le teorie atomiche e la configurazione elettronica
trasformazioni fisiche della materia
gli stati della materia, sistemi omogenei e eterogenei, sostanze pure e miscugli
le trasformazioni fisiche della materia
gli stati fisici della materia
Contenuti più popolari di Chimica
9Nomenclatura
Nomenclatura chimica inorganica
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Le biomolecole
Appunti sulle biomolecole approfonditi: introduzione, carboidrati, lipidi, proteine e acidi nucleici
APPUNTI DNA ED RNA
Tutto il DNA con la duplicazione del DNA. Tutto l’RNA con trascrizione e traduzione
i legami chimici
i legami chimici
Legami chimici pdf
Legami covalenti, ionici e metallici
Le cellule 🧫
Cellula provariote, cellula eucariote animale e cellula eucariote vegetale.
replicazione del DNA
struttura doppia elica DNA, replicazione DNA, complesso di replicazione, DNA polimerasi, telomeri
Il Metabolismo
Appunti del metabolismo che comprendono: metabolismo del glucosio (glicolisi, respirazione cellulare e fermentazione), metabolismo degli zuccheri (Glicogenosintesi, Glicogenolisi), Gluconeogenesi, metabolismo dei lipidi, catabolismo degli amminoacidi
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.