Preparati a padroneggiare la nomenclatura inorganica! Questa è la chiave... Mostra di più
Guida alla Nomenclatura Chimica Inorganica






Valenza e Numero di Ossidazione
La valenza è semplicemente il numero di legami che un atomo può formare. Per esempio, l'ossigeno ha valenza 2, l'idrogeno 1.
Il numero di ossidazione (n.o.) è la carica che un elemento avrebbe se tutti gli elettroni di legame fossero assegnati all'elemento più elettronegativo. Ogni elemento può avere più numeri di ossidazione diversi a seconda del composto.
Regole fondamentali per calcolare il n.o.:
- Nelle sostanze elementari, il n.o. è sempre 0
- Negli ioni, il n.o. corrisponde alla carica
- La somma dei n.o. in un composto neutro è sempre 0
Ricorda: L'ossigeno ha quasi sempre n.o. -2 , l'idrogeno +1 .
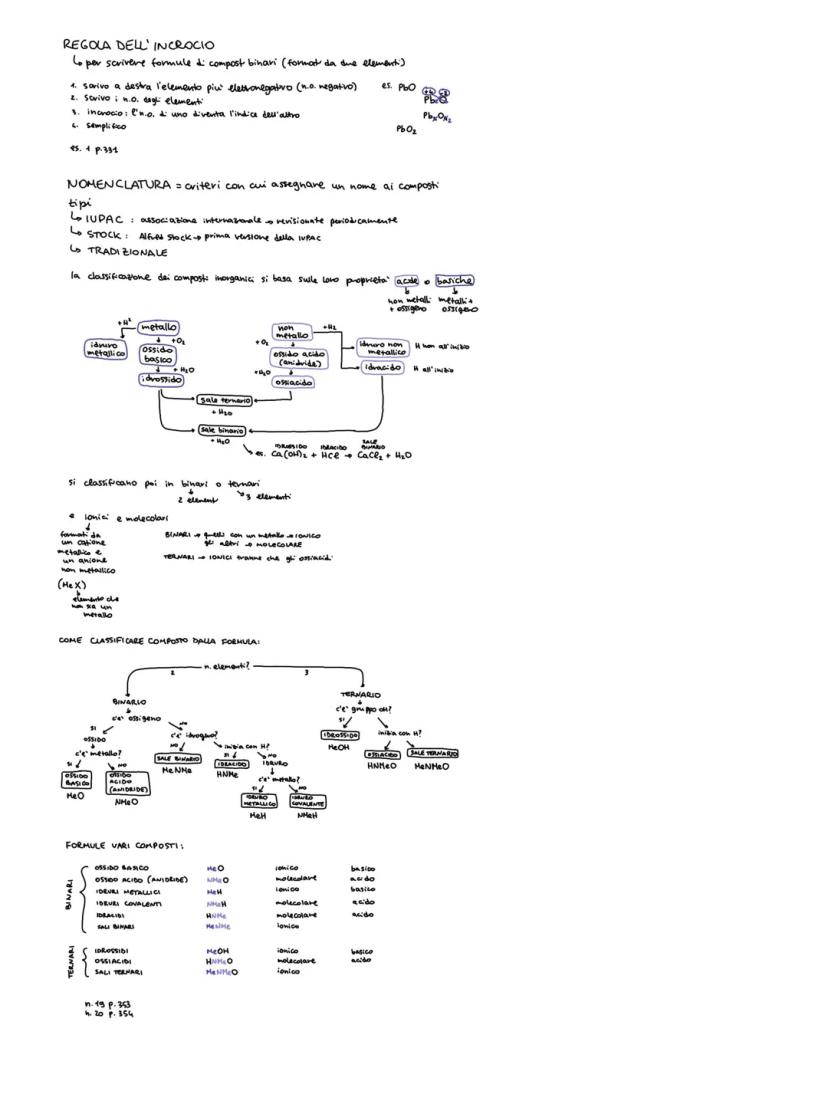
Regola dell'Incrocio e Nomenclatura
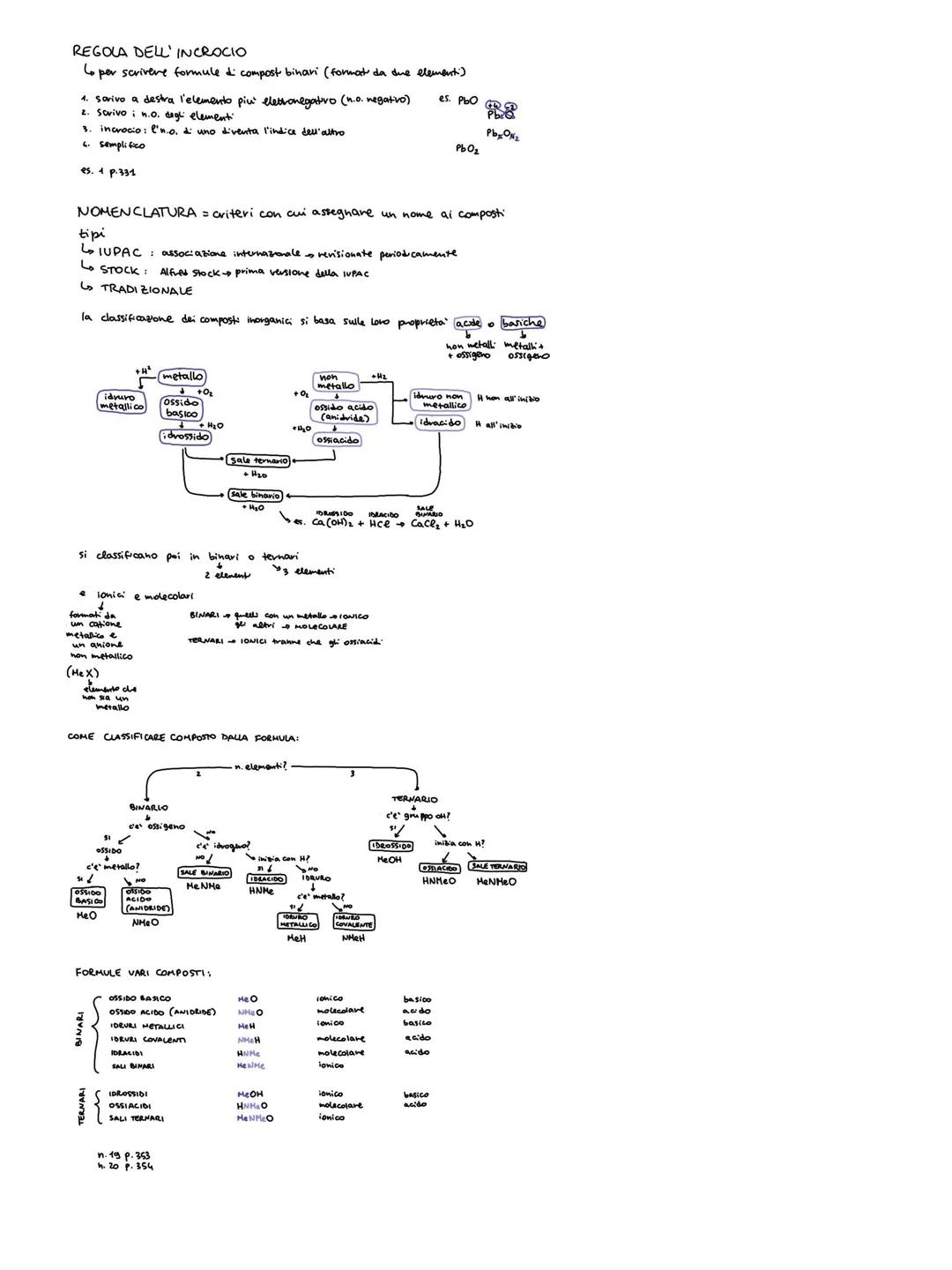
La regola dell'incrocio ti permette di scrivere facilmente le formule dei composti binari. Scrivi l'elemento più elettronegativo a destra, poi incrocia i numeri di ossidazione: quello di un elemento diventa l'indice dell'altro.
Esistono tre tipi di nomenclatura: IUPAC (quella ufficiale internazionale), Stock (versione semplificata) e tradizionale (quella più antica ma ancora usata).
I composti inorganici si classificano in base alle loro proprietà: acidi o basici, binari o ternari (2 o 3 elementi), ionici o molecolari.
Schema di classificazione rapida:
- Con ossigeno: ossidi basici (metalli) o acidi/anidridi (non metalli)
- Con idrogeno: idruri (senza ossigeno) o idracidi/ossiacidi
- Sali: derivano dalla combinazione di acidi e basi
Trucco: Per riconoscere un composto dalla formula, guarda prima quanti elementi ci sono, poi cerca ossigeno e idrogeno per capire la famiglia.
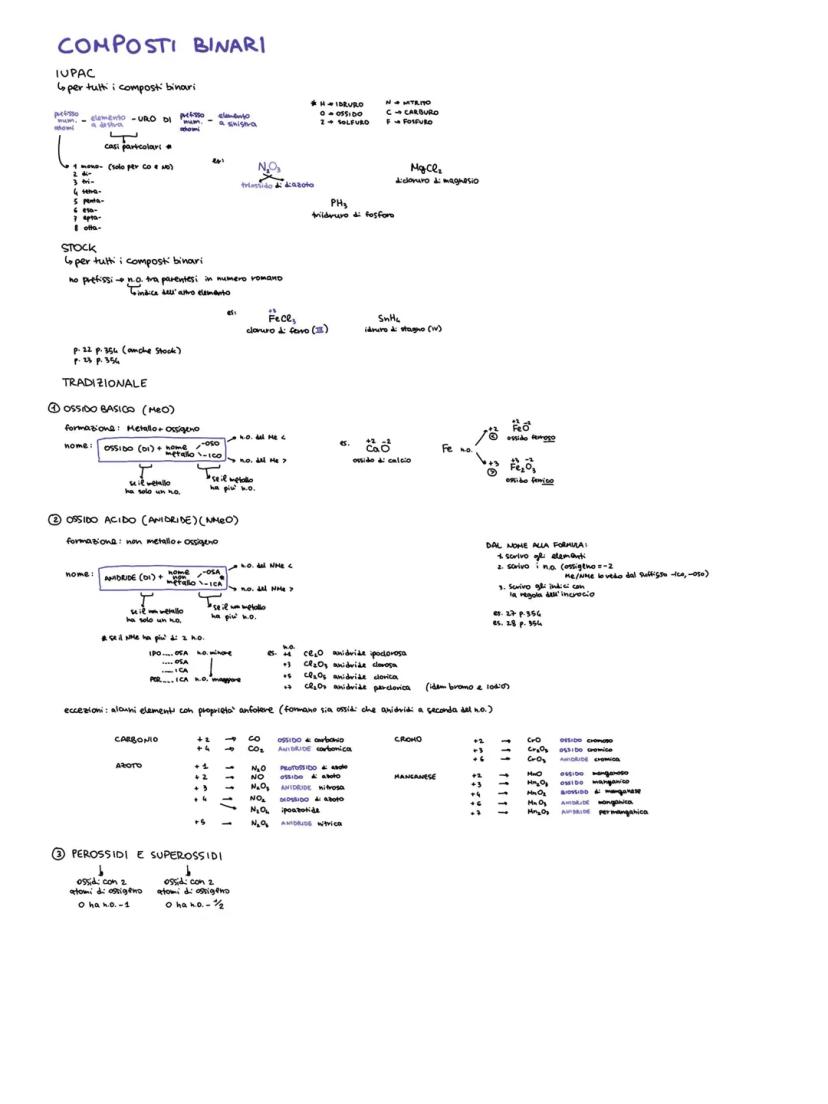
Composti Binari - Ossidi
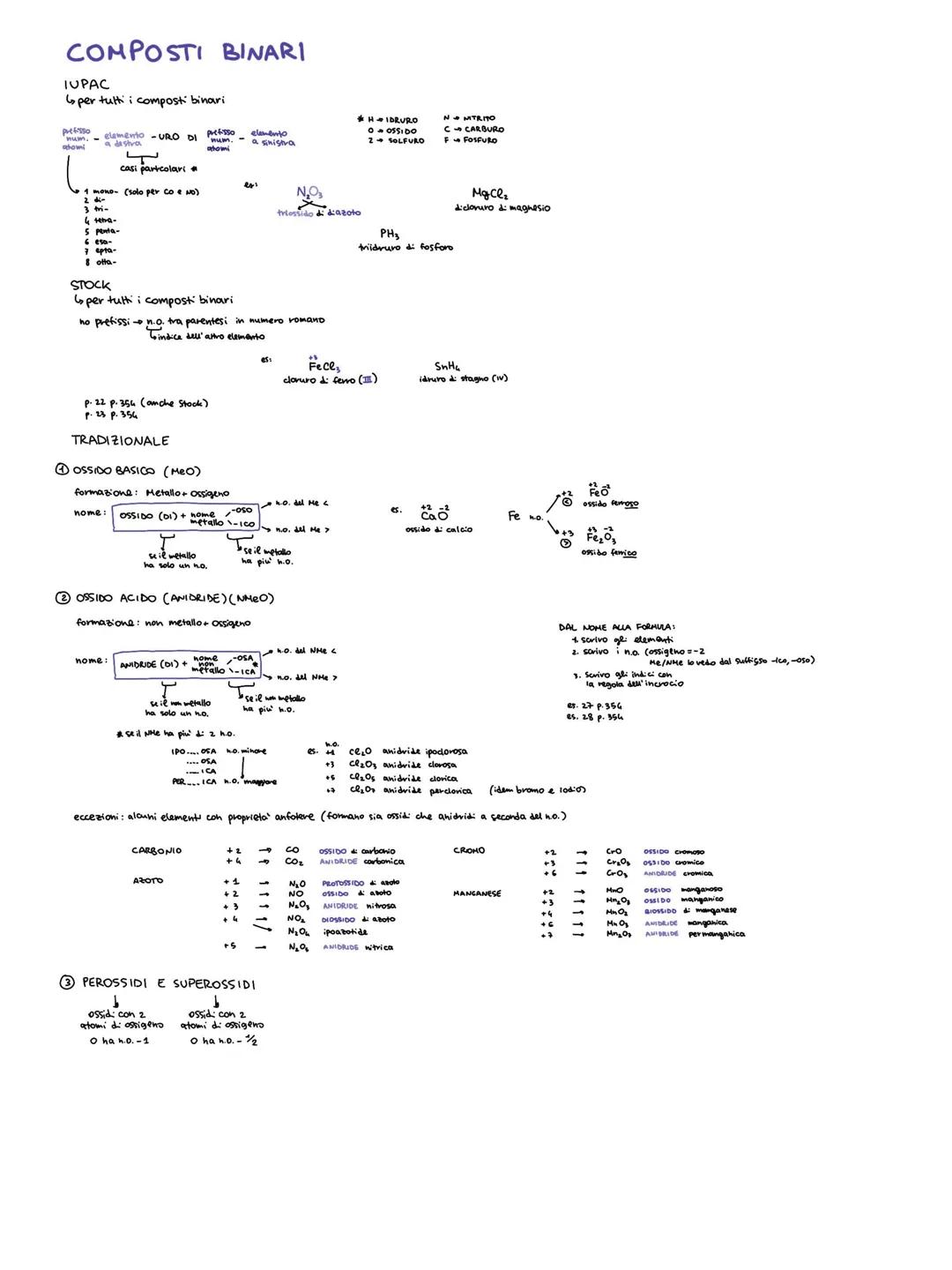
Gli ossidi basici si formano da metallo + ossigeno. Nella nomenclatura tradizionale usi "ossido di..." seguito dal nome del metallo. Se il metallo ha più numeri di ossidazione, aggiungi i suffissi -oso (n.o. minore) e -ico (n.o. maggiore).
Gli ossidi acidi (anidridi) vengono da non metallo + ossigeno. Si chiamano "anidride..." con gli stessi suffissi degli ossidi basici. Per gli alogeni (cloro, bromo, iodo) hai quattro possibilità: ipo...osa, ...osa, ...ica, per...ica.
Eccezioni importanti: Alcuni elementi come carbonio, azoto, cromo e manganese possono comportarsi sia da metalli che da non metalli a seconda del numero di ossidazione.
Attenzione: I perossidi hanno due atomi di ossigeno legati tra loro, quindi l'ossigeno ha n.o. -1 invece del solito -2!
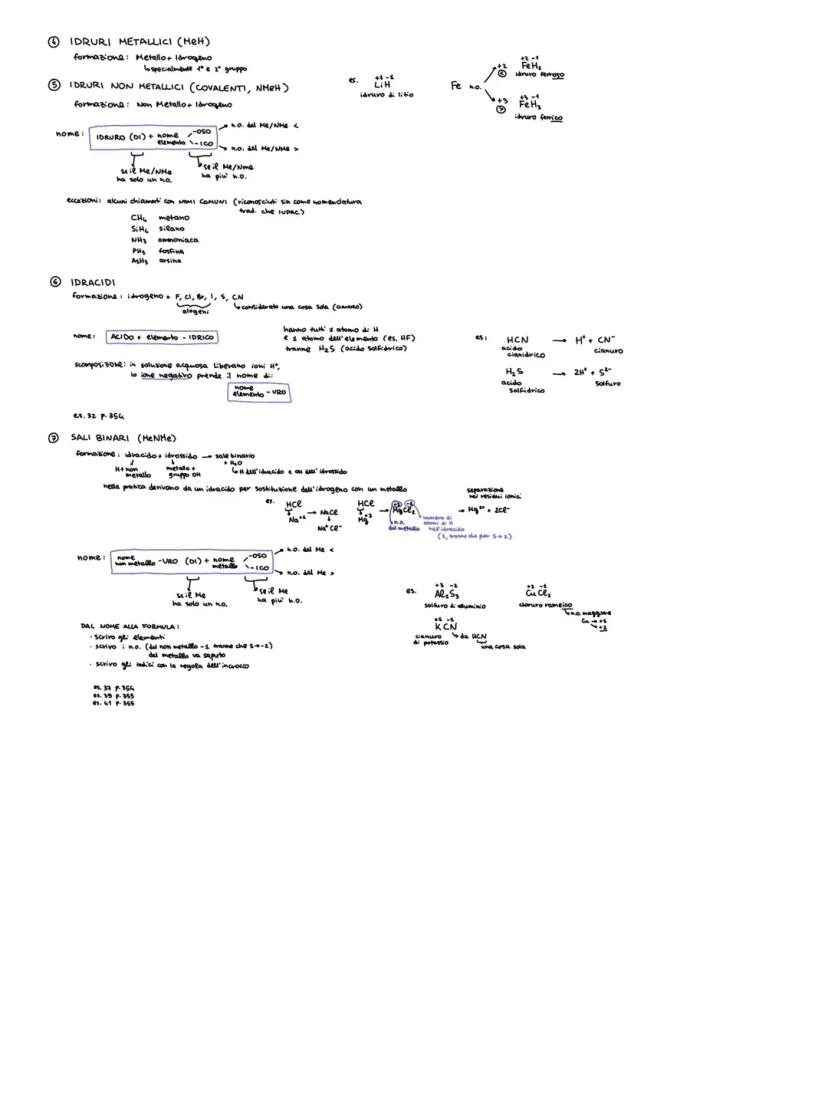
Idruri e Idracidi
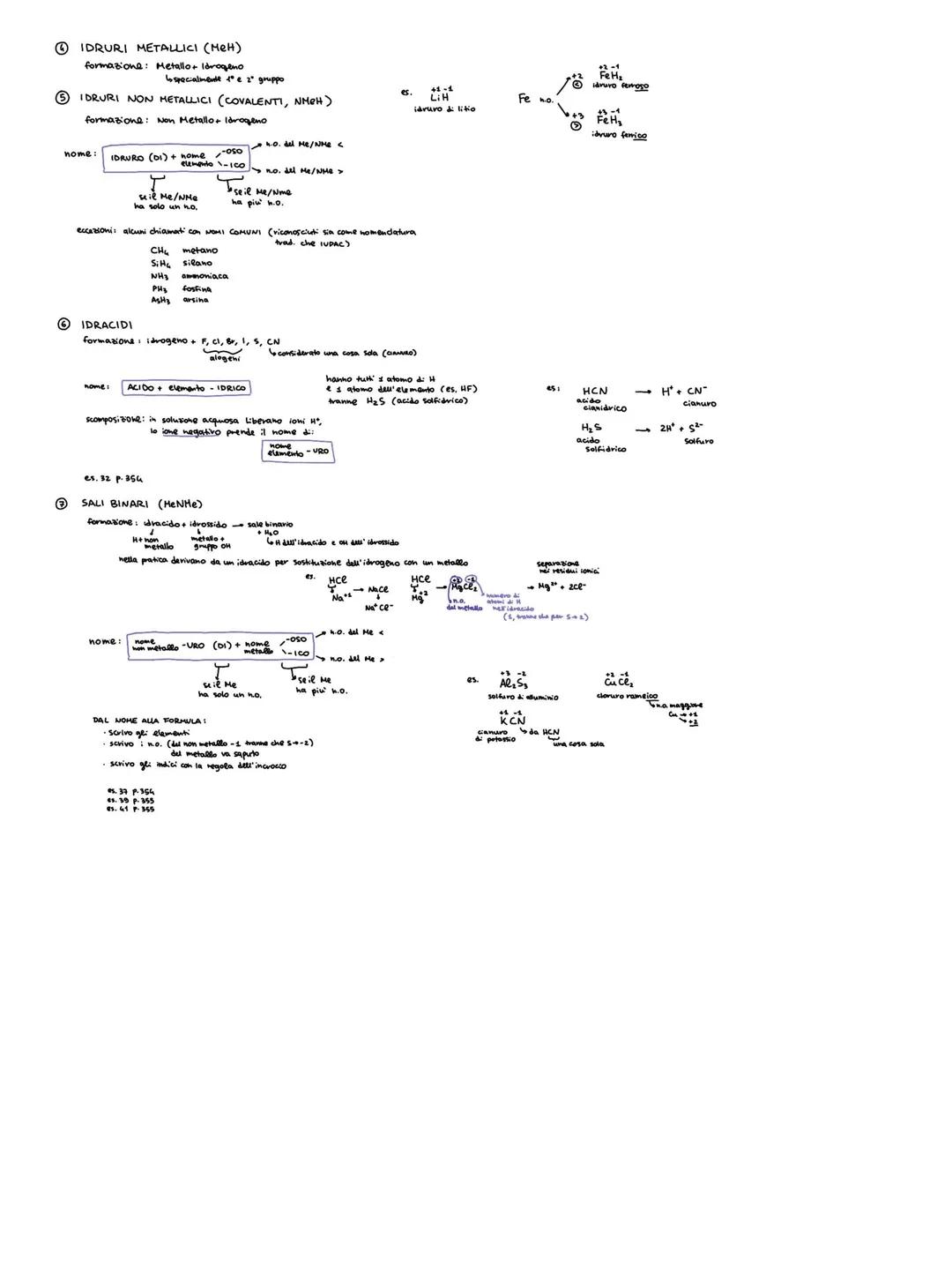
Gli idruri metallici seguono la regola "idruro di..." con i soliti suffissi -oso/-ico. Alcuni hanno nomi comuni come metano (CH₄) e ammoniaca (NH₃).
Gli idracidi si formano da idrogeno + non metalli del VII gruppo (alogeni) più zolfo e cianuro. Il nome è sempre "acido ...idrico" .
I sali binari derivano dagli idracidi sostituendo l'idrogeno con un metallo. Il nome finisce sempre in "-uro di..." seguito dal metallo.
Formula magica per i sali binari: prendi l'idracido, togli l'idrogeno e metti il metallo al suo posto, poi bilancia con la regola dell'incrocio.
Memorizza: Gli idracidi più comuni sono HF, HCl, HBr, HI (acidi degli alogeni), H₂S (acido solfidrico) e HCN (acido cianidrico).
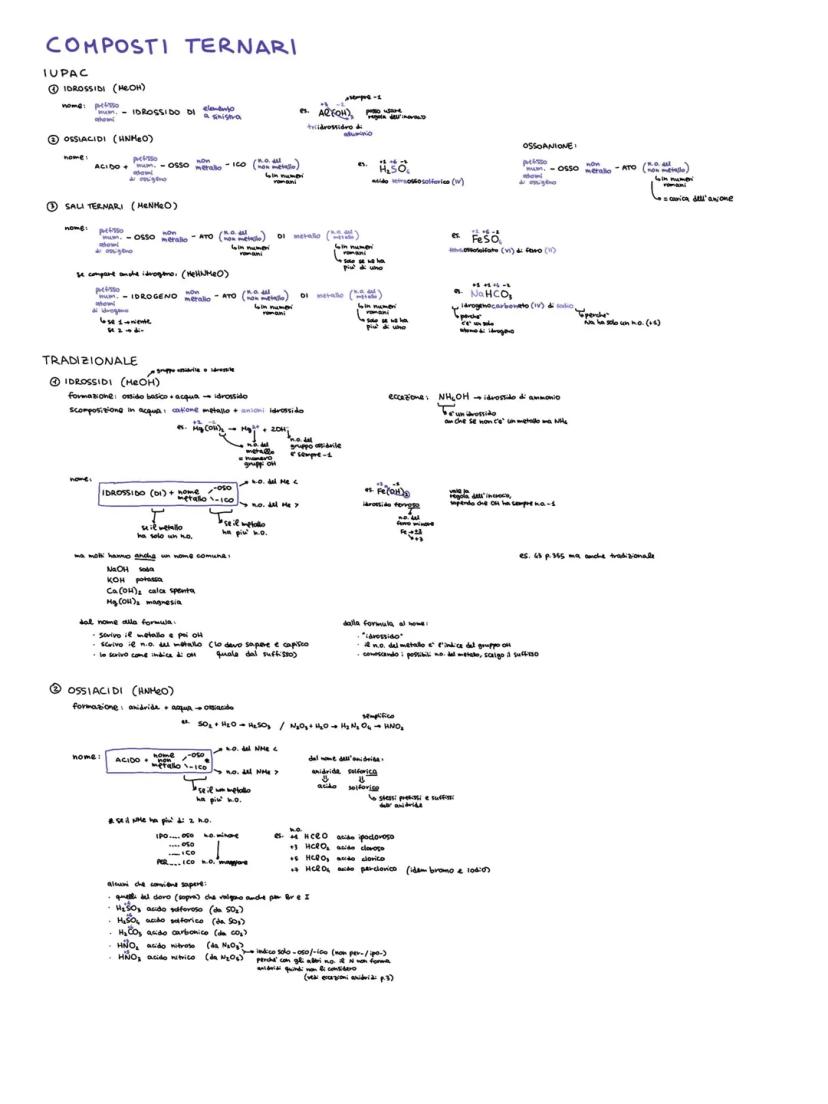
Composti Ternari - Idrossidi e Ossiacidi
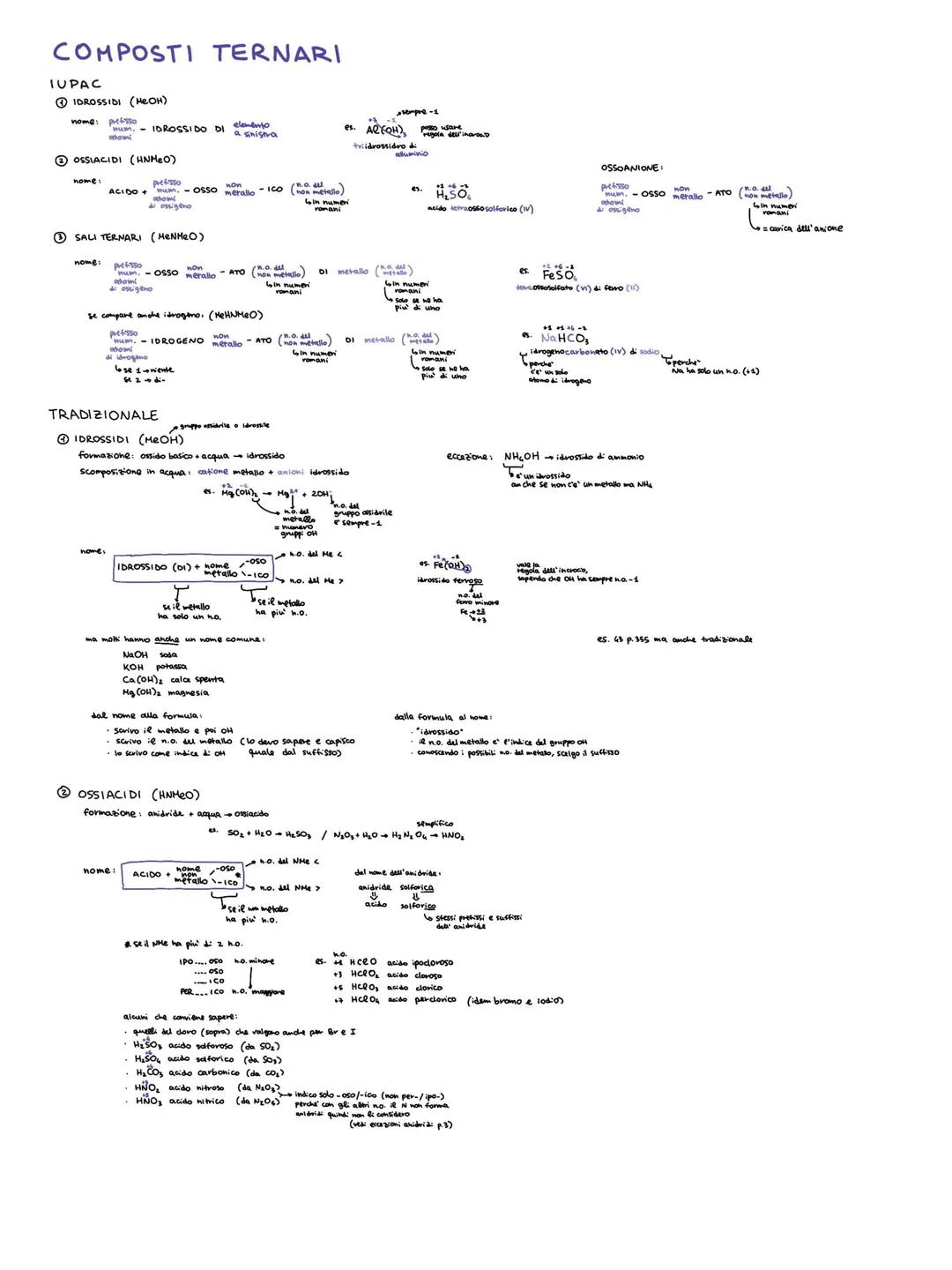
Gli idrossidi sono sempre basici. Il nome è "idrossido di..." con i soliti suffissi. Alcuni hanno nomi comuni: NaOH = soda, Ca(OH)₂ = calce spenta.
Gli ossiacidi derivano dalle anidridi che reagiscono con l'acqua. Mantengono gli stessi prefissi e suffissi dell'anidride di partenza, ma si chiamano "acido..." invece di "anidride".
Ossiacidi da memorizzare assolutamente:
- Alogeni: acido ipocloroso, cloroso, clorico, perclorico (anche per bromo e iodo)
- Altri importanti: H₂SO₄ (solforico), HNO₃ (nitrico), H₃PO₄ (fosforico), H₂CO₃ (carbonico)
Caso speciale: Gli acidi poliprotici (con più idrogeni) si dissociano a tappe, formando diversi ioni con cariche diverse.
Trucco: Dal nome dell'anidride all'ossiacido basta sostituire "anidride" con "acido" e mantenere tutto il resto uguale.

Ossiacidi Speciali e Ossoanioni
Alcuni elementi come boro, silicio e fosforo formano ossiacidi particolari con prefissi meta-, piro- e orto- a seconda di quante molecole d'acqua reagiscono con l'anidride.
Da sapere a memoria:
- H₃PO₄ = acido fosforico
- H₄P₂O₇ = acido pirofosforico
- H₃BO₃ = acido borico
Quando gli ossiacidi si dissociano in acqua, formano ioni H⁺ e ossoanioni (ioni negativi poliatomici). Il nome dell'ossoanione deriva dall'acido: se l'acido finisce in -oso, lo ione finisce in -ito; se finisce in -ico, lo ione finisce in -ato.
I poliacidi si formano quando più molecole di anidride reagiscono con acqua, creando acidi complessi come il dicromico (H₂Cr₂O₇).
Regola d'oro: Dall'acido allo ione cambia solo il suffisso: -oso diventa -ito, -ico diventa -ato.

Sali Ternari
I sali ternari si formano quando un metallo prende il posto dell'idrogeno in un ossiacido. È come se l'idrossido "mangiasse" l'ossiacido liberando acqua.
Per il nome: prendi l'ossiacido, togli "acido", cambia i suffissi e aggiungi "di..." seguito dal metallo con i suoi suffissi.
Esempi: H₂SO₄ + Ba → BaSO₄ = solfato di bario
Sostituzione parziale (sali acidi): Se rimangono alcuni idrogeni, il sale si chiama "acido" o si usa il prefisso "idrogeno-". Esempio: NaHSO₄ = solfato acido di sodio.
Per la formula: parti dal nome dell'acido, scrivi l'ossoanione, bilancia le cariche con la regola dell'incrocio.
Metodo infallibile: Conosci l'acido → conosci lo ione → aggiungi il metallo → bilancia le cariche.

Sali Speciali
I sali basici contengono gruppi ossidrili (OH⁻) oltre all'anione principale. Si chiamano con il prefisso "mono-" o "di-basico". Esempio: Bi(OH)₂Cl = cloruro di-basico di bismuto.
I sali di ammonio hanno lo ione ammonio (NH₄⁺) al posto del metallo. Esempio: (NH₄)₂SO₄ = solfato di ammonio.
I sali doppi hanno due cationi metallici diversi, tipici di minerali e rocce. Esempio: CaMg(CO₃)₂ = carbonato doppio di calcio e magnesio.
I sali idrati includono molecole d'acqua nella loro struttura cristallina. Esempio: CuSO₄·5H₂O = solfato rameico pentaidrato.
Curiosità: I sali idrati spesso cambiano colore quando perdono l'acqua, per questo il solfato di rame passa da blu (idrato) a bianco (anidro).

Schema Riassuntivo Completo
NOMENCLATURA TRADIZIONALE:
- Ossidi basici: ossido + metallo
- Anidridi: anidride + non metallo (ipo...osa, ...osa, ...ica, per...ica)
- Idruri: idruro di + metallo
- Idracidi: acido + elemento + idrico
- Idrossidi: idrossido di + metallo
- Ossiacidi: acido + non metallo
- Sali: nome anione + di + metallo
NOMENCLATURA STOCK: Tutti i composti binari: nome elemento + (numero romano) + "...uro di" + altro elemento
NOMENCLATURA IUPAC: Composti binari: prefisso + elemento + "uro di" + prefisso + altro elemento
Nomi comuni da ricordare: soda (NaOH), potassa (KOH), calce spenta Ca(OH)₂, metano (CH₄), ammoniaca (NH₃)
Consiglio finale: Impara prima la nomenclatura tradizionale perché è quella più usata, poi passa alle altre. La pratica costante è la chiave del successo!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti simili
Contenuti più popolari: nomenclatura chimica
4NOMENCLATURA COMPOSTI CHIMICI
Una scheda riassuntiva e intuitiva sulla nomenclatura 😉
I composti aromatici
Nomenclatura e reattività del benzene
Regole nomenclatura chimica
Regole per la nomenclatura chimica inorganica
Gli alcani
Gli alcani lineari, come si ottengono quali proprietà hanno, e come reagiscono.
Contenuti più popolari di Chimica
9Nomenclatura
Nomenclatura chimica inorganica
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Le biomolecole
Appunti sulle biomolecole approfonditi: introduzione, carboidrati, lipidi, proteine e acidi nucleici
APPUNTI DNA ED RNA
Tutto il DNA con la duplicazione del DNA. Tutto l’RNA con trascrizione e traduzione
i legami chimici
i legami chimici
Legami chimici pdf
Legami covalenti, ionici e metallici
Le cellule 🧫
Cellula provariote, cellula eucariote animale e cellula eucariote vegetale.
replicazione del DNA
struttura doppia elica DNA, replicazione DNA, complesso di replicazione, DNA polimerasi, telomeri
Il Metabolismo
Appunti del metabolismo che comprendono: metabolismo del glucosio (glicolisi, respirazione cellulare e fermentazione), metabolismo degli zuccheri (Glicogenosintesi, Glicogenolisi), Gluconeogenesi, metabolismo dei lipidi, catabolismo degli amminoacidi
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Guida alla Nomenclatura Chimica Inorganica
Preparati a padroneggiare la nomenclatura inorganica! Questa è la chiave per decifrare e creare i nomi di tutti i composti chimici. Con le regole giuste, imparerai a passare dalle formule ai nomi e viceversa senza sforzo.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Valenza e Numero di Ossidazione
La valenza è semplicemente il numero di legami che un atomo può formare. Per esempio, l'ossigeno ha valenza 2, l'idrogeno 1.
Il numero di ossidazione (n.o.) è la carica che un elemento avrebbe se tutti gli elettroni di legame fossero assegnati all'elemento più elettronegativo. Ogni elemento può avere più numeri di ossidazione diversi a seconda del composto.
Regole fondamentali per calcolare il n.o.:
- Nelle sostanze elementari, il n.o. è sempre 0
- Negli ioni, il n.o. corrisponde alla carica
- La somma dei n.o. in un composto neutro è sempre 0
Ricorda: L'ossigeno ha quasi sempre n.o. -2 , l'idrogeno +1 .

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Regola dell'Incrocio e Nomenclatura
La regola dell'incrocio ti permette di scrivere facilmente le formule dei composti binari. Scrivi l'elemento più elettronegativo a destra, poi incrocia i numeri di ossidazione: quello di un elemento diventa l'indice dell'altro.
Esistono tre tipi di nomenclatura: IUPAC (quella ufficiale internazionale), Stock (versione semplificata) e tradizionale (quella più antica ma ancora usata).
I composti inorganici si classificano in base alle loro proprietà: acidi o basici, binari o ternari (2 o 3 elementi), ionici o molecolari.
Schema di classificazione rapida:
- Con ossigeno: ossidi basici (metalli) o acidi/anidridi (non metalli)
- Con idrogeno: idruri (senza ossigeno) o idracidi/ossiacidi
- Sali: derivano dalla combinazione di acidi e basi
Trucco: Per riconoscere un composto dalla formula, guarda prima quanti elementi ci sono, poi cerca ossigeno e idrogeno per capire la famiglia.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Composti Binari - Ossidi
Gli ossidi basici si formano da metallo + ossigeno. Nella nomenclatura tradizionale usi "ossido di..." seguito dal nome del metallo. Se il metallo ha più numeri di ossidazione, aggiungi i suffissi -oso (n.o. minore) e -ico (n.o. maggiore).
Gli ossidi acidi (anidridi) vengono da non metallo + ossigeno. Si chiamano "anidride..." con gli stessi suffissi degli ossidi basici. Per gli alogeni (cloro, bromo, iodo) hai quattro possibilità: ipo...osa, ...osa, ...ica, per...ica.
Eccezioni importanti: Alcuni elementi come carbonio, azoto, cromo e manganese possono comportarsi sia da metalli che da non metalli a seconda del numero di ossidazione.
Attenzione: I perossidi hanno due atomi di ossigeno legati tra loro, quindi l'ossigeno ha n.o. -1 invece del solito -2!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Idruri e Idracidi
Gli idruri metallici seguono la regola "idruro di..." con i soliti suffissi -oso/-ico. Alcuni hanno nomi comuni come metano (CH₄) e ammoniaca (NH₃).
Gli idracidi si formano da idrogeno + non metalli del VII gruppo (alogeni) più zolfo e cianuro. Il nome è sempre "acido ...idrico" .
I sali binari derivano dagli idracidi sostituendo l'idrogeno con un metallo. Il nome finisce sempre in "-uro di..." seguito dal metallo.
Formula magica per i sali binari: prendi l'idracido, togli l'idrogeno e metti il metallo al suo posto, poi bilancia con la regola dell'incrocio.
Memorizza: Gli idracidi più comuni sono HF, HCl, HBr, HI (acidi degli alogeni), H₂S (acido solfidrico) e HCN (acido cianidrico).

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Composti Ternari - Idrossidi e Ossiacidi
Gli idrossidi sono sempre basici. Il nome è "idrossido di..." con i soliti suffissi. Alcuni hanno nomi comuni: NaOH = soda, Ca(OH)₂ = calce spenta.
Gli ossiacidi derivano dalle anidridi che reagiscono con l'acqua. Mantengono gli stessi prefissi e suffissi dell'anidride di partenza, ma si chiamano "acido..." invece di "anidride".
Ossiacidi da memorizzare assolutamente:
- Alogeni: acido ipocloroso, cloroso, clorico, perclorico (anche per bromo e iodo)
- Altri importanti: H₂SO₄ (solforico), HNO₃ (nitrico), H₃PO₄ (fosforico), H₂CO₃ (carbonico)
Caso speciale: Gli acidi poliprotici (con più idrogeni) si dissociano a tappe, formando diversi ioni con cariche diverse.
Trucco: Dal nome dell'anidride all'ossiacido basta sostituire "anidride" con "acido" e mantenere tutto il resto uguale.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Ossiacidi Speciali e Ossoanioni
Alcuni elementi come boro, silicio e fosforo formano ossiacidi particolari con prefissi meta-, piro- e orto- a seconda di quante molecole d'acqua reagiscono con l'anidride.
Da sapere a memoria:
- H₃PO₄ = acido fosforico
- H₄P₂O₇ = acido pirofosforico
- H₃BO₃ = acido borico
Quando gli ossiacidi si dissociano in acqua, formano ioni H⁺ e ossoanioni (ioni negativi poliatomici). Il nome dell'ossoanione deriva dall'acido: se l'acido finisce in -oso, lo ione finisce in -ito; se finisce in -ico, lo ione finisce in -ato.
I poliacidi si formano quando più molecole di anidride reagiscono con acqua, creando acidi complessi come il dicromico (H₂Cr₂O₇).
Regola d'oro: Dall'acido allo ione cambia solo il suffisso: -oso diventa -ito, -ico diventa -ato.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Sali Ternari
I sali ternari si formano quando un metallo prende il posto dell'idrogeno in un ossiacido. È come se l'idrossido "mangiasse" l'ossiacido liberando acqua.
Per il nome: prendi l'ossiacido, togli "acido", cambia i suffissi e aggiungi "di..." seguito dal metallo con i suoi suffissi.
Esempi: H₂SO₄ + Ba → BaSO₄ = solfato di bario
Sostituzione parziale (sali acidi): Se rimangono alcuni idrogeni, il sale si chiama "acido" o si usa il prefisso "idrogeno-". Esempio: NaHSO₄ = solfato acido di sodio.
Per la formula: parti dal nome dell'acido, scrivi l'ossoanione, bilancia le cariche con la regola dell'incrocio.
Metodo infallibile: Conosci l'acido → conosci lo ione → aggiungi il metallo → bilancia le cariche.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Sali Speciali
I sali basici contengono gruppi ossidrili (OH⁻) oltre all'anione principale. Si chiamano con il prefisso "mono-" o "di-basico". Esempio: Bi(OH)₂Cl = cloruro di-basico di bismuto.
I sali di ammonio hanno lo ione ammonio (NH₄⁺) al posto del metallo. Esempio: (NH₄)₂SO₄ = solfato di ammonio.
I sali doppi hanno due cationi metallici diversi, tipici di minerali e rocce. Esempio: CaMg(CO₃)₂ = carbonato doppio di calcio e magnesio.
I sali idrati includono molecole d'acqua nella loro struttura cristallina. Esempio: CuSO₄·5H₂O = solfato rameico pentaidrato.
Curiosità: I sali idrati spesso cambiano colore quando perdono l'acqua, per questo il solfato di rame passa da blu (idrato) a bianco (anidro).

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Schema Riassuntivo Completo
NOMENCLATURA TRADIZIONALE:
- Ossidi basici: ossido + metallo
- Anidridi: anidride + non metallo (ipo...osa, ...osa, ...ica, per...ica)
- Idruri: idruro di + metallo
- Idracidi: acido + elemento + idrico
- Idrossidi: idrossido di + metallo
- Ossiacidi: acido + non metallo
- Sali: nome anione + di + metallo
NOMENCLATURA STOCK: Tutti i composti binari: nome elemento + (numero romano) + "...uro di" + altro elemento
NOMENCLATURA IUPAC: Composti binari: prefisso + elemento + "uro di" + prefisso + altro elemento
Nomi comuni da ricordare: soda (NaOH), potassa (KOH), calce spenta Ca(OH)₂, metano (CH₄), ammoniaca (NH₃)
Consiglio finale: Impara prima la nomenclatura tradizionale perché è quella più usata, poi passa alle altre. La pratica costante è la chiave del successo!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti simili
Contenuti più popolari: nomenclatura chimica
4NOMENCLATURA COMPOSTI CHIMICI
Una scheda riassuntiva e intuitiva sulla nomenclatura 😉
I composti aromatici
Nomenclatura e reattività del benzene
Regole nomenclatura chimica
Regole per la nomenclatura chimica inorganica
Gli alcani
Gli alcani lineari, come si ottengono quali proprietà hanno, e come reagiscono.
Contenuti più popolari di Chimica
9Nomenclatura
Nomenclatura chimica inorganica
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Le biomolecole
Appunti sulle biomolecole approfonditi: introduzione, carboidrati, lipidi, proteine e acidi nucleici
APPUNTI DNA ED RNA
Tutto il DNA con la duplicazione del DNA. Tutto l’RNA con trascrizione e traduzione
i legami chimici
i legami chimici
Legami chimici pdf
Legami covalenti, ionici e metallici
Le cellule 🧫
Cellula provariote, cellula eucariote animale e cellula eucariote vegetale.
replicazione del DNA
struttura doppia elica DNA, replicazione DNA, complesso di replicazione, DNA polimerasi, telomeri
Il Metabolismo
Appunti del metabolismo che comprendono: metabolismo del glucosio (glicolisi, respirazione cellulare e fermentazione), metabolismo degli zuccheri (Glicogenosintesi, Glicogenolisi), Gluconeogenesi, metabolismo dei lipidi, catabolismo degli amminoacidi
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.