I legami chimici sono le forze che tengono uniti gli... Mostra di più
Tipi di Legami Chimici







Introduzione ai Legami Chimici
I legami chimici sono forze attrattive di natura elettrica che si formano tra atomi e molecole. Pensaci: tutti gli atomi isolati (tranne i gas nobili) hanno livelli energetici esterni incompleti, il che li rende instabili e con alta energia.
Per diminuire l'energia e aumentare la stabilità, questi atomi formano legami chimici con altri atomi uguali o diversi. La configurazione elettronica esterna può essere rappresentata con la notazione di Lewis, che ci aiuta a visualizzare come si comportano gli elettroni.
I legami si dividono in due categorie principali: primari (forti, tra atomi) e secondari (deboli, tra molecole). I legami primari includono ionico, covalente e metallico. L'energia di legame è l'energia liberata quando si forma il legame, ed è anche quella necessaria per romperlo.
Ricorda: I gas nobili sono stabili perché hanno configurazioni elettroniche complete - tutti gli altri atomi cercano di imitarli!

Legame Ionico
Il legame ionico si forma tra atomi con un'alta differenza di elettronegatività (ΔE ≥ 1,9). Avviene tipicamente tra metalli e non metalli: il metallo perde elettroni diventando un catione (ione positivo), mentre il non metallo acquista elettroni diventando un anione (ione negativo).
Gli ioni possono essere monoatomici (un solo atomo) o poliatomici (gruppi di atomi legati covalentemente). In un composto ionico, le forze di attrazione dispongono gli ioni in una struttura ordinata chiamata reticolo cristallino.
I reticoli più comuni sono quello cubico a facce centrate (ogni ione circondato da 6 ioni di carica opposta) e quello cubico a corpo centrato (ogni ione circondato da 8 ioni di carica opposta). Il numero di coordinazione indica quanti ioni di carica opposta circondano ogni ione.
Esempio pratico: Nel sale da cucina (NaCl), il sodio perde un elettrone e il cloro lo acquista!

Legame Covalente: Basi
Il legame covalente si stabilisce tra atomi di non metalli che condividono elettroni. Si forma quando la differenza di elettronegatività è piccola (ΔE < 1,9). Gli atomi mettono in comune elettroni per raggiungere l'ottetto e diminuire la loro energia.
Esistono tre tipi principali: covalente semplice (condivisione di una coppia di elettroni), doppio (due coppie) e triplo (tre coppie). Il legame può essere omopolare (tra atomi uguali) o eteropolare (tra atomi diversi).
Il legame covalente dativo è speciale: entrambi gli elettroni provengono dallo stesso atomo. Questo accade quando un atomo ha già raggiunto l'ottetto ma possiede doppietti elettronici liberi.
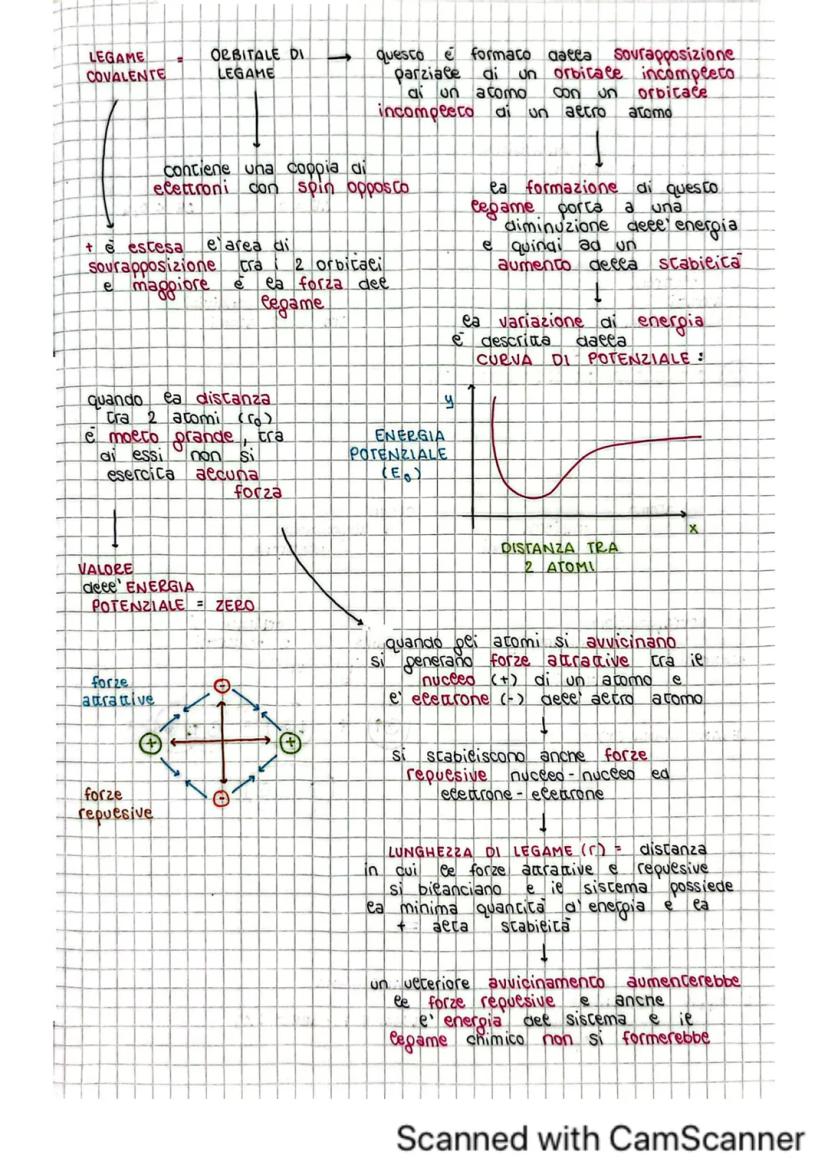
L'orbitale di legame si forma dalla sovrapposizione di orbitali incompleti di due atomi. Maggiore è l'area di sovrapposizione, più forte è il legame.
Trucco: Se la differenza di elettronegatività è minore di 0,4, il legame è praticamente apolare!
Energia e Stabilità nei Legami
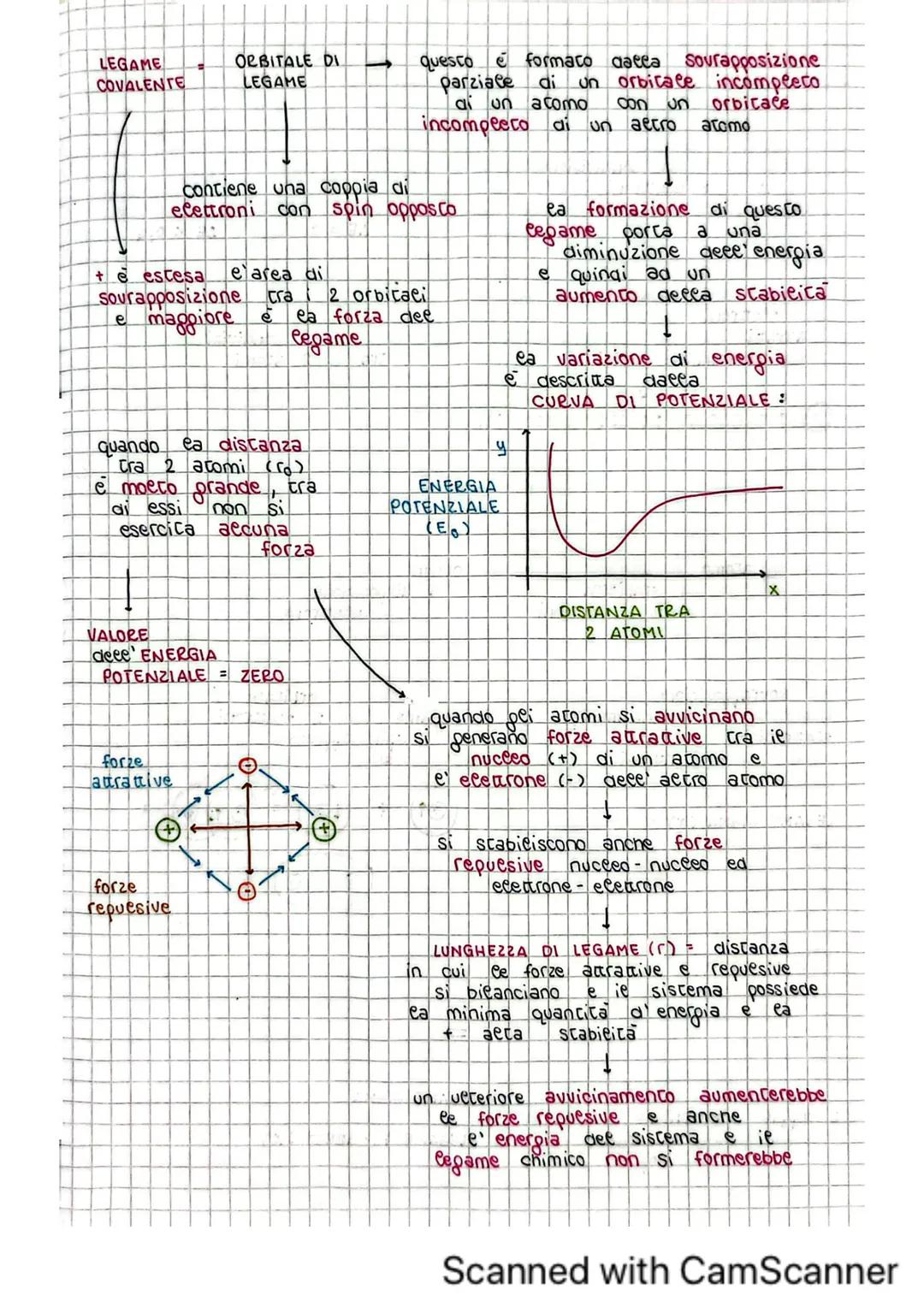
La formazione del legame covalente è descritta dalla curva di potenziale. Quando due atomi sono molto distanti, non si esercita alcuna forza tra loro . Avvicinandosi, si generano forze attrattive tra nucleo positivo e elettroni negativi.
Contemporaneamente si creano anche forze repulsive tra nuclei e tra elettroni. La lunghezza di legame è la distanza in cui forze attrattive e repulsive si bilanciano perfettamente, dando al sistema la minima energia e massima stabilità.
Se gli atomi si avvicinassero ulteriormente, le forze repulsive aumenterebbero troppo e il legame non si formerebbe. È un equilibrio perfetto che la natura ha trovato per creare stabilità.
La sovrapposizione frontale degli orbitali determina un addensamento elettronico sull'asse che unisce i nuclei, formando un orbitale di legame con due elettroni di spin opposto.
Visualizza: Immagina due magneti che si attraggono fino a una distanza perfetta - troppo vicini si respingono!

Legami Sigma e Pi-greco
Nel legame covalente omopolare (o apolare), gli elettroni sono condivisi equamente perché ΔE = 0 oppure ΔE < 0,4. La molecola di idrogeno (H₂) è l'esempio perfetto: ogni atomo contribuisce con un elettrone, raggiungendo la stabilità con 2 elettroni intorno al nucleo.
Il legame sigma (σ) si forma dalla sovrapposizione frontale e l'orbitale avvolge la retta tra i due nuclei. Nella molecola di ossigeno (O₂), oltre al legame sigma c'è anche un legame pi-greco (π), che si trova sopra e sotto la retta che unisce i nuclei.
L'azoto (N₂) ha un legame triplo: un sigma e due pi-greco. Questo lo rende estremamente stabile, motivo per cui l'azoto atmosferico è così inerte chimicamente.
I legami pi-greco si formano dalla sovrapposizione laterale degli orbitali e sono generalmente più deboli dei sigma, che hanno sovrapposizione frontale più efficace.
Regola pratica: Il primo legame è sempre sigma, il secondo e terzo sono sempre pi-greco!

Legame Covalente Polare
Nel legame covalente eteropolare (o polare), la differenza di elettronegatività è significativa (0,4 < ΔE < 1,9). Gli elettroni di legame sono più attratti dall'atomo più elettronegativo, creando una distribuzione asimmetrica della carica elettrica.
L'atomo più elettronegativo assume una parziale carica negativa (δ-), mentre quello meno elettronegativo assume una parziale carica positiva (δ+). Si forma così un dipolo: due cariche uguali e opposte separate da una certa distanza.
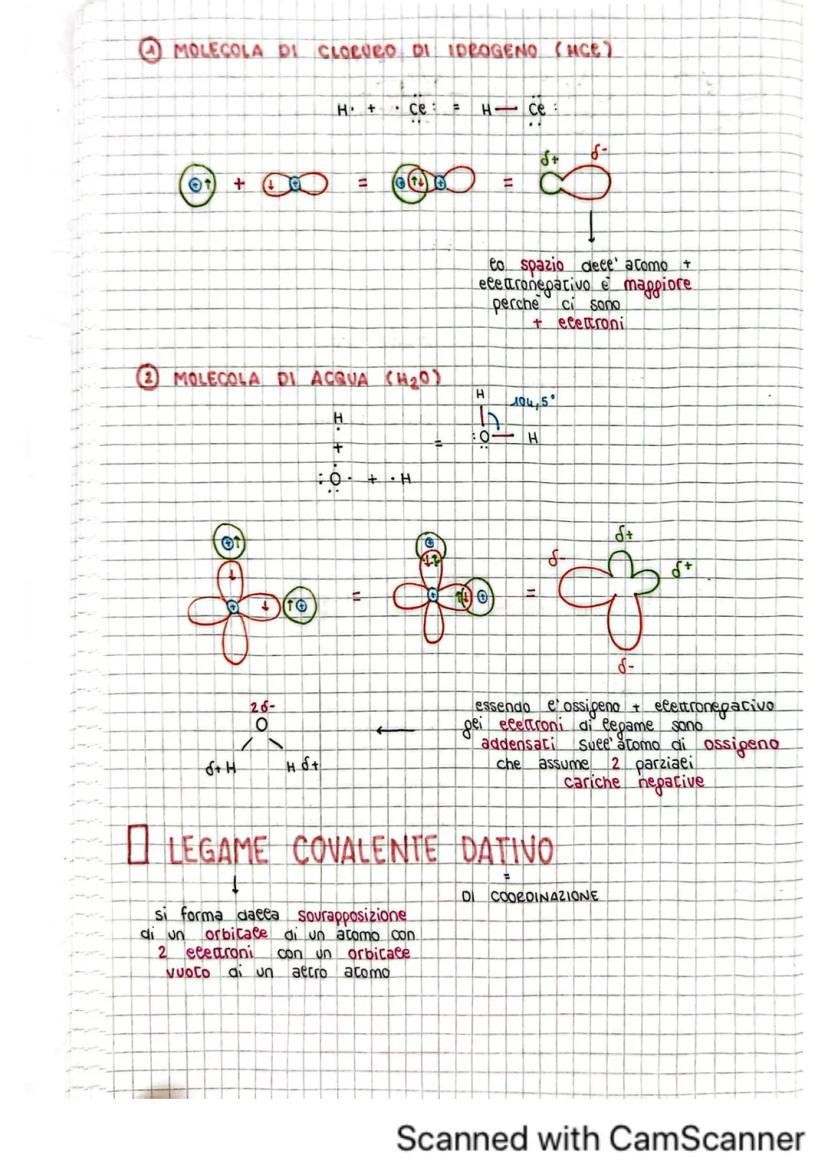
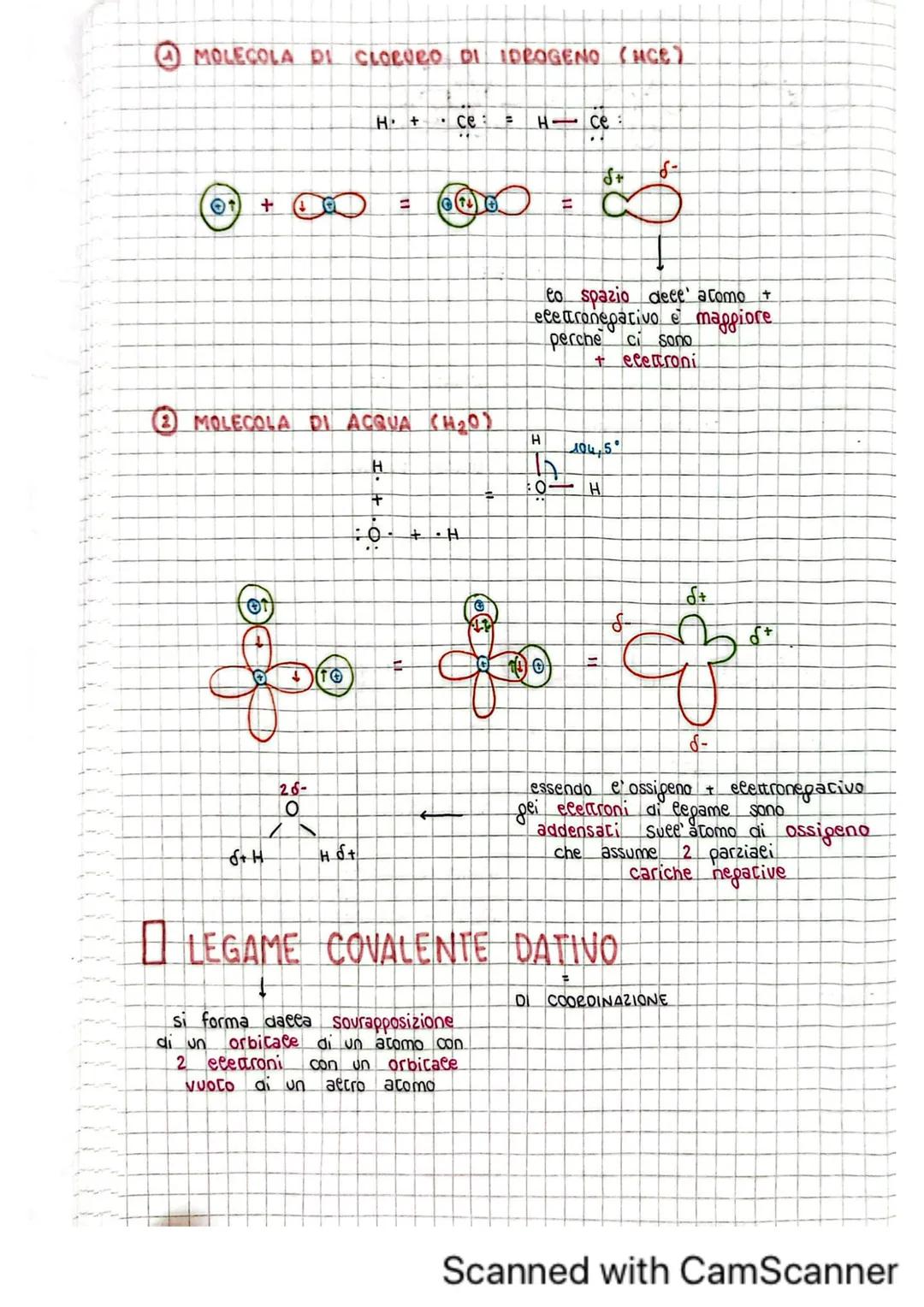
Nell'acido cloridrico (HCl), il cloro è più elettronegativo dell'idrogeno, quindi attrae maggiormente gli elettroni. Nell'acqua (H₂O), l'ossigeno è più elettronegativo dell'idrogeno, creando due dipoli che danno alla molecola la sua caratteristica polarità.
La polarità delle molecole influenza moltissime proprietà fisiche e chimiche, come la solubilità e i punti di ebollizione.
Curiosità: La polarità dell'acqua è il motivo per cui può sciogliere il sale ma non l'olio!
Legame Dativo e Forme Molecolari
Il legame covalente dativo (o di coordinazione) si forma quando un atomo che ha già raggiunto l'ottetto fornisce entrambi gli elettroni a un altro atomo con un orbitale vuoto. L'atomo donatore deve avere doppietti elettronici non impegnati, mentre l'atomo accettore deve avere orbitali vuoti.
Se l'atomo donatore ha 2 o 3 doppietti liberi, può formare 2 o 3 legami dativi. Nel diossido di zolfo (SO₂), lo zolfo forma legami dativi con entrambi gli atomi di ossigeno.
Nelle molecole come HCl e H₂O, la distribuzione spaziale degli elettroni determina la forma molecolare. L'acqua ha una forma angolare con angolo di circa 104,5° a causa dei doppietti elettronici non condivisi sull'ossigeno.
La geometria molecolare influenza drasticamente le proprietà delle sostanze, dalla loro reattività alle loro proprietà fisiche.
Ricorda: Un legame dativo, una volta formato, è identico a un normale legame covalente!

Legame Metallico
Il legame metallico si forma tra atomi metallici disposti in un reticolo cristallino ordinato. Poiché i metalli hanno bassi valori di energia di ionizzazione, cedono facilmente i loro elettroni esterni diventando cationi.
Gli elettroni esterni si muovono liberamente intorno agli ioni positivi, formando quello che viene chiamato "mare di elettroni". Il legame metallico è proprio questa forza di attrazione tra gli ioni positivi fissi e gli elettroni mobili.
La cella elementare è l'unità del reticolo che si ripete. Questa struttura spiega le proprietà tipiche dei metalli: conducibilità elettrica (elettroni mobili), malleabilità (gli ioni possono scorrere) e lucentezza (elettroni che riflettono la luce).
Il legame si rappresenta con il simbolo del metallo e l'indicazione dello stato fisico, come Ag(s) per l'argento solido.
Visualizza: Gli elettroni nei metalli sono come un fluido che scorre tra sfere positive impacchettate!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti simili
Contenuti più popolari: Ossidazione
9Chimica organica
Nomenclatura e proprietà di idrocarburi e alogenoderivati: ALCANI, ALCHENI, ALCHINI, IDROCARBURI AROMATICI, ALCOLI, FENOLI, ETERI, ALDEIDI, CHETONI, ACIDI CARBOSSILICI, SAPONI, ESTERI, AMMINE
I carboidrati
Monosaccaridi, disaccaridi e polisaccaridi
Idrocarburi alifatici e aliciclici: Alcani, cicloalcani, Alcheni, Alchini
Alcani, cicloalcani, Alcheni, Alchini con rispettive reazioni
Chimica, programma intero di quinto
Chimica Organica, Biomolecole, Matabolismo del glucosio, Ciclo di Krebs e Fosforilazione Ossidativa; Biochimica del corpo umano, accenni alla fotosintesi. Gli Acidi Nucleici e il DNA, Replicazione, Trascrizione e Traduzione.
Enzimi
Biochimica: gli enzimi - che cosa sono e funzione - specificità enzima - cofattori enzimatici - azione catalitica - attività enzimatica e regolazione
i carboidrati
appunti sui carboidrati: monosaccaridi, proiezioni di Fischer, proiezioni di Haworth, reazioni dei monosaccaridi, oligosaccaridi (lattosio, maltosio e saccarosio) e polisaccaridi (amido, glicogeno, cellulosa, chitina e eteropolisaccaridi)
Reazioni di ossido-riduzione (redox)
teoria + esercizi
I derivati degli idrocarburi
Appunti chimica
Reazioni di ossido-riduzione (redox)
Il numero di ossidazione, ossidante e riducente, bilanciamento regole principali, metodo delle semi reazioni, metodo della variazione di n.o. Appunti presi a lezioni integrati con il libro di testo. Ho preso 9 nella verifica.
Contenuti più popolari di Scienze
9ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Apparato respiratorio
fai un quiz
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Cellula procariote ed eucariote.
Descrizione delle diverse tipologie di microscopi ottici ed elettronici e la struttura della cellula procariote ed eucariote. Composizione delle cellule ed organuli cellulari.
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Tipi di Legami Chimici
I legami chimici sono le forze che tengono uniti gli atomi e le molecole, ed è essenziale capirli per comprendere come funziona la chimica. Esistono tre tipi principali di legami - ionico, covalente e metallico - ognuno con caratteristiche uniche... Mostra di più

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Introduzione ai Legami Chimici
I legami chimici sono forze attrattive di natura elettrica che si formano tra atomi e molecole. Pensaci: tutti gli atomi isolati (tranne i gas nobili) hanno livelli energetici esterni incompleti, il che li rende instabili e con alta energia.
Per diminuire l'energia e aumentare la stabilità, questi atomi formano legami chimici con altri atomi uguali o diversi. La configurazione elettronica esterna può essere rappresentata con la notazione di Lewis, che ci aiuta a visualizzare come si comportano gli elettroni.
I legami si dividono in due categorie principali: primari (forti, tra atomi) e secondari (deboli, tra molecole). I legami primari includono ionico, covalente e metallico. L'energia di legame è l'energia liberata quando si forma il legame, ed è anche quella necessaria per romperlo.
Ricorda: I gas nobili sono stabili perché hanno configurazioni elettroniche complete - tutti gli altri atomi cercano di imitarli!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legame Ionico
Il legame ionico si forma tra atomi con un'alta differenza di elettronegatività (ΔE ≥ 1,9). Avviene tipicamente tra metalli e non metalli: il metallo perde elettroni diventando un catione (ione positivo), mentre il non metallo acquista elettroni diventando un anione (ione negativo).
Gli ioni possono essere monoatomici (un solo atomo) o poliatomici (gruppi di atomi legati covalentemente). In un composto ionico, le forze di attrazione dispongono gli ioni in una struttura ordinata chiamata reticolo cristallino.
I reticoli più comuni sono quello cubico a facce centrate (ogni ione circondato da 6 ioni di carica opposta) e quello cubico a corpo centrato (ogni ione circondato da 8 ioni di carica opposta). Il numero di coordinazione indica quanti ioni di carica opposta circondano ogni ione.
Esempio pratico: Nel sale da cucina (NaCl), il sodio perde un elettrone e il cloro lo acquista!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legame Covalente: Basi
Il legame covalente si stabilisce tra atomi di non metalli che condividono elettroni. Si forma quando la differenza di elettronegatività è piccola (ΔE < 1,9). Gli atomi mettono in comune elettroni per raggiungere l'ottetto e diminuire la loro energia.
Esistono tre tipi principali: covalente semplice (condivisione di una coppia di elettroni), doppio (due coppie) e triplo (tre coppie). Il legame può essere omopolare (tra atomi uguali) o eteropolare (tra atomi diversi).
Il legame covalente dativo è speciale: entrambi gli elettroni provengono dallo stesso atomo. Questo accade quando un atomo ha già raggiunto l'ottetto ma possiede doppietti elettronici liberi.
L'orbitale di legame si forma dalla sovrapposizione di orbitali incompleti di due atomi. Maggiore è l'area di sovrapposizione, più forte è il legame.
Trucco: Se la differenza di elettronegatività è minore di 0,4, il legame è praticamente apolare!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Energia e Stabilità nei Legami
La formazione del legame covalente è descritta dalla curva di potenziale. Quando due atomi sono molto distanti, non si esercita alcuna forza tra loro . Avvicinandosi, si generano forze attrattive tra nucleo positivo e elettroni negativi.
Contemporaneamente si creano anche forze repulsive tra nuclei e tra elettroni. La lunghezza di legame è la distanza in cui forze attrattive e repulsive si bilanciano perfettamente, dando al sistema la minima energia e massima stabilità.
Se gli atomi si avvicinassero ulteriormente, le forze repulsive aumenterebbero troppo e il legame non si formerebbe. È un equilibrio perfetto che la natura ha trovato per creare stabilità.
La sovrapposizione frontale degli orbitali determina un addensamento elettronico sull'asse che unisce i nuclei, formando un orbitale di legame con due elettroni di spin opposto.
Visualizza: Immagina due magneti che si attraggono fino a una distanza perfetta - troppo vicini si respingono!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legami Sigma e Pi-greco
Nel legame covalente omopolare (o apolare), gli elettroni sono condivisi equamente perché ΔE = 0 oppure ΔE < 0,4. La molecola di idrogeno (H₂) è l'esempio perfetto: ogni atomo contribuisce con un elettrone, raggiungendo la stabilità con 2 elettroni intorno al nucleo.
Il legame sigma (σ) si forma dalla sovrapposizione frontale e l'orbitale avvolge la retta tra i due nuclei. Nella molecola di ossigeno (O₂), oltre al legame sigma c'è anche un legame pi-greco (π), che si trova sopra e sotto la retta che unisce i nuclei.
L'azoto (N₂) ha un legame triplo: un sigma e due pi-greco. Questo lo rende estremamente stabile, motivo per cui l'azoto atmosferico è così inerte chimicamente.
I legami pi-greco si formano dalla sovrapposizione laterale degli orbitali e sono generalmente più deboli dei sigma, che hanno sovrapposizione frontale più efficace.
Regola pratica: Il primo legame è sempre sigma, il secondo e terzo sono sempre pi-greco!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legame Covalente Polare
Nel legame covalente eteropolare (o polare), la differenza di elettronegatività è significativa (0,4 < ΔE < 1,9). Gli elettroni di legame sono più attratti dall'atomo più elettronegativo, creando una distribuzione asimmetrica della carica elettrica.
L'atomo più elettronegativo assume una parziale carica negativa (δ-), mentre quello meno elettronegativo assume una parziale carica positiva (δ+). Si forma così un dipolo: due cariche uguali e opposte separate da una certa distanza.
Nell'acido cloridrico (HCl), il cloro è più elettronegativo dell'idrogeno, quindi attrae maggiormente gli elettroni. Nell'acqua (H₂O), l'ossigeno è più elettronegativo dell'idrogeno, creando due dipoli che danno alla molecola la sua caratteristica polarità.
La polarità delle molecole influenza moltissime proprietà fisiche e chimiche, come la solubilità e i punti di ebollizione.
Curiosità: La polarità dell'acqua è il motivo per cui può sciogliere il sale ma non l'olio!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legame Dativo e Forme Molecolari
Il legame covalente dativo (o di coordinazione) si forma quando un atomo che ha già raggiunto l'ottetto fornisce entrambi gli elettroni a un altro atomo con un orbitale vuoto. L'atomo donatore deve avere doppietti elettronici non impegnati, mentre l'atomo accettore deve avere orbitali vuoti.
Se l'atomo donatore ha 2 o 3 doppietti liberi, può formare 2 o 3 legami dativi. Nel diossido di zolfo (SO₂), lo zolfo forma legami dativi con entrambi gli atomi di ossigeno.
Nelle molecole come HCl e H₂O, la distribuzione spaziale degli elettroni determina la forma molecolare. L'acqua ha una forma angolare con angolo di circa 104,5° a causa dei doppietti elettronici non condivisi sull'ossigeno.
La geometria molecolare influenza drasticamente le proprietà delle sostanze, dalla loro reattività alle loro proprietà fisiche.
Ricorda: Un legame dativo, una volta formato, è identico a un normale legame covalente!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legame Metallico
Il legame metallico si forma tra atomi metallici disposti in un reticolo cristallino ordinato. Poiché i metalli hanno bassi valori di energia di ionizzazione, cedono facilmente i loro elettroni esterni diventando cationi.
Gli elettroni esterni si muovono liberamente intorno agli ioni positivi, formando quello che viene chiamato "mare di elettroni". Il legame metallico è proprio questa forza di attrazione tra gli ioni positivi fissi e gli elettroni mobili.
La cella elementare è l'unità del reticolo che si ripete. Questa struttura spiega le proprietà tipiche dei metalli: conducibilità elettrica (elettroni mobili), malleabilità (gli ioni possono scorrere) e lucentezza (elettroni che riflettono la luce).
Il legame si rappresenta con il simbolo del metallo e l'indicazione dello stato fisico, come Ag(s) per l'argento solido.
Visualizza: Gli elettroni nei metalli sono come un fluido che scorre tra sfere positive impacchettate!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti simili
Contenuti più popolari: Ossidazione
9Chimica organica
Nomenclatura e proprietà di idrocarburi e alogenoderivati: ALCANI, ALCHENI, ALCHINI, IDROCARBURI AROMATICI, ALCOLI, FENOLI, ETERI, ALDEIDI, CHETONI, ACIDI CARBOSSILICI, SAPONI, ESTERI, AMMINE
I carboidrati
Monosaccaridi, disaccaridi e polisaccaridi
Idrocarburi alifatici e aliciclici: Alcani, cicloalcani, Alcheni, Alchini
Alcani, cicloalcani, Alcheni, Alchini con rispettive reazioni
Chimica, programma intero di quinto
Chimica Organica, Biomolecole, Matabolismo del glucosio, Ciclo di Krebs e Fosforilazione Ossidativa; Biochimica del corpo umano, accenni alla fotosintesi. Gli Acidi Nucleici e il DNA, Replicazione, Trascrizione e Traduzione.
Enzimi
Biochimica: gli enzimi - che cosa sono e funzione - specificità enzima - cofattori enzimatici - azione catalitica - attività enzimatica e regolazione
i carboidrati
appunti sui carboidrati: monosaccaridi, proiezioni di Fischer, proiezioni di Haworth, reazioni dei monosaccaridi, oligosaccaridi (lattosio, maltosio e saccarosio) e polisaccaridi (amido, glicogeno, cellulosa, chitina e eteropolisaccaridi)
Reazioni di ossido-riduzione (redox)
teoria + esercizi
I derivati degli idrocarburi
Appunti chimica
Reazioni di ossido-riduzione (redox)
Il numero di ossidazione, ossidante e riducente, bilanciamento regole principali, metodo delle semi reazioni, metodo della variazione di n.o. Appunti presi a lezioni integrati con il libro di testo. Ho preso 9 nella verifica.
Contenuti più popolari di Scienze
9ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Apparato respiratorio
fai un quiz
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Cellula procariote ed eucariote.
Descrizione delle diverse tipologie di microscopi ottici ed elettronici e la struttura della cellula procariote ed eucariote. Composizione delle cellule ed organuli cellulari.
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.