Gli idrocarburi aromatici sono composti organici con una struttura particolare... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
2,994
•
Aggiornato Apr 24, 2026
•
Gli idrocarburi aromatici sono composti organici con una struttura particolare... Mostra di più



Il termine "aromatico" nasce dall'odore piacevole di questi composti, ma oggi indica una particolare reattività chimica. Il benzene è l'idrocarburo aromatico di riferimento, mentre gli areni sono tutti i composti che lo contengono.
Oltre agli aromatici, devi conoscere i principali gruppi funzionali: il gruppo carbonilico caratterizza aldeidi e chetoni, il gruppo carbinolico gli alcoli, e il gruppo carbossilico gli acidi carbossilici.
La benzaldeide è un esempio perfetto di come questi gruppi si combinano: è un'aldeide attaccata a un anello benzenico. Questa combinazione tra aromatici e altri gruppi funzionali crea una varietà infinita di composti organici.
💡 Ricorda: La differenza tra aldeidi e chetoni sta nella posizione del carbonile - all'estremità per le aldeidi, all'interno per i chetoni!
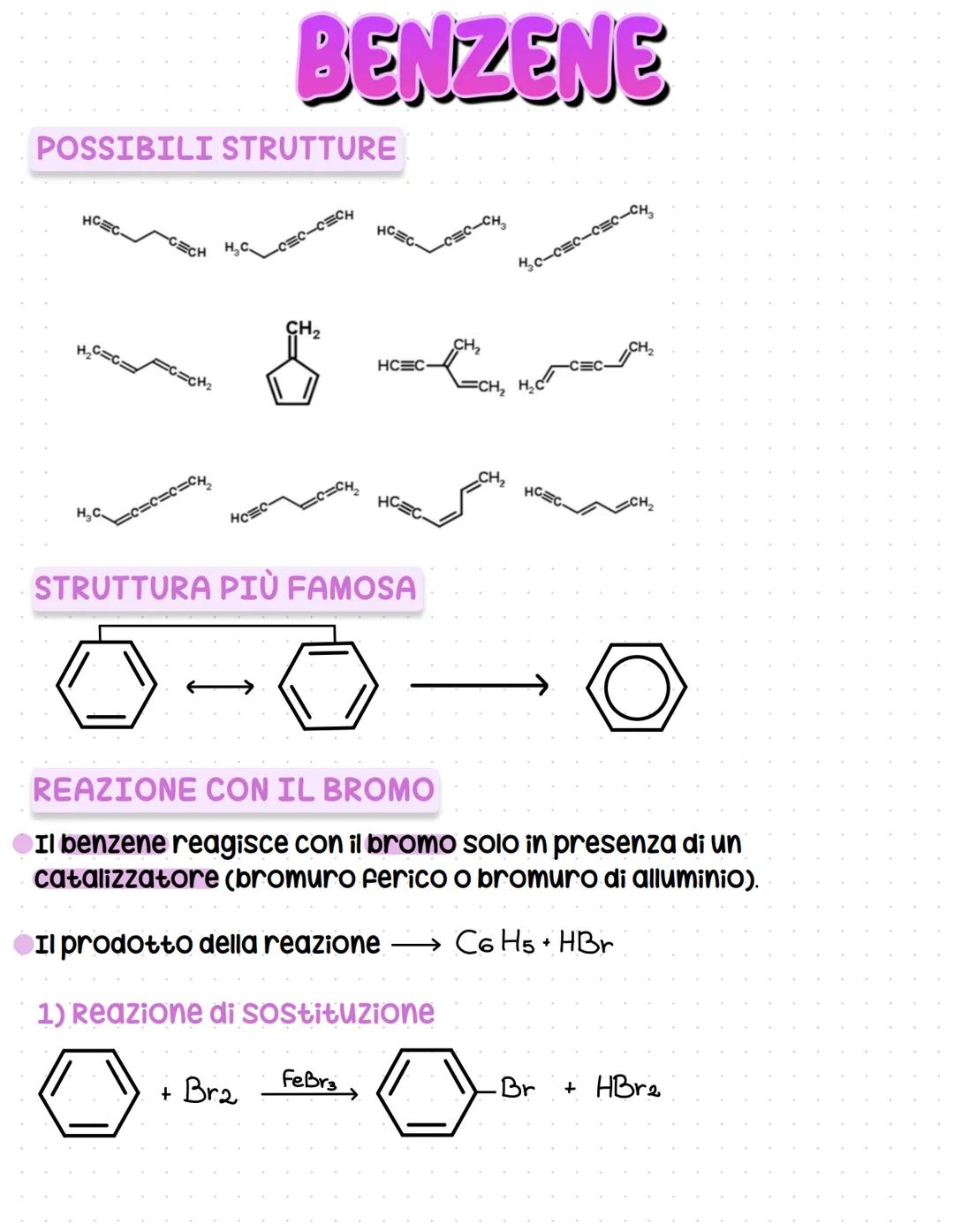
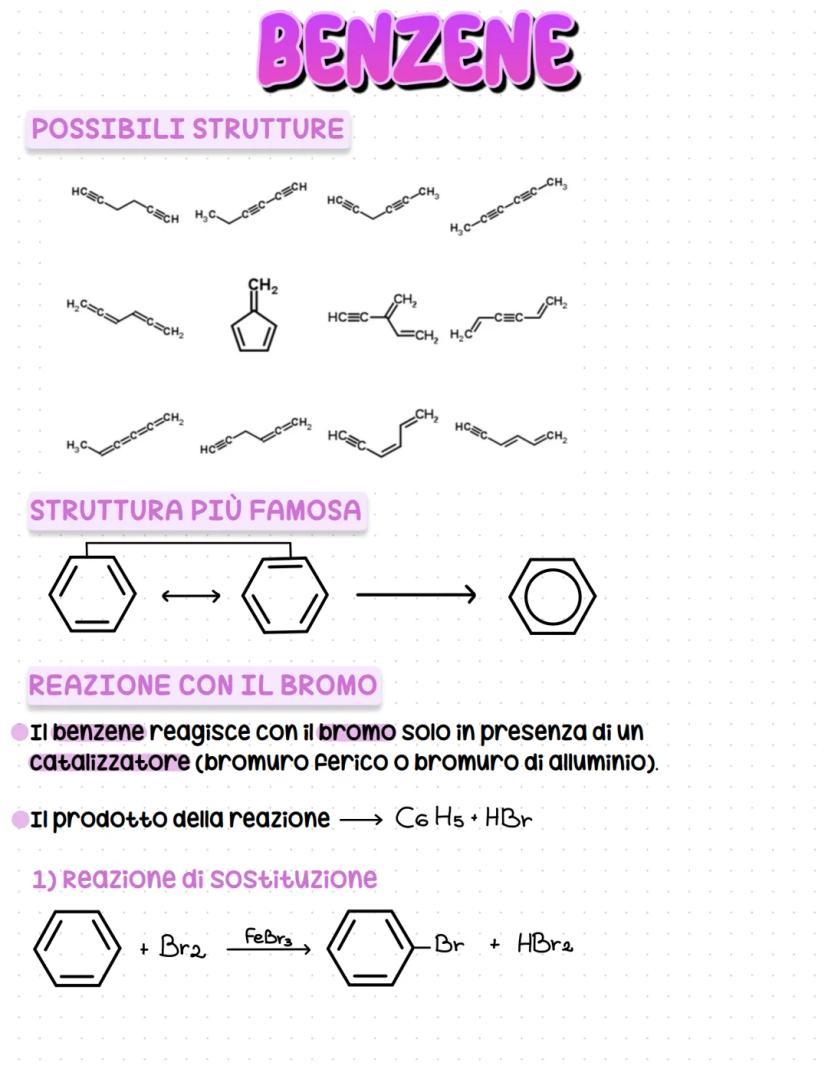
Il benzene ha formula C₆H₆ e può essere rappresentato in diversi modi. La struttura più famosa è quella dell'esagono con doppi legami alternati, proposta da Kekulé.
Quando il benzene reagisce con il bromo, succede qualcosa di particolare: serve un catalizzatore (come FeBr₃) e il prodotto è C₆H₅Br + HBr. Questa è una reazione di sostituzione, non di addizione come negli alcheni normali.
Un fatto importante: tutti gli atomi di carbonio nel benzene sono equivalenti. Per questo otteniamo un solo derivato monosostituito e solo tre diversi derivati disostituiti. Questo ci dice molto sulla simmetria della molecola.
⚗️ Esperimento chiave: Il benzene + Br₂ con FeBr₃ dà sostituzione, non addizione - questo è il primo indizio della sua natura speciale!
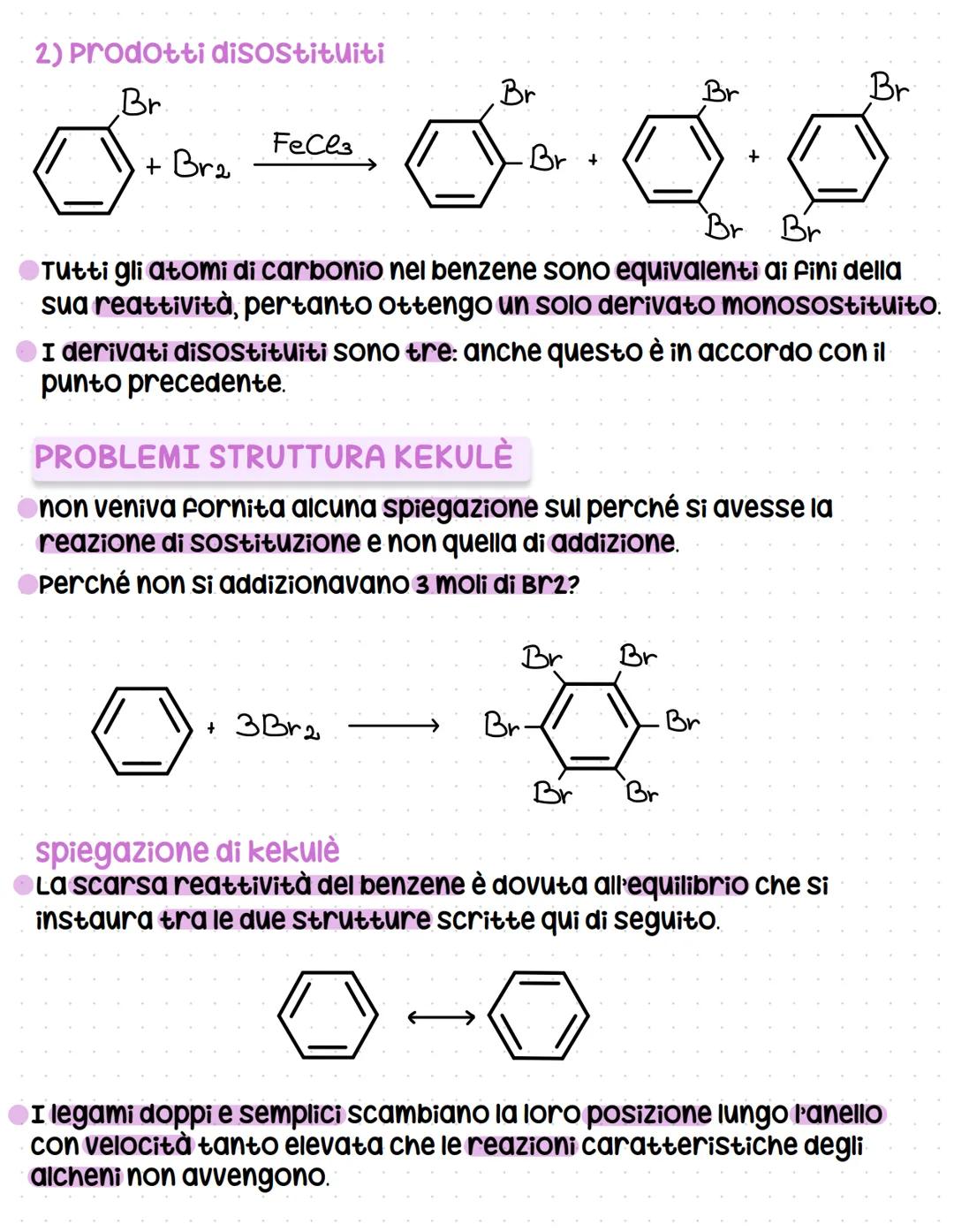
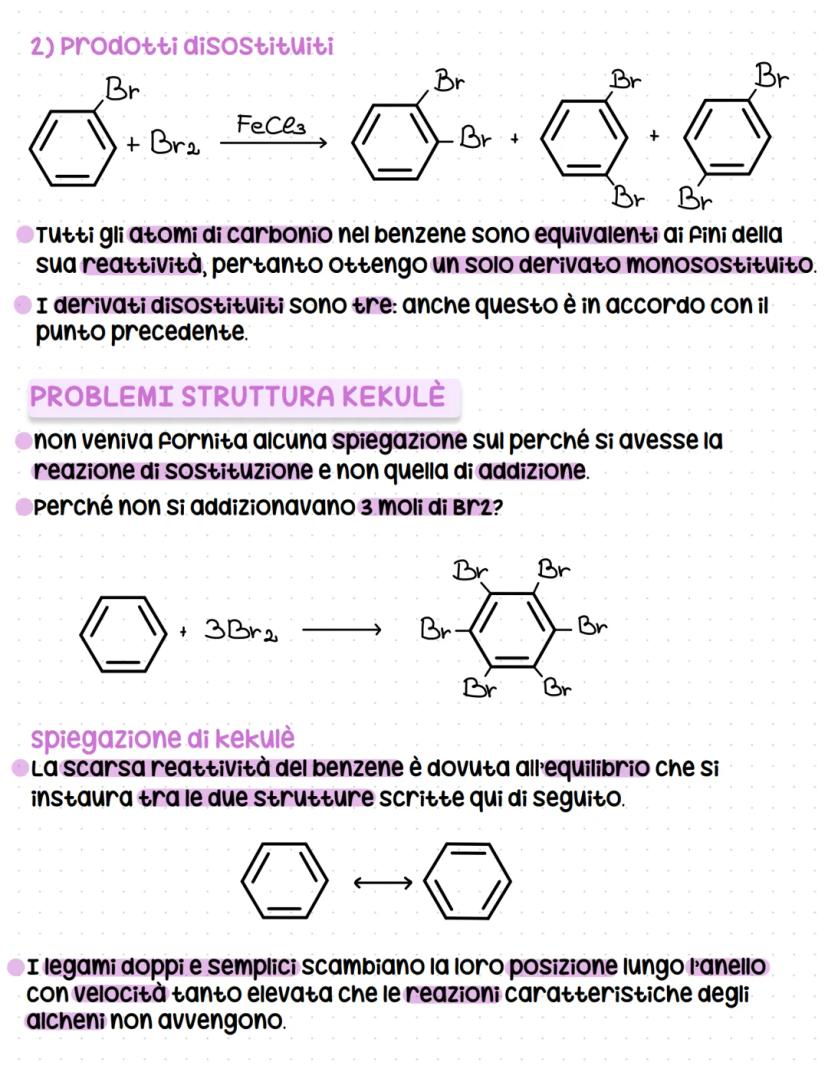
La struttura di Kekulé non spiegava perché il benzene desse reazioni di sostituzione invece che di addizione. Perché non si addizionavano 3 moli di Br₂ come ci aspetteremmo da un composto con tre doppi legami?
Kekulé propose che ci fosse un equilibrio rapido tra due strutture con doppi legami in posizioni diverse. Secondo lui, questo "spostamento" veloce dei doppi legami rendeva il composto poco reattivo verso le reazioni tipiche degli alcheni.
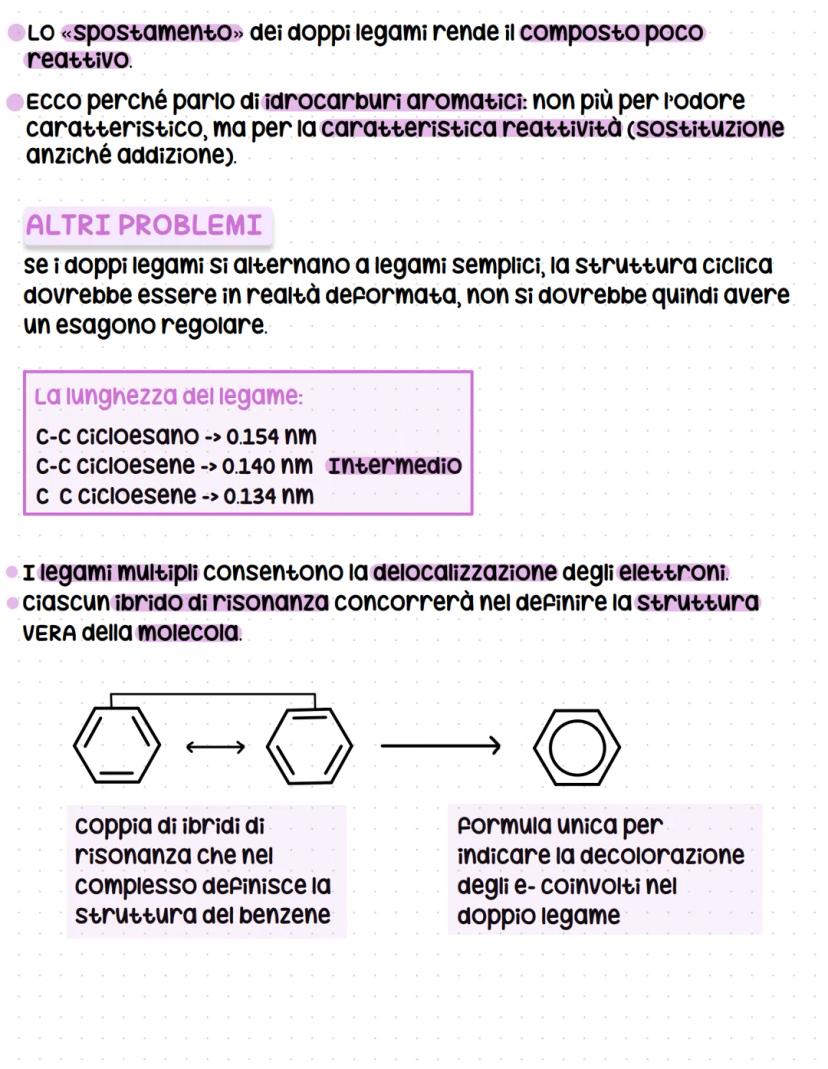
Però questa spiegazione aveva altri problemi: se i legami fossero davvero semplici e doppi alternati, l'esagono non dovrebbe essere regolare. Le lunghezze di legame misurate sperimentalmente sono tutte uguali e intermedie tra quelle di legami semplici e doppi.
🔍 Osservazione cruciale: Tutti i legami C-C nel benzene hanno la stessa lunghezza (0.140 nm) - né semplici né doppi, ma qualcosa di intermedio!
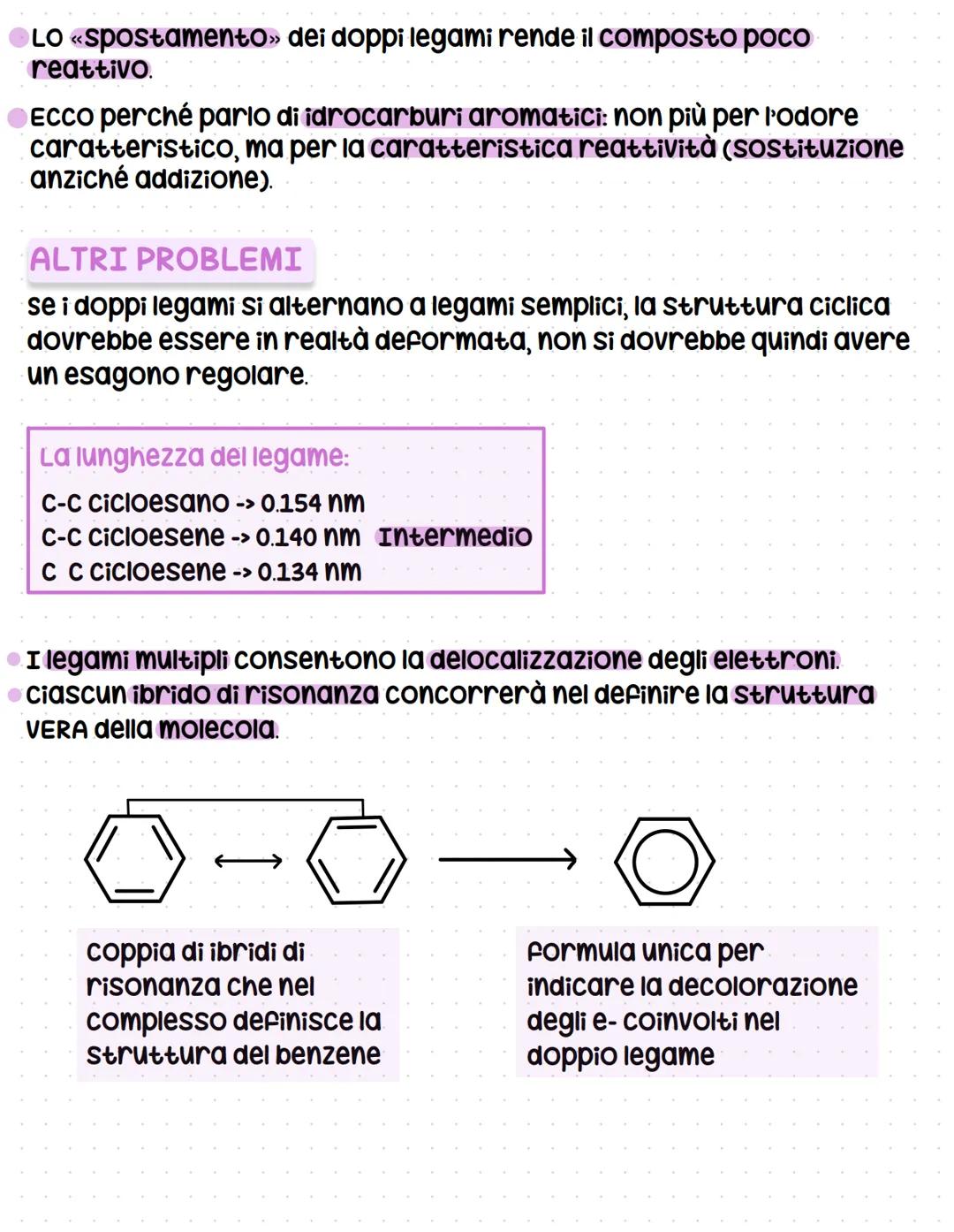
La vera struttura del benzene è un ibrido di risonanza tra le due strutture di Kekulé. I doppi legami sono delocalizzati su tutto l'anello, creando una nuvola elettronica uniforme.
Questa delocalizzazione si rappresenta spesso con un cerchio all'interno dell'esagono. Gli elettroni π non appartengono a legami specifici ma sono distribuiti uniformemente, rendendo tutti i legami C-C equivalenti.
La risonanza spiega perfettamente le proprietà osservate: lunghezze di legame intermedie, geometria regolare e stabilità particolare. Non esistono né legami semplici né doppi puri, ma un tipo intermedio di legame.
La delocalizzazione elettronica è la chiave per capire tutta la chimica aromatica. Ogni volta che vedi un anello benzenico, ricorda che gli elettroni sono "spalmati" su tutta la struttura.
📚 Concetto fondamentale: La risonanza non è un equilibrio tra strutture diverse - è una singola struttura ibrida più stabile!
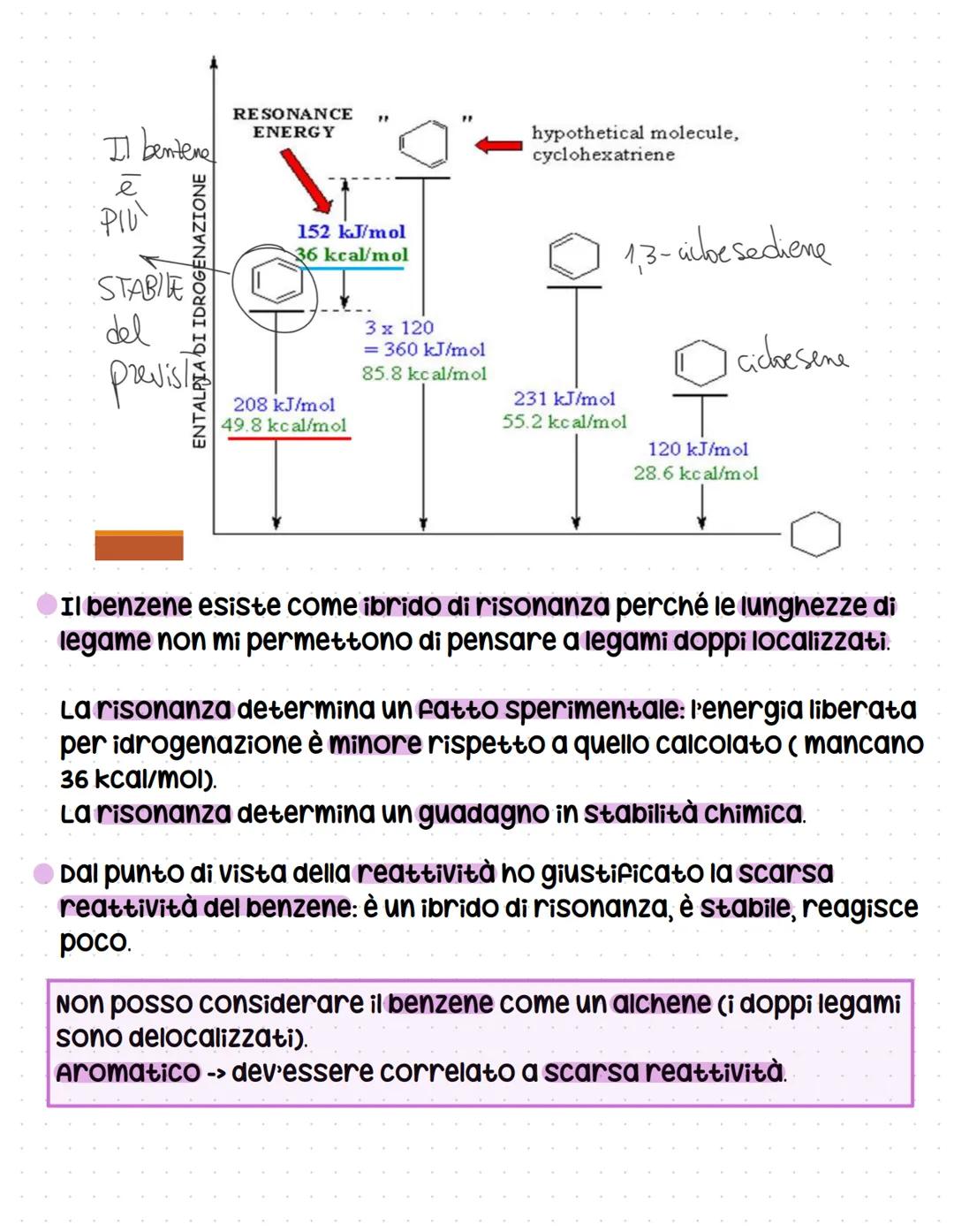
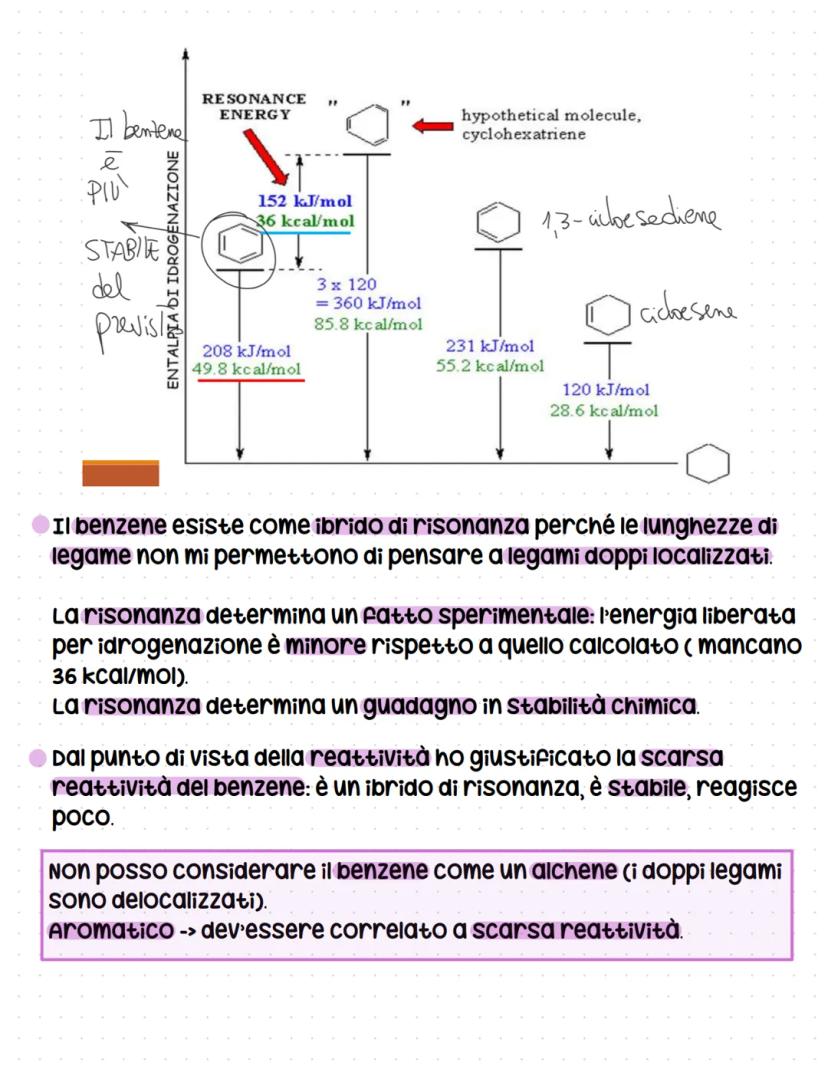
Il benzene è molto più stabile del previsto! L'energia di risonanza è di 152 kJ/mol - questa è l'energia "extra" di stabilità dovuta alla delocalizzazione.
Confrontando le entalpie di idrogenazione: il cicloesene rilascia 120 kJ/mol, il cicloesadiene 231 kJ/mol. Se il benzene fosse davvero un "cicloesatriene", dovrebbe rilasciare 360 kJ/mol, ma ne rilascia solo 208 kJ/mol.
Questa differenza di 152 kJ/mol è l'energia di risonanza - il "bonus" di stabilità che la delocalizzazione regala al benzene. È per questo che il benzene reagisce poco: è troppo stabile nella sua forma aromatica.
Dal punto di vista della reattività, ora capiamo perché il benzene non si comporta come un alchene normale. La sua stabilità extra lo rende riluttante a perdere l'aromaticità.
🎯 Punto chiave: Il benzene è 36 kcal/mol più stabile di quanto dovrebbe essere - questa energia extra spiega la sua scarsa reattività!

Nonostante abbia tre insaturazioni, il benzene non si comporta come gli alcheni o gli alchini. Non è un semplice cicloesatriene perché la sua energia di idrogenazione è troppo bassa.
La differenza tra energia calcolata e misurata conferma che il benzene è un ibrido di risonanza. Non esistono legami semplici e doppi distinti, ma un unico tipo di legame C-C con caratteristiche intermedie.
Questa struttura speciale spiega tutte le proprietà del benzene: geometria regolare, lunghezze di legame uniformi, stabilità eccezionale e reattività particolare.
Il concetto di aromaticità ora ha un significato preciso: non più l'odore piacevole, ma la presenza di elettroni π delocalizzati che conferiscono stabilità extra e reattività di sostituzione.
✨ Definizione moderna: Aromatico = elettroni π delocalizzati + stabilità extra + reazioni di sostituzione!
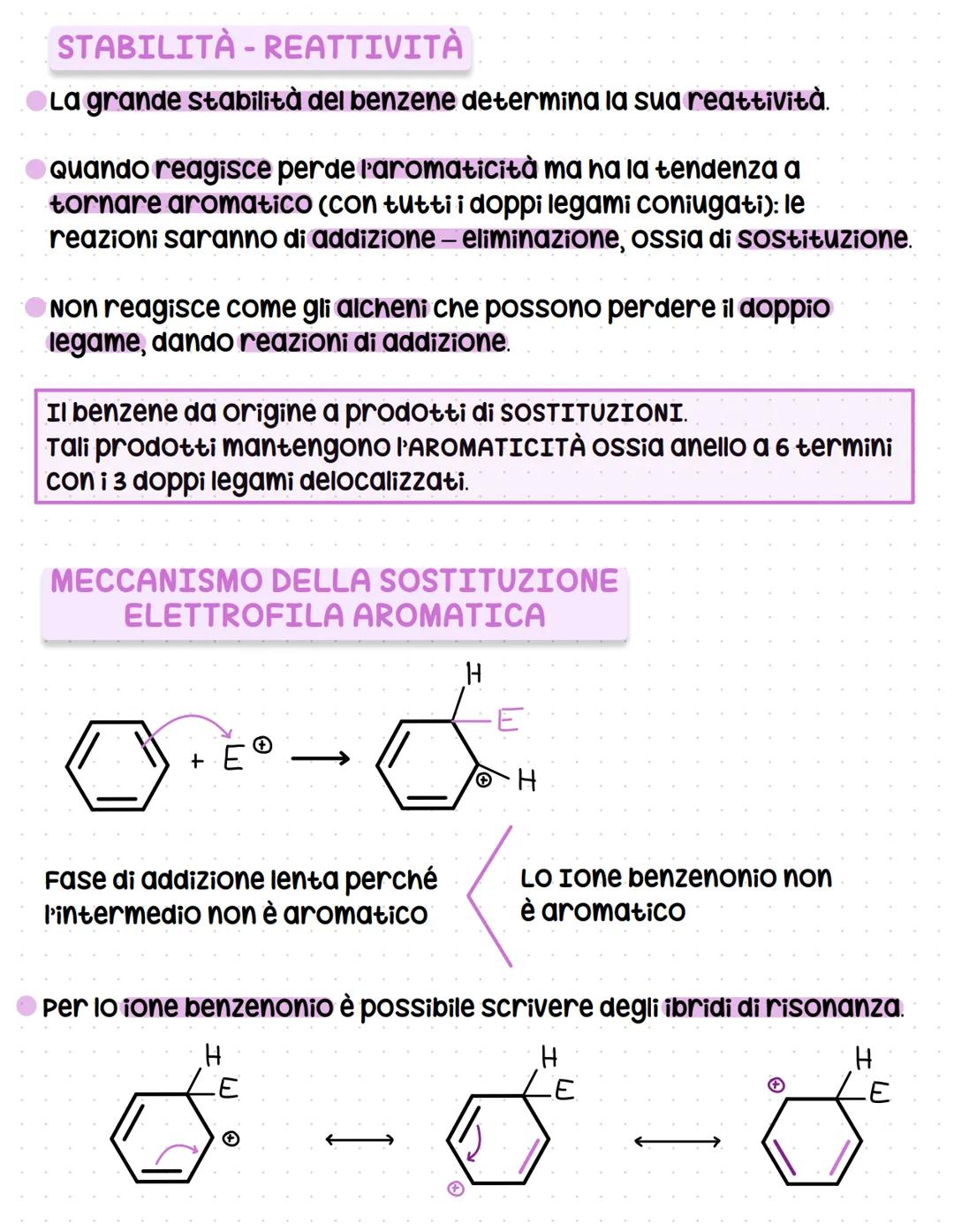
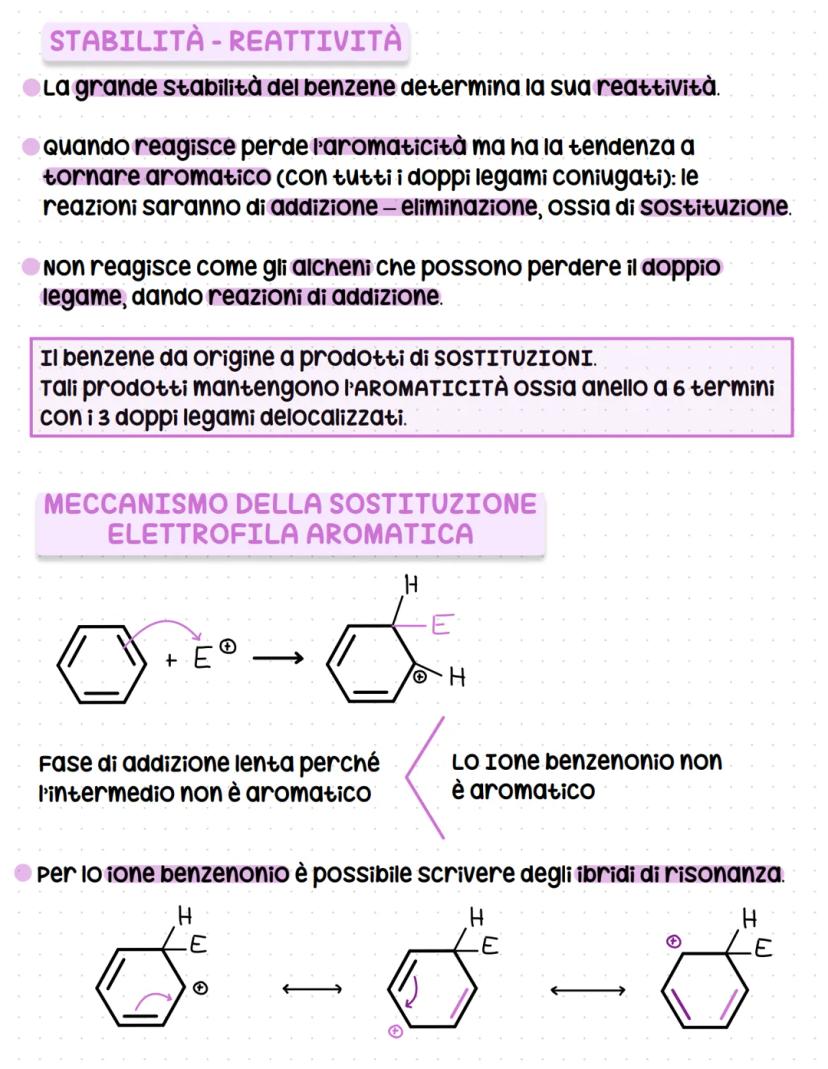
La grande stabilità del benzene determina il suo tipo di reattività. Quando reagisce, perde temporaneamente l'aromaticità ma tende subito a recuperarla - da qui le reazioni di sostituzione.
Il meccanismo della sostituzione elettrofila aromatica ha due fasi. Prima: un elettrofilo (E⁺) attacca l'anello formando lo ione benzenonio, che non è aromatico ma è stabilizzato per risonanza.
Lo ione benzenonio può essere rappresentato con tre strutture di risonanza diverse, tutte equivalenti. Questa risonanza compensa parzialmente la perdita di aromaticità.
Seconda fase: lo ione benzenonio perde un H⁺ per ripristinare l'aromaticità. Un nucleofilo agisce da base (non si addiziona!) perché l'obiettivo è sempre tornare alla struttura aromatica stabile.
⚡ Strategia della natura: Perdere temporaneamente l'aromaticità per poi riconquistarla - questo è il "trucco" del benzene!
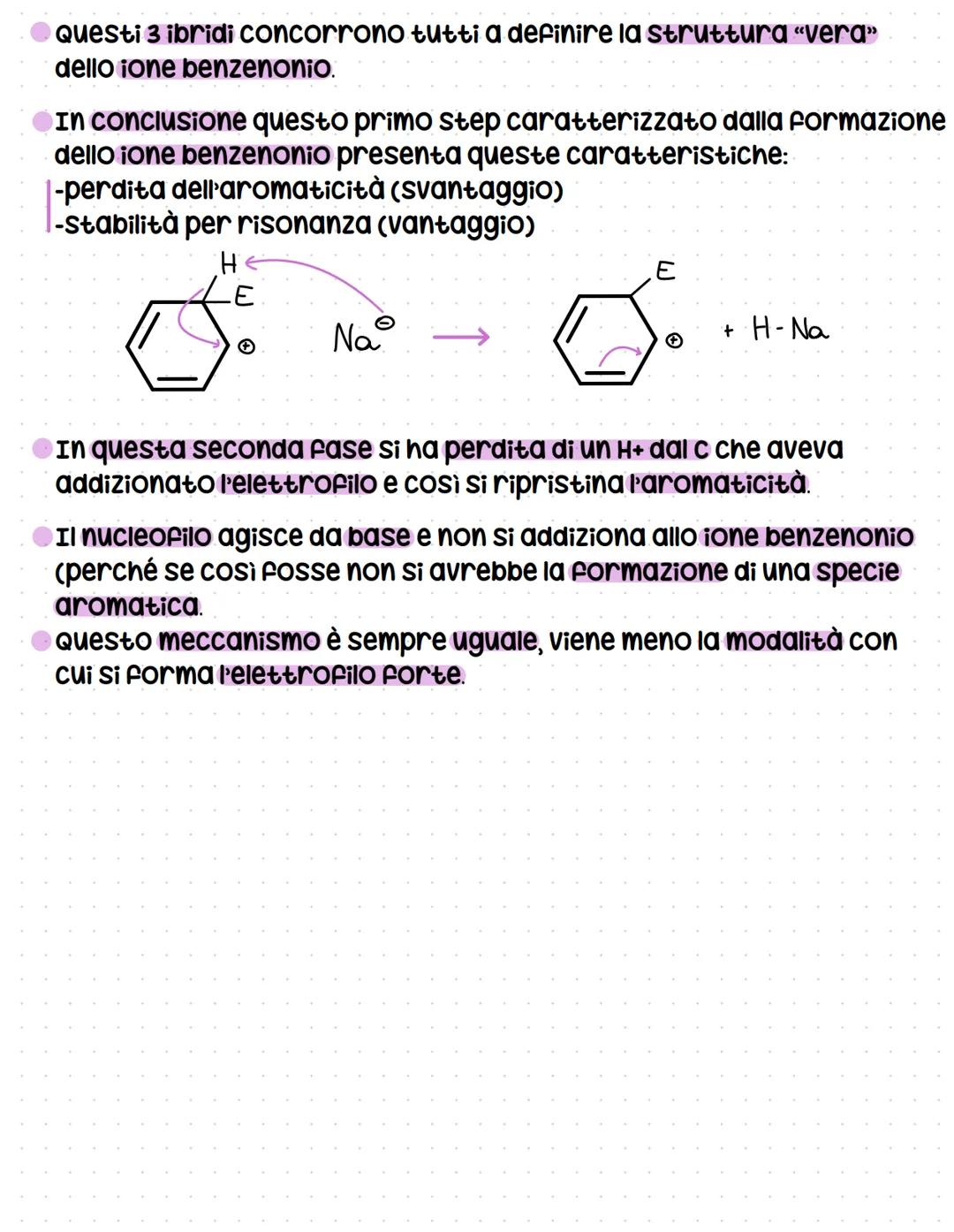
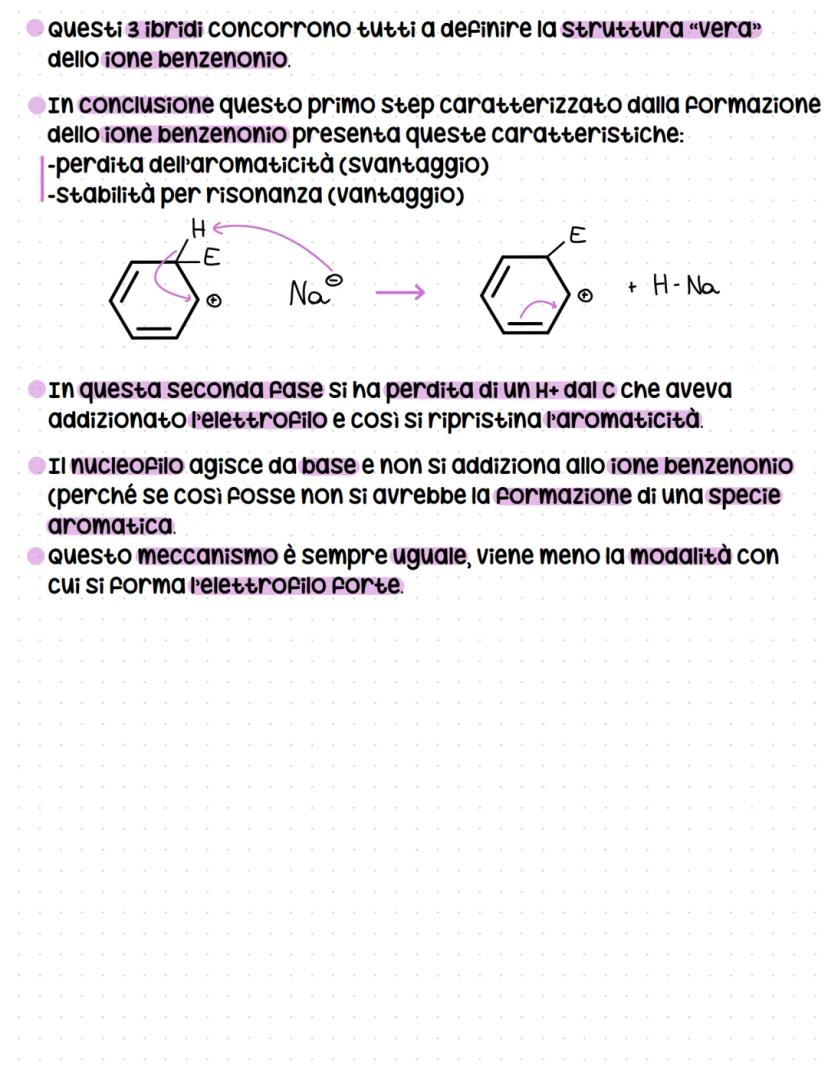
I tre ibridi di risonanza dello ione benzenonio concorrono tutti a definire la sua struttura reale. Questa risonanza è fondamentale per stabilizzare l'intermedio non aromatico.
Nella seconda fase, la perdita di H⁺ ripristina l'aromaticità. Il nucleofilo (rappresentato come Na⁻) agisce da base di Brønsted, strappando il protone invece di addizionarsi.
Se il nucleofilo si addizionasse, otterremmo un prodotto non aromatico - cosa che la natura evita a tutti i costi! L'aromaticità è troppo preziosa per essere sacrificata.
Questo meccanismo generale è sempre uguale per tutte le sostituzioni elettrofile aromatiche. Cambia solo il modo in cui si forma l'elettrofilo forte, ma i due step fondamentali rimangono identici.
🔄 Pattern universale: Attacco elettrofilo → intermedio non aromatico → perdita H⁺ → ritorno all'aromaticità!
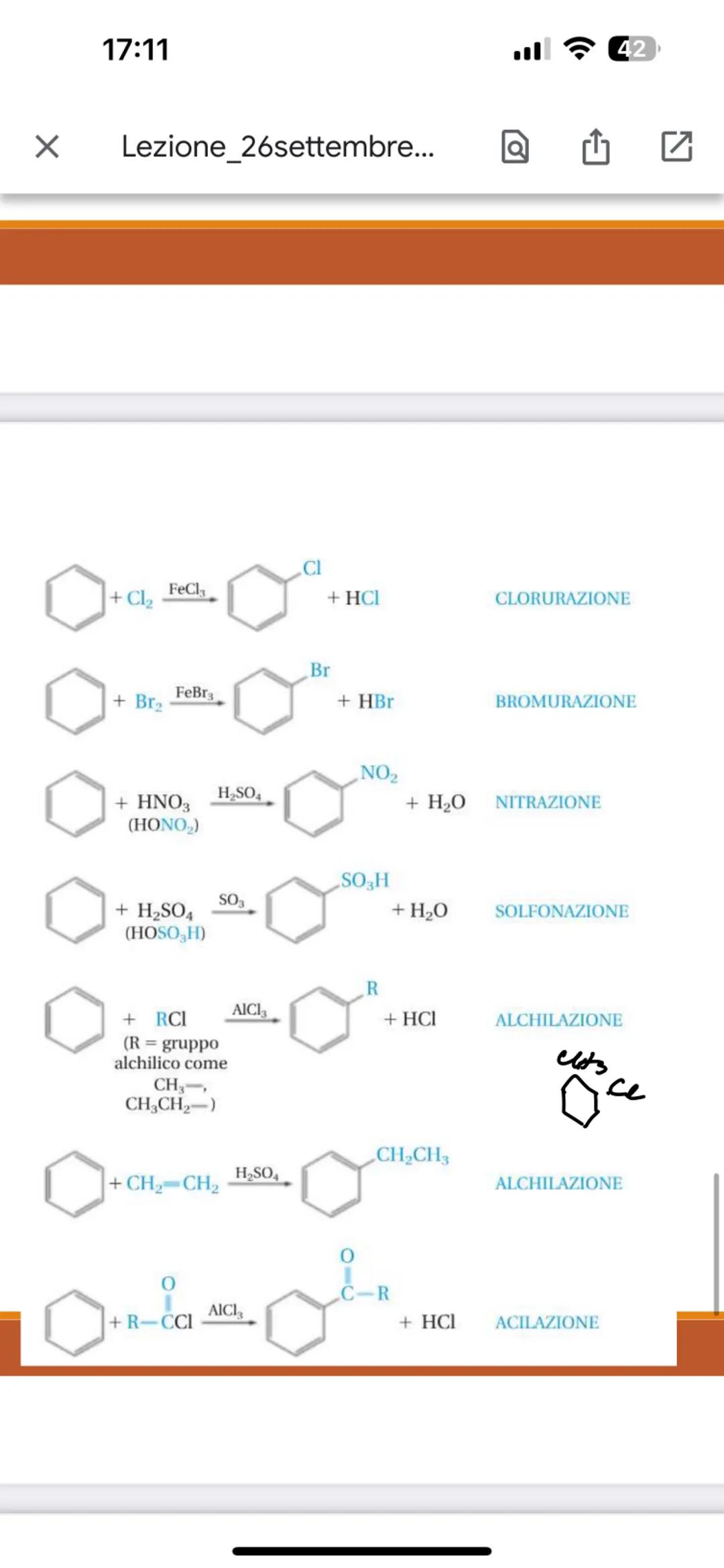
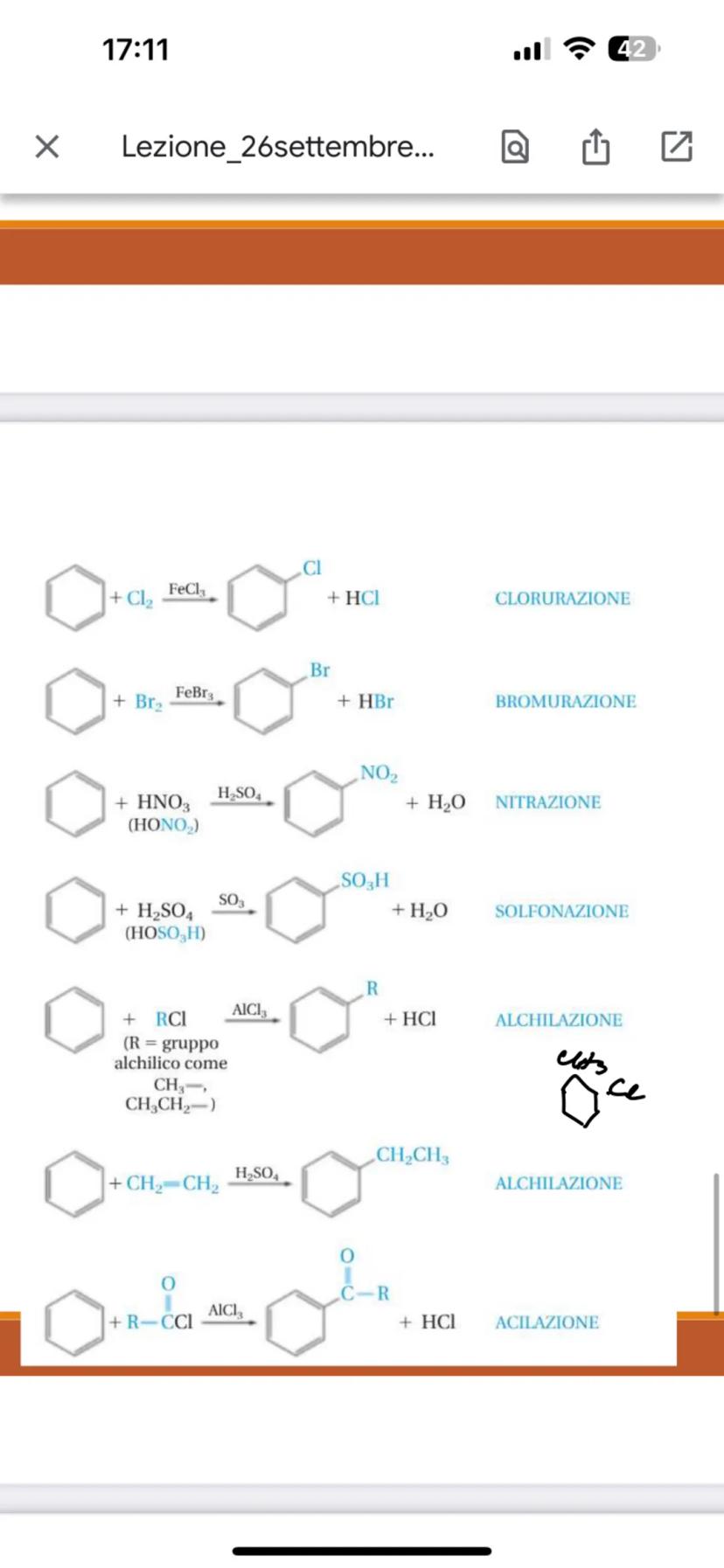
Le reazioni più importanti sono: clorurazione , bromurazione , nitrazione , solfonazione .
Ci sono anche l'alchilazione e l'acilazione . Ognuna introduce un gruppo diverso sull'anello benzenico.
Tutte seguono lo stesso meccanismo base: formazione dell'elettrofilo, attacco all'anello, perdita di H⁺. I catalizzatori acidi di Lewis (come FeCl₃, AlCl₃) sono spesso necessari per rendere gli elettrofili abbastanza reattivi.
Queste reazioni sono fondamentali nell'industria chimica per produrre farmaci, coloranti, esplosivi e mille altri composti utili.
🏭 Applicazione industriale: Ogni giorno vengono prodotte tonnellate di composti aromatici usando queste reazioni!
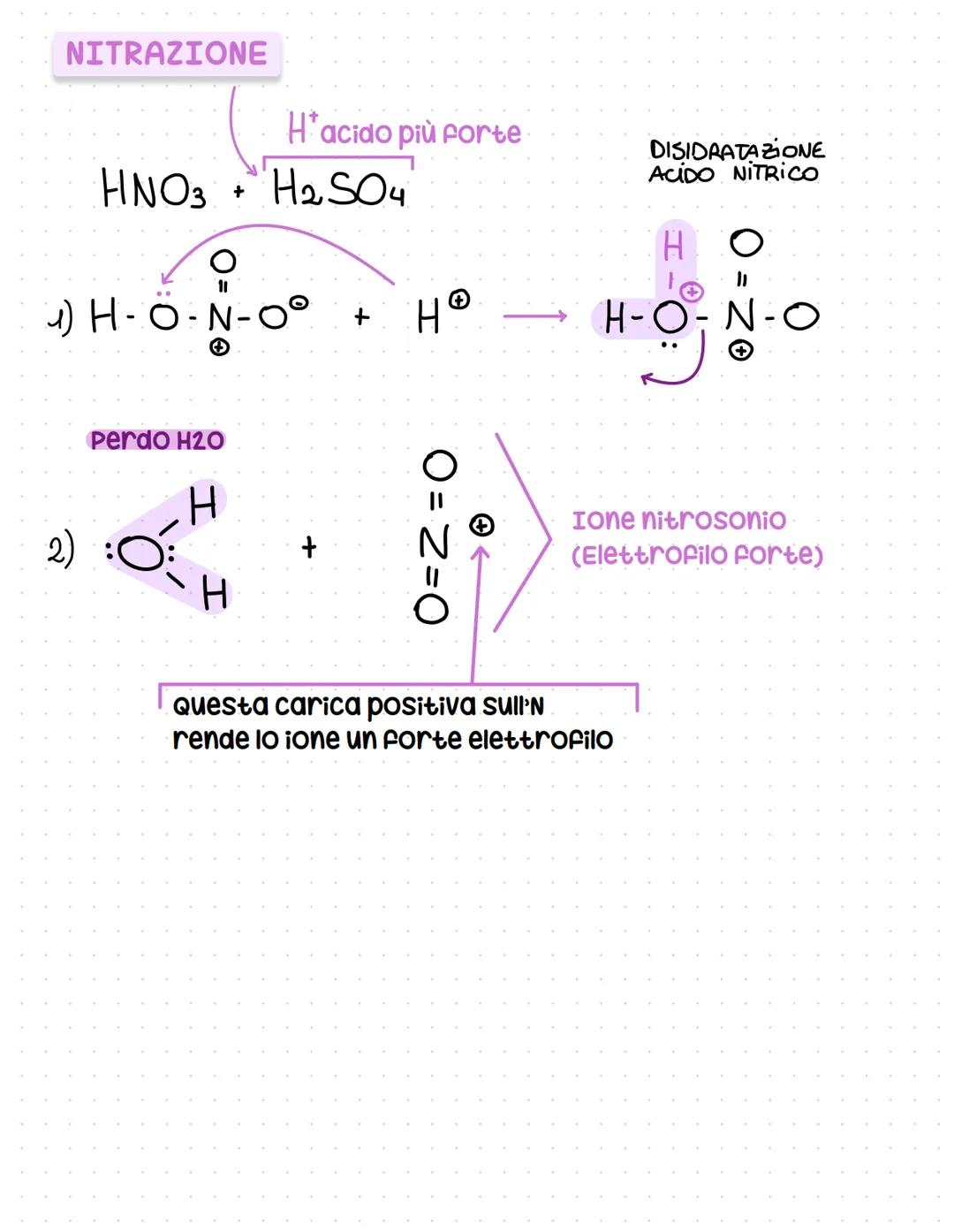
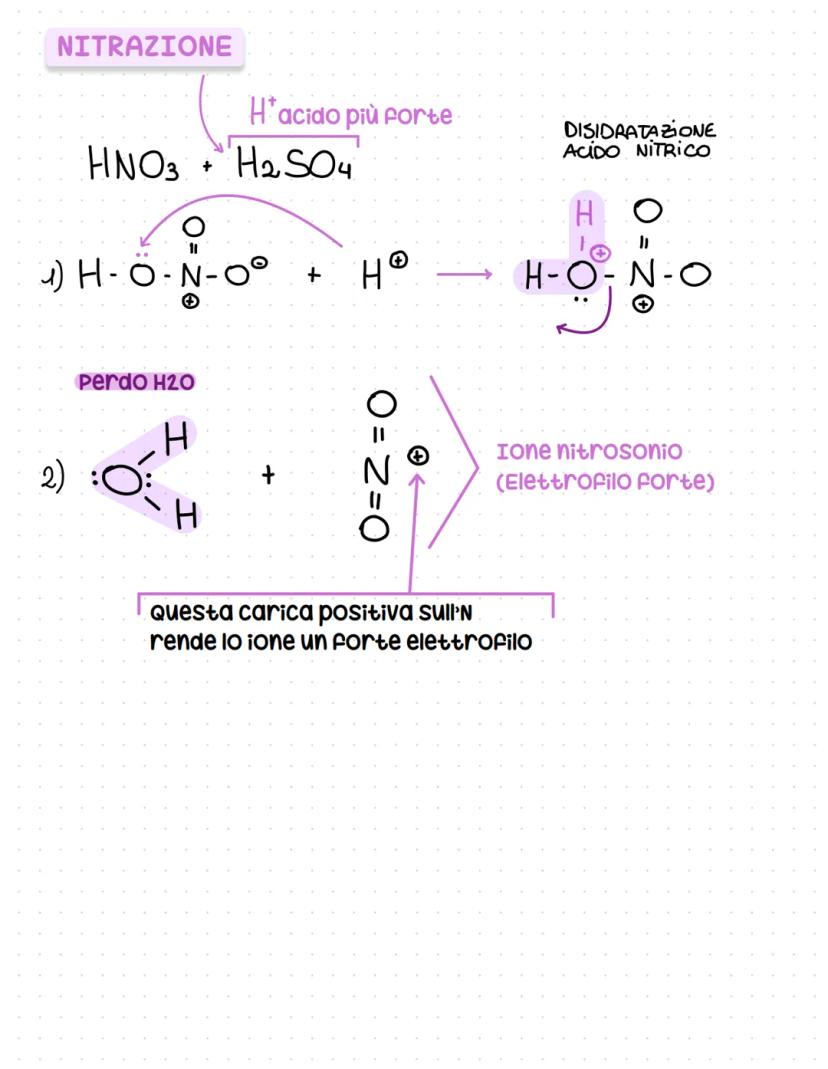
La nitrazione è una delle reazioni più importanti e usa una miscela di acido nitrico e solforico (miscela nitrante). L'acido solforico, più forte, protona l'acido nitrico.
Il meccanismo: HNO₃ viene protonato da H₂SO₄, poi perde acqua formando lo ione nitrosonio (NO₂⁺). Questo ione, con la carica positiva sull'azoto, è un elettrofilo molto forte.
Lo ione nitrosonio attacca poi l'anello benzenico seguendo il meccanismo standard di sostituzione elettrofila. Il prodotto finale è il nitrobenzene, importante per produrre esplosivi e coloranti.
La disidratazione dell'acido nitrico è la chiave per generare l'elettrofilo. Senza l'acido solforico, la reazione non procederebbe perché HNO₃ da solo non è elettrofilo abbastanza.
💥 Curiosità: Il nitrobenzene è il precursore di molti esplosivi - ecco perché la nitrazione è così studiata!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
Gli idrocarburi aromatici sono composti organici con una struttura particolare che li rende molto stabili e reattivi in modo diverso dagli alcheni. Il benzene è il rappresentante più importante di questa famiglia e capire la sua struttura e reattività ti... Mostra di più

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Il termine "aromatico" nasce dall'odore piacevole di questi composti, ma oggi indica una particolare reattività chimica. Il benzene è l'idrocarburo aromatico di riferimento, mentre gli areni sono tutti i composti che lo contengono.
Oltre agli aromatici, devi conoscere i principali gruppi funzionali: il gruppo carbonilico caratterizza aldeidi e chetoni, il gruppo carbinolico gli alcoli, e il gruppo carbossilico gli acidi carbossilici.
La benzaldeide è un esempio perfetto di come questi gruppi si combinano: è un'aldeide attaccata a un anello benzenico. Questa combinazione tra aromatici e altri gruppi funzionali crea una varietà infinita di composti organici.
💡 Ricorda: La differenza tra aldeidi e chetoni sta nella posizione del carbonile - all'estremità per le aldeidi, all'interno per i chetoni!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Il benzene ha formula C₆H₆ e può essere rappresentato in diversi modi. La struttura più famosa è quella dell'esagono con doppi legami alternati, proposta da Kekulé.
Quando il benzene reagisce con il bromo, succede qualcosa di particolare: serve un catalizzatore (come FeBr₃) e il prodotto è C₆H₅Br + HBr. Questa è una reazione di sostituzione, non di addizione come negli alcheni normali.
Un fatto importante: tutti gli atomi di carbonio nel benzene sono equivalenti. Per questo otteniamo un solo derivato monosostituito e solo tre diversi derivati disostituiti. Questo ci dice molto sulla simmetria della molecola.
⚗️ Esperimento chiave: Il benzene + Br₂ con FeBr₃ dà sostituzione, non addizione - questo è il primo indizio della sua natura speciale!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La struttura di Kekulé non spiegava perché il benzene desse reazioni di sostituzione invece che di addizione. Perché non si addizionavano 3 moli di Br₂ come ci aspetteremmo da un composto con tre doppi legami?
Kekulé propose che ci fosse un equilibrio rapido tra due strutture con doppi legami in posizioni diverse. Secondo lui, questo "spostamento" veloce dei doppi legami rendeva il composto poco reattivo verso le reazioni tipiche degli alcheni.
Però questa spiegazione aveva altri problemi: se i legami fossero davvero semplici e doppi alternati, l'esagono non dovrebbe essere regolare. Le lunghezze di legame misurate sperimentalmente sono tutte uguali e intermedie tra quelle di legami semplici e doppi.
🔍 Osservazione cruciale: Tutti i legami C-C nel benzene hanno la stessa lunghezza (0.140 nm) - né semplici né doppi, ma qualcosa di intermedio!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La vera struttura del benzene è un ibrido di risonanza tra le due strutture di Kekulé. I doppi legami sono delocalizzati su tutto l'anello, creando una nuvola elettronica uniforme.
Questa delocalizzazione si rappresenta spesso con un cerchio all'interno dell'esagono. Gli elettroni π non appartengono a legami specifici ma sono distribuiti uniformemente, rendendo tutti i legami C-C equivalenti.
La risonanza spiega perfettamente le proprietà osservate: lunghezze di legame intermedie, geometria regolare e stabilità particolare. Non esistono né legami semplici né doppi puri, ma un tipo intermedio di legame.
La delocalizzazione elettronica è la chiave per capire tutta la chimica aromatica. Ogni volta che vedi un anello benzenico, ricorda che gli elettroni sono "spalmati" su tutta la struttura.
📚 Concetto fondamentale: La risonanza non è un equilibrio tra strutture diverse - è una singola struttura ibrida più stabile!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Il benzene è molto più stabile del previsto! L'energia di risonanza è di 152 kJ/mol - questa è l'energia "extra" di stabilità dovuta alla delocalizzazione.
Confrontando le entalpie di idrogenazione: il cicloesene rilascia 120 kJ/mol, il cicloesadiene 231 kJ/mol. Se il benzene fosse davvero un "cicloesatriene", dovrebbe rilasciare 360 kJ/mol, ma ne rilascia solo 208 kJ/mol.
Questa differenza di 152 kJ/mol è l'energia di risonanza - il "bonus" di stabilità che la delocalizzazione regala al benzene. È per questo che il benzene reagisce poco: è troppo stabile nella sua forma aromatica.
Dal punto di vista della reattività, ora capiamo perché il benzene non si comporta come un alchene normale. La sua stabilità extra lo rende riluttante a perdere l'aromaticità.
🎯 Punto chiave: Il benzene è 36 kcal/mol più stabile di quanto dovrebbe essere - questa energia extra spiega la sua scarsa reattività!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Nonostante abbia tre insaturazioni, il benzene non si comporta come gli alcheni o gli alchini. Non è un semplice cicloesatriene perché la sua energia di idrogenazione è troppo bassa.
La differenza tra energia calcolata e misurata conferma che il benzene è un ibrido di risonanza. Non esistono legami semplici e doppi distinti, ma un unico tipo di legame C-C con caratteristiche intermedie.
Questa struttura speciale spiega tutte le proprietà del benzene: geometria regolare, lunghezze di legame uniformi, stabilità eccezionale e reattività particolare.
Il concetto di aromaticità ora ha un significato preciso: non più l'odore piacevole, ma la presenza di elettroni π delocalizzati che conferiscono stabilità extra e reattività di sostituzione.
✨ Definizione moderna: Aromatico = elettroni π delocalizzati + stabilità extra + reazioni di sostituzione!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La grande stabilità del benzene determina il suo tipo di reattività. Quando reagisce, perde temporaneamente l'aromaticità ma tende subito a recuperarla - da qui le reazioni di sostituzione.
Il meccanismo della sostituzione elettrofila aromatica ha due fasi. Prima: un elettrofilo (E⁺) attacca l'anello formando lo ione benzenonio, che non è aromatico ma è stabilizzato per risonanza.
Lo ione benzenonio può essere rappresentato con tre strutture di risonanza diverse, tutte equivalenti. Questa risonanza compensa parzialmente la perdita di aromaticità.
Seconda fase: lo ione benzenonio perde un H⁺ per ripristinare l'aromaticità. Un nucleofilo agisce da base (non si addiziona!) perché l'obiettivo è sempre tornare alla struttura aromatica stabile.
⚡ Strategia della natura: Perdere temporaneamente l'aromaticità per poi riconquistarla - questo è il "trucco" del benzene!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
I tre ibridi di risonanza dello ione benzenonio concorrono tutti a definire la sua struttura reale. Questa risonanza è fondamentale per stabilizzare l'intermedio non aromatico.
Nella seconda fase, la perdita di H⁺ ripristina l'aromaticità. Il nucleofilo (rappresentato come Na⁻) agisce da base di Brønsted, strappando il protone invece di addizionarsi.
Se il nucleofilo si addizionasse, otterremmo un prodotto non aromatico - cosa che la natura evita a tutti i costi! L'aromaticità è troppo preziosa per essere sacrificata.
Questo meccanismo generale è sempre uguale per tutte le sostituzioni elettrofile aromatiche. Cambia solo il modo in cui si forma l'elettrofilo forte, ma i due step fondamentali rimangono identici.
🔄 Pattern universale: Attacco elettrofilo → intermedio non aromatico → perdita H⁺ → ritorno all'aromaticità!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Le reazioni più importanti sono: clorurazione , bromurazione , nitrazione , solfonazione .
Ci sono anche l'alchilazione e l'acilazione . Ognuna introduce un gruppo diverso sull'anello benzenico.
Tutte seguono lo stesso meccanismo base: formazione dell'elettrofilo, attacco all'anello, perdita di H⁺. I catalizzatori acidi di Lewis (come FeCl₃, AlCl₃) sono spesso necessari per rendere gli elettrofili abbastanza reattivi.
Queste reazioni sono fondamentali nell'industria chimica per produrre farmaci, coloranti, esplosivi e mille altri composti utili.
🏭 Applicazione industriale: Ogni giorno vengono prodotte tonnellate di composti aromatici usando queste reazioni!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La nitrazione è una delle reazioni più importanti e usa una miscela di acido nitrico e solforico (miscela nitrante). L'acido solforico, più forte, protona l'acido nitrico.
Il meccanismo: HNO₃ viene protonato da H₂SO₄, poi perde acqua formando lo ione nitrosonio (NO₂⁺). Questo ione, con la carica positiva sull'azoto, è un elettrofilo molto forte.
Lo ione nitrosonio attacca poi l'anello benzenico seguendo il meccanismo standard di sostituzione elettrofila. Il prodotto finale è il nitrobenzene, importante per produrre esplosivi e coloranti.
La disidratazione dell'acido nitrico è la chiave per generare l'elettrofilo. Senza l'acido solforico, la reazione non procederebbe perché HNO₃ da solo non è elettrofilo abbastanza.
💥 Curiosità: Il nitrobenzene è il precursore di molti esplosivi - ecco perché la nitrazione è così studiata!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
34
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
nomenclatura e proprietà fisiche reazioni aldeidi chetoni
Equilibrio, principio di Le Chatelier, prodotto di solubilità
Reazioni e sintesi degli alcoli + esercizi svolti
Teoria degli urti, velocità di reazione, principio di le chatelier
in questa raccolta troverete : informazioni base sull olio , i lipidi e le loro funzioni ,i gliceridi,le cere , i fosfolipidi, i glicolipidi , gli steroidi ,i terpeni e le vitamine liposolubili
appunti sulla velocità di reazione, equazione cinetica, teoria degli urti e meccanismo di reazione
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS