Bene, oggi esploriamo il mondo affascinante della chimica organica-... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
311
•
Aggiornato Apr 28, 2026
•
Sara Negossi
@saranegossi
Bene, oggi esploriamo il mondo affascinante della chimica organica-... Mostra di più










Perché dovresti interessarti alla chimica organica? Semplice: tutto quello che ti circonda - dalla plastica del tuo smartphone ai carburanti che muovono le auto - è fatto di composti organici!
I composti organici hanno quattro caratteristiche fondamentali: contengono sempre carbonio, sono incredibilmente complessi, esistono in infinite varietà e sono ottimi combustibili. Ecco perché benzina, carbone e gas naturale bruciano così bene - sono tutti miscele di composti organici.
Gli elementi più importanti in chimica organica si chiamano CHNOPS: carbonio, idrogeno, azoto, ossigeno, fosforo e zolfo. Nonostante non siano gli elementi più abbondanti sulla Terra, sono alla base di tutta la vita.
💡 Curiosità: La chimica organica è anche chiamata "chimica del carbonio" perché tutti i composti organici hanno forti legami carbonio-carbonio come struttura portante!

Per capire come si comporta il carbonio, devi prima conoscere gli orbitali - quelle regioni dello spazio dove hai il 95% di probabilità di trovare un elettrone. Non sono orbite fisse, ma volumi con forme diverse!
I quattro numeri quantici descrivono completamente ogni elettrone:
La configurazione elettronica ti dice come sono distribuiti gli elettroni nei vari livelli. Per esempio, lo zolfo (16 elettroni) ha configurazione: 1s² 2s² 2p⁶ 3s² 3p⁴.
💡 Ricorda: La regola dell'ottetto dice che gli atomi sono stabili quando hanno 8 elettroni nel livello più esterno - per questo si legano tra loro!

Il riempimento degli orbitali segue un ordine preciso: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s... Sembra complicato? C'è uno schema visivo che ti aiuta a ricordarlo!
La regola dell'ottetto è il principio fondamentale: ogni atomo vuole avere 8 elettroni nel livello più esterno per essere stabile (come i gas nobili). Per raggiungerlo, gli atomi possono cedere, acquistare o condividere elettroni.
Gli atomi si legano quando l'energia del sistema unito è minore di quella degli atomi separati. È come dire che "l'unione fa la forza" anche nel mondo atomico!
I legami chimici dipendono dagli elettroni di valenza (quelli nel livello più esterno). Gli elementi dei primi gruppi hanno orbitali "quasi vuoti", quelli degli ultimi gruppi li hanno "quasi pieni".
💡 Tip per l'esame: Memorizza che il primo livello può contenere al massimo 2 elettroni - per questo si parla di "regola dell'ottetto-duetto"!

La differenza di elettronegatività (ΔEn) tra due atomi determina che tipo di legame si formerà. È come un "tira e molla" per gli elettroni!
Legame covalente puro : gli elettroni sono condivisi equamente, come in O₂ o tra atomi identici.
Legame covalente polare (0,4 < ΔEn < 1,7): gli elettroni "preferiscono" stare vicino all'atomo più elettronegativo. L'acqua è l'esempio perfetto!
Legame ionico (ΔEn > 1,7): l'elettrone si trasferisce completamente dall'atomo meno elettronegativo a quello più elettronegativo. Si formano ioni con cariche opposte che si attraggono.
Nel legame ionico hai cationi (positivi, hanno perso elettroni) e anioni (negativi, hanno guadagnato elettroni). Questi si organizzano in reticoli cristallini tridimensionali - non sono molecole!
💡 Memoria visiva: Pensa al sale da cucina (NaCl) - è il classico esempio di legame ionico che forma cristalli!

I legami covalenti possono essere singoli, doppi o tripli. Il primo legame è sempre sigma (sovrapposizione frontale), i successivi sono pi greco (sovrapposizione laterale).
Nel legame covalente eteropolare, gli elettroni si posizionano più vicino all'atomo più elettronegativo, creando cariche parziali . La molecola diventa un dipolo - elettricamente neutra ma con separazione di cariche.
Il legame metallico è speciale: gli elettroni di valenza sono "delocalizzati" e si muovono liberamente intorno a tutti i cationi del metallo. È come un mare di elettroni che tiene insieme il reticolo!
Questa struttura spiega le proprietà dei metalli: conducono elettricità (elettroni mobili), sono duttili e malleabili (i cationi possono scivolare senza rompere i legami).
💡 Connessione pratica: I fili elettrici sono di rame proprio per la delocalizzazione elettronica del legame metallico!

Ora arriviamo al protagonista: il carbonio! Ha configurazione elettronica 1s² 2s² 2p², quindi dovrebbe formare solo 2 legami... invece ne forma sempre 4. Come mai?
La risposta è l'ibridazione - il carbonio "adatta" i suoi orbitali per formare legami più stabili ed efficienti. Nello stato eccitato, un elettrone passa dall'orbitale 2s al 2p vuoto, creando 4 elettroni spaiati.
Gli orbitali ibridi si formano mescolando orbitali diversi (s, p) dello stesso atomo. Questo processo costa un po' di energia, ma il guadagno energetico dai legami formati è molto maggiore!
Il carbonio può formare catene lunghissime con se stesso grazie ai legami covalenti omopolari molto stabili. Può creare strutture lineari, ramificate o ad anello - sempre mantenendo 4 legami intorno a sé.
💡 Esempio pratico: Pensa ai diamanti - sono reticoli tridimensionali di carbonio dove ogni atomo è legato tetraedricamente ad altri 4 atomi di carbonio!

L'ibridazione avviene quando gli atomi sono in stato eccitato e la loro configurazione elettronica cambia temporaneamente. Un elettrone di coppia può spostarsi in un orbitale vuoto di energia leggermente superiore.
Prendiamo il berillio come esempio: normalmente ha configurazione 2s², ma nello stato eccitato diventa 2s¹ 2p¹. I due orbitali con singoletti si mescolano formando due orbitali ibridi identici.
Nel carbonio, la configurazione passa da 2s² 2p² a 2s¹ 2p³, creando 4 elettroni spaiati pronti a formare legami. Questi si possono ibridare in modi diversi secondo le necessità della molecola.
L'ibridazione permette di formare più legami covalenti e rende le molecole più stabili. È come se l'atomo si "riarrangiasse" per ottenere la configurazione più vantaggiosa.
💡 Concetto chiave: L'ibridazione spiega perché il carbonio, pur avendo solo 2 elettroni spaiati nella configurazione base, può sempre formare 4 legami!

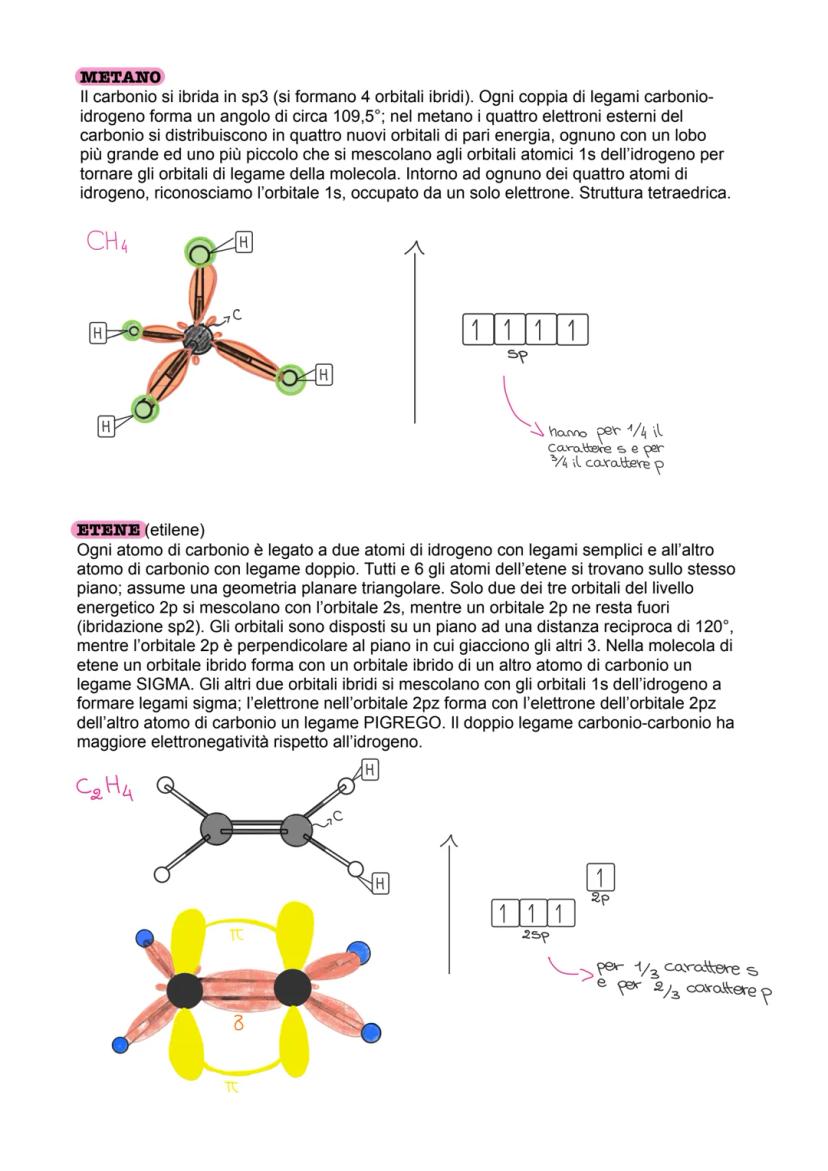
Ibridazione sp³: L'orbitale 2s si mescola con tutti e 3 gli orbitali 2p, formando 4 orbitali ibridi identici. Geometria tetraedrica con angoli di 109,5°. Esempio: metano (CH₄).
Ibridazione sp²: L'orbitale 2s si mescola con 2 orbitali 2p, lasciandone uno libero. Si formano 3 orbitali ibridi su un piano (120° tra loro) + 1 orbitale p perpendicolare. Geometria planare triangolare.
Ibridazione sp: L'orbitale 2s si mescola con 1 solo orbitale 2p. Si formano 2 orbitali ibridi opposti (180°) + 2 orbitali p perpendicolari. Geometria lineare.
Ogni tipo di ibridazione ha caratteristiche diverse: sp³ ha carattere s per 1/4 e p per 3/4, sp² ha carattere s per 1/3 e p per 2/3, sp ha carattere s e p al 50%.
💡 Trucco per ricordare: sp³ = 4 legami/tetraedro, sp² = 3 ibridi + 1 doppio legame/piano, sp = 2 ibridi + 2 legami multipli/lineare!
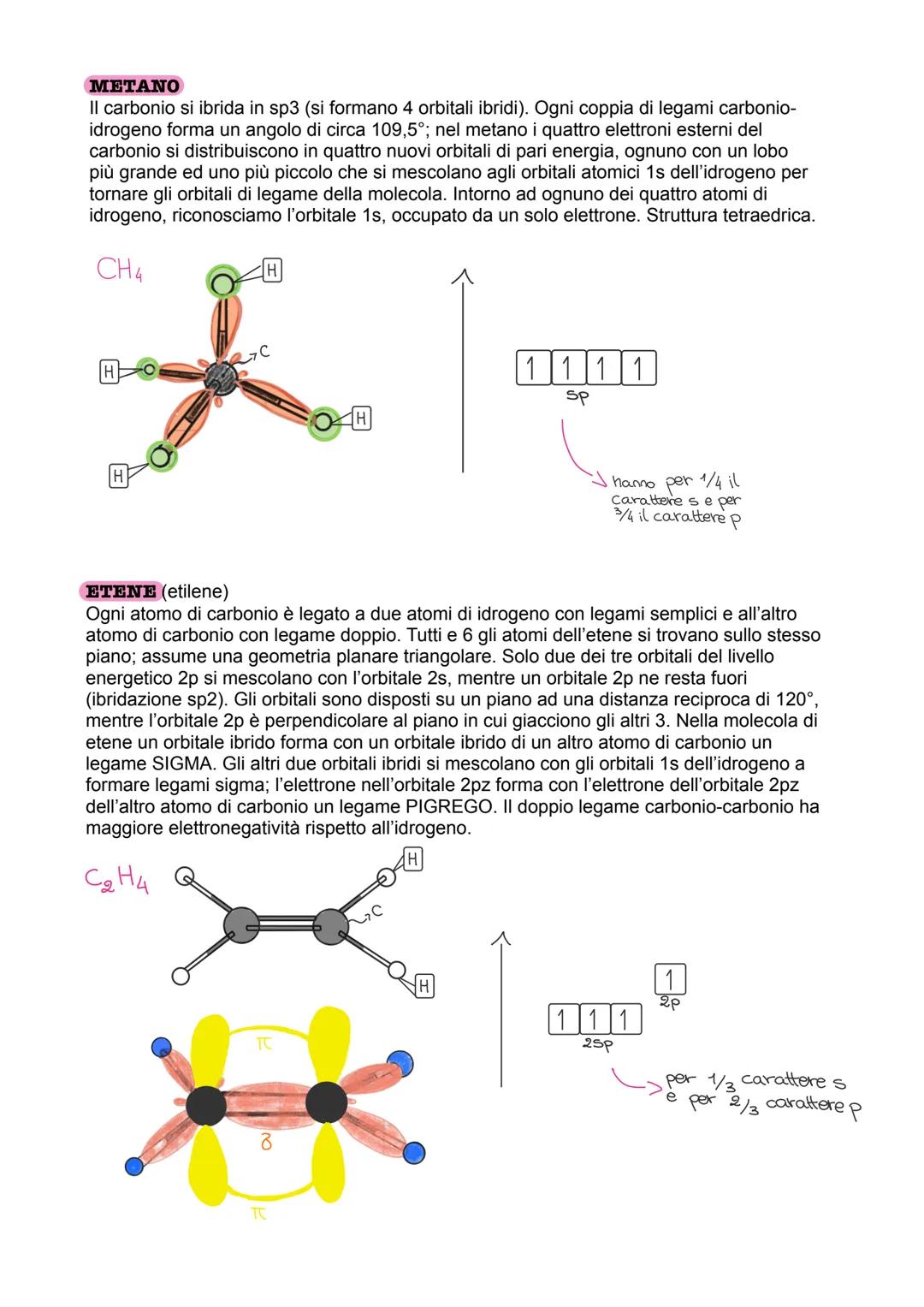
Metano (CH₄): Il carbonio è ibridato sp³, formando una struttura tetraedrica perfetta. I 4 orbitali ibridi si sovrappongono agli orbitali 1s degli idrogeni, creando 4 legami sigma identici con angoli di 109,5°.
Etene (C₂H₄): Ogni carbonio è ibridato sp², creando una molecola planare. Tra i due carboni si forma un legame doppio: un sigma (forte) più un pi greco (più debole). Gli angoli sono di 120°.
Il legame sigma si forma sempre per primo dalla sovrapposizione frontale degli orbitali. I legami pi greco derivano dalla sovrapposizione laterale e sono più deboli.
Nel doppio legame C=C dell'etene, la rotazione è impedita dal legame pi greco. Questo crea la possibilità di isomeria geometrica - molecole con stessa formula ma disposizione spaziale diversa.
💡 Visualizza: Il metano è come una piramide a 4 facce con il carbonio al centro, l'etene è "schiacciato" su un piano!

Etino (C₂H₂): I carboni sono ibridati sp con geometria lineare. Il legame triplo è formato da 1 sigma + 2 pi greco. La molecola è rigida - non c'è rotazione possibile intorno al legame triplo.
Gli idrocarburi sono i nostri combustibili fossili: petrolio (da organismi marini), carbone (da antiche foreste) e gas naturali. Sono tutti residui di materia organica fossilizzata nel tempo.
Il petrolio ("olio di roccia") si forma in condizioni particolari che richiedono tre tipi di rocce: la roccia madre (ricca di materia organica), la roccia serbatoio (porosa) e la roccia impermeabile (che impedisce la fuoriuscita).
La formazione del petrolio inizia con la deposizione di sedimenti ricchi di organismi morti sul fondale marino. Nel tempo, pressione e temperatura trasformano questa materia organica in idrocarburi.
💡 Connessione ambientale: Capire l'origine fossile di questi composti ti aiuta a comprendere perché sono risorse limitate e inquinanti!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
Sara Negossi
@saranegossi
Bene, oggi esploriamo il mondo affascinante della chimica organica- quella branca che studia tutti i composti che costituiscono gli esseri viventi! È incredibile pensare che il 98% di tutti i composti chimici conosciuti sono organici, e tutti hanno una... Mostra di più

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Perché dovresti interessarti alla chimica organica? Semplice: tutto quello che ti circonda - dalla plastica del tuo smartphone ai carburanti che muovono le auto - è fatto di composti organici!
I composti organici hanno quattro caratteristiche fondamentali: contengono sempre carbonio, sono incredibilmente complessi, esistono in infinite varietà e sono ottimi combustibili. Ecco perché benzina, carbone e gas naturale bruciano così bene - sono tutti miscele di composti organici.
Gli elementi più importanti in chimica organica si chiamano CHNOPS: carbonio, idrogeno, azoto, ossigeno, fosforo e zolfo. Nonostante non siano gli elementi più abbondanti sulla Terra, sono alla base di tutta la vita.
💡 Curiosità: La chimica organica è anche chiamata "chimica del carbonio" perché tutti i composti organici hanno forti legami carbonio-carbonio come struttura portante!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Per capire come si comporta il carbonio, devi prima conoscere gli orbitali - quelle regioni dello spazio dove hai il 95% di probabilità di trovare un elettrone. Non sono orbite fisse, ma volumi con forme diverse!
I quattro numeri quantici descrivono completamente ogni elettrone:
La configurazione elettronica ti dice come sono distribuiti gli elettroni nei vari livelli. Per esempio, lo zolfo (16 elettroni) ha configurazione: 1s² 2s² 2p⁶ 3s² 3p⁴.
💡 Ricorda: La regola dell'ottetto dice che gli atomi sono stabili quando hanno 8 elettroni nel livello più esterno - per questo si legano tra loro!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Il riempimento degli orbitali segue un ordine preciso: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s... Sembra complicato? C'è uno schema visivo che ti aiuta a ricordarlo!
La regola dell'ottetto è il principio fondamentale: ogni atomo vuole avere 8 elettroni nel livello più esterno per essere stabile (come i gas nobili). Per raggiungerlo, gli atomi possono cedere, acquistare o condividere elettroni.
Gli atomi si legano quando l'energia del sistema unito è minore di quella degli atomi separati. È come dire che "l'unione fa la forza" anche nel mondo atomico!
I legami chimici dipendono dagli elettroni di valenza (quelli nel livello più esterno). Gli elementi dei primi gruppi hanno orbitali "quasi vuoti", quelli degli ultimi gruppi li hanno "quasi pieni".
💡 Tip per l'esame: Memorizza che il primo livello può contenere al massimo 2 elettroni - per questo si parla di "regola dell'ottetto-duetto"!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La differenza di elettronegatività (ΔEn) tra due atomi determina che tipo di legame si formerà. È come un "tira e molla" per gli elettroni!
Legame covalente puro : gli elettroni sono condivisi equamente, come in O₂ o tra atomi identici.
Legame covalente polare (0,4 < ΔEn < 1,7): gli elettroni "preferiscono" stare vicino all'atomo più elettronegativo. L'acqua è l'esempio perfetto!
Legame ionico (ΔEn > 1,7): l'elettrone si trasferisce completamente dall'atomo meno elettronegativo a quello più elettronegativo. Si formano ioni con cariche opposte che si attraggono.
Nel legame ionico hai cationi (positivi, hanno perso elettroni) e anioni (negativi, hanno guadagnato elettroni). Questi si organizzano in reticoli cristallini tridimensionali - non sono molecole!
💡 Memoria visiva: Pensa al sale da cucina (NaCl) - è il classico esempio di legame ionico che forma cristalli!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
I legami covalenti possono essere singoli, doppi o tripli. Il primo legame è sempre sigma (sovrapposizione frontale), i successivi sono pi greco (sovrapposizione laterale).
Nel legame covalente eteropolare, gli elettroni si posizionano più vicino all'atomo più elettronegativo, creando cariche parziali . La molecola diventa un dipolo - elettricamente neutra ma con separazione di cariche.
Il legame metallico è speciale: gli elettroni di valenza sono "delocalizzati" e si muovono liberamente intorno a tutti i cationi del metallo. È come un mare di elettroni che tiene insieme il reticolo!
Questa struttura spiega le proprietà dei metalli: conducono elettricità (elettroni mobili), sono duttili e malleabili (i cationi possono scivolare senza rompere i legami).
💡 Connessione pratica: I fili elettrici sono di rame proprio per la delocalizzazione elettronica del legame metallico!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Ora arriviamo al protagonista: il carbonio! Ha configurazione elettronica 1s² 2s² 2p², quindi dovrebbe formare solo 2 legami... invece ne forma sempre 4. Come mai?
La risposta è l'ibridazione - il carbonio "adatta" i suoi orbitali per formare legami più stabili ed efficienti. Nello stato eccitato, un elettrone passa dall'orbitale 2s al 2p vuoto, creando 4 elettroni spaiati.
Gli orbitali ibridi si formano mescolando orbitali diversi (s, p) dello stesso atomo. Questo processo costa un po' di energia, ma il guadagno energetico dai legami formati è molto maggiore!
Il carbonio può formare catene lunghissime con se stesso grazie ai legami covalenti omopolari molto stabili. Può creare strutture lineari, ramificate o ad anello - sempre mantenendo 4 legami intorno a sé.
💡 Esempio pratico: Pensa ai diamanti - sono reticoli tridimensionali di carbonio dove ogni atomo è legato tetraedricamente ad altri 4 atomi di carbonio!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
L'ibridazione avviene quando gli atomi sono in stato eccitato e la loro configurazione elettronica cambia temporaneamente. Un elettrone di coppia può spostarsi in un orbitale vuoto di energia leggermente superiore.
Prendiamo il berillio come esempio: normalmente ha configurazione 2s², ma nello stato eccitato diventa 2s¹ 2p¹. I due orbitali con singoletti si mescolano formando due orbitali ibridi identici.
Nel carbonio, la configurazione passa da 2s² 2p² a 2s¹ 2p³, creando 4 elettroni spaiati pronti a formare legami. Questi si possono ibridare in modi diversi secondo le necessità della molecola.
L'ibridazione permette di formare più legami covalenti e rende le molecole più stabili. È come se l'atomo si "riarrangiasse" per ottenere la configurazione più vantaggiosa.
💡 Concetto chiave: L'ibridazione spiega perché il carbonio, pur avendo solo 2 elettroni spaiati nella configurazione base, può sempre formare 4 legami!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Ibridazione sp³: L'orbitale 2s si mescola con tutti e 3 gli orbitali 2p, formando 4 orbitali ibridi identici. Geometria tetraedrica con angoli di 109,5°. Esempio: metano (CH₄).
Ibridazione sp²: L'orbitale 2s si mescola con 2 orbitali 2p, lasciandone uno libero. Si formano 3 orbitali ibridi su un piano (120° tra loro) + 1 orbitale p perpendicolare. Geometria planare triangolare.
Ibridazione sp: L'orbitale 2s si mescola con 1 solo orbitale 2p. Si formano 2 orbitali ibridi opposti (180°) + 2 orbitali p perpendicolari. Geometria lineare.
Ogni tipo di ibridazione ha caratteristiche diverse: sp³ ha carattere s per 1/4 e p per 3/4, sp² ha carattere s per 1/3 e p per 2/3, sp ha carattere s e p al 50%.
💡 Trucco per ricordare: sp³ = 4 legami/tetraedro, sp² = 3 ibridi + 1 doppio legame/piano, sp = 2 ibridi + 2 legami multipli/lineare!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Metano (CH₄): Il carbonio è ibridato sp³, formando una struttura tetraedrica perfetta. I 4 orbitali ibridi si sovrappongono agli orbitali 1s degli idrogeni, creando 4 legami sigma identici con angoli di 109,5°.
Etene (C₂H₄): Ogni carbonio è ibridato sp², creando una molecola planare. Tra i due carboni si forma un legame doppio: un sigma (forte) più un pi greco (più debole). Gli angoli sono di 120°.
Il legame sigma si forma sempre per primo dalla sovrapposizione frontale degli orbitali. I legami pi greco derivano dalla sovrapposizione laterale e sono più deboli.
Nel doppio legame C=C dell'etene, la rotazione è impedita dal legame pi greco. Questo crea la possibilità di isomeria geometrica - molecole con stessa formula ma disposizione spaziale diversa.
💡 Visualizza: Il metano è come una piramide a 4 facce con il carbonio al centro, l'etene è "schiacciato" su un piano!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Etino (C₂H₂): I carboni sono ibridati sp con geometria lineare. Il legame triplo è formato da 1 sigma + 2 pi greco. La molecola è rigida - non c'è rotazione possibile intorno al legame triplo.
Gli idrocarburi sono i nostri combustibili fossili: petrolio (da organismi marini), carbone (da antiche foreste) e gas naturali. Sono tutti residui di materia organica fossilizzata nel tempo.
Il petrolio ("olio di roccia") si forma in condizioni particolari che richiedono tre tipi di rocce: la roccia madre (ricca di materia organica), la roccia serbatoio (porosa) e la roccia impermeabile (che impedisce la fuoriuscita).
La formazione del petrolio inizia con la deposizione di sedimenti ricchi di organismi morti sul fondale marino. Nel tempo, pressione e temperatura trasformano questa materia organica in idrocarburi.
💡 Connessione ambientale: Capire l'origine fossile di questi composti ti aiuta a comprendere perché sono risorse limitate e inquinanti!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
6
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS