La chimica organica è il mondo affascinante dei composti del... Mostra di più
La Chimica del Carbonio: Isomerie e Applicazioni




La Chimica del Carbonio
Hai mai pensato a cosa rende il carbonio così speciale? È letteralmente l'elemento della vita! Il carbonio forma il 94% di tutti i composti conosciuti grazie alla sua capacità unica di legarsi con se stesso e altri elementi.
La sua forza sta nei quattro elettroni di valenza che gli permettono di creare quattro legami covalenti. Può legarsi con idrogeno, ossigeno, azoto e molti altri elementi (eteroelementi), formando catene lineari, ramificate o addirittura strutture cilindriche.
L'ibridizzazione è il trucco che il carbonio usa per massimizzare i suoi legami. Invece di usare solo due elettroni spaiati, "promuove" un elettrone e mescola i suoi orbitali per crearne di nuovi. È come riorganizzare una stanza per far entrare più persone - l'energia spesa vale la pena per i risultati ottenuti!
💡 Ricorda: L'ibridizzazione spiega perché il carbonio può formare quattro legami equivalenti invece di solo due.
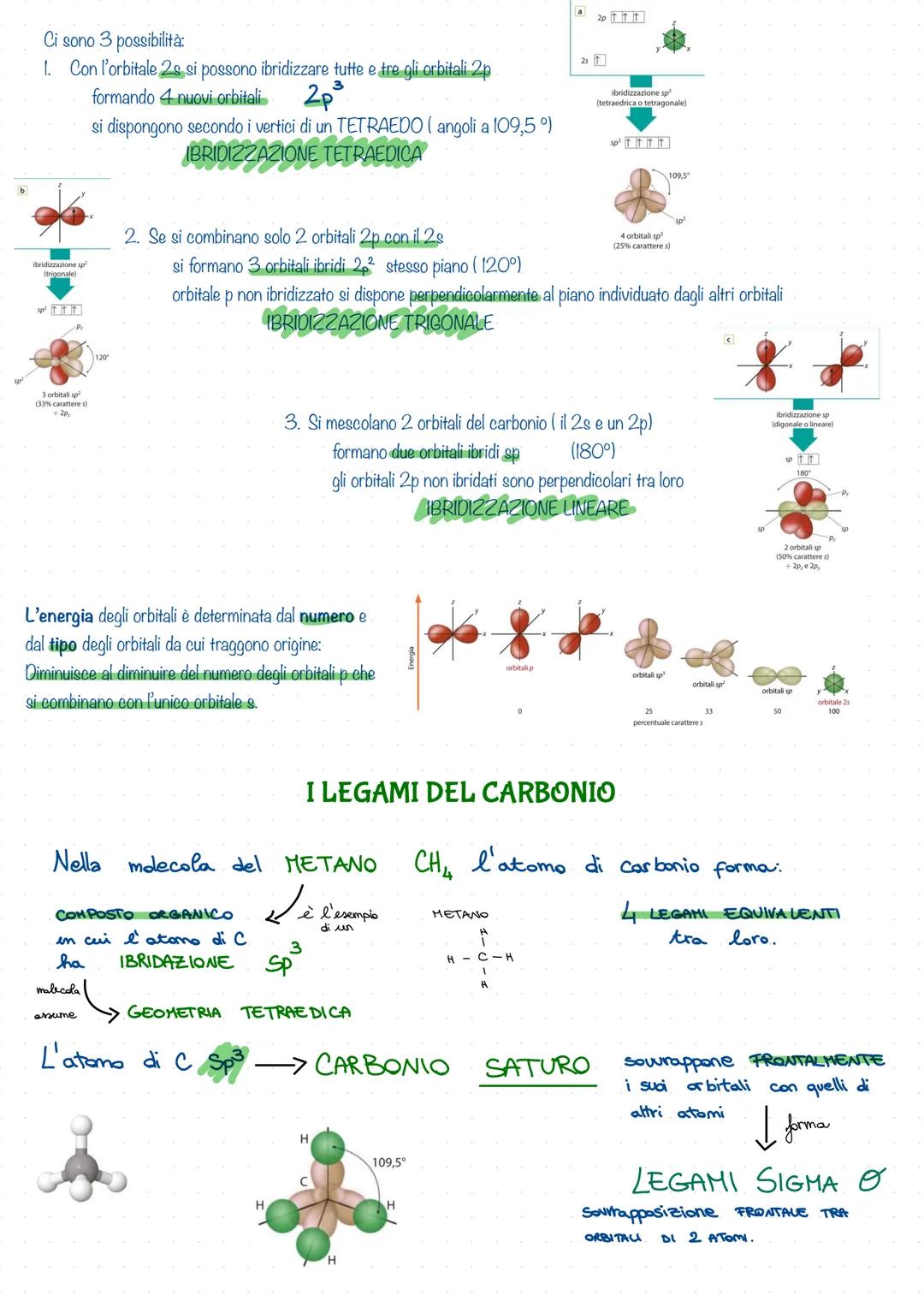
Tipi di Ibridizzazione
Il carbonio ha tre "personalità" diverse a seconda di come organizza i suoi orbitali. Pensala come tre modi diversi di vestirsi per occasioni diverse!
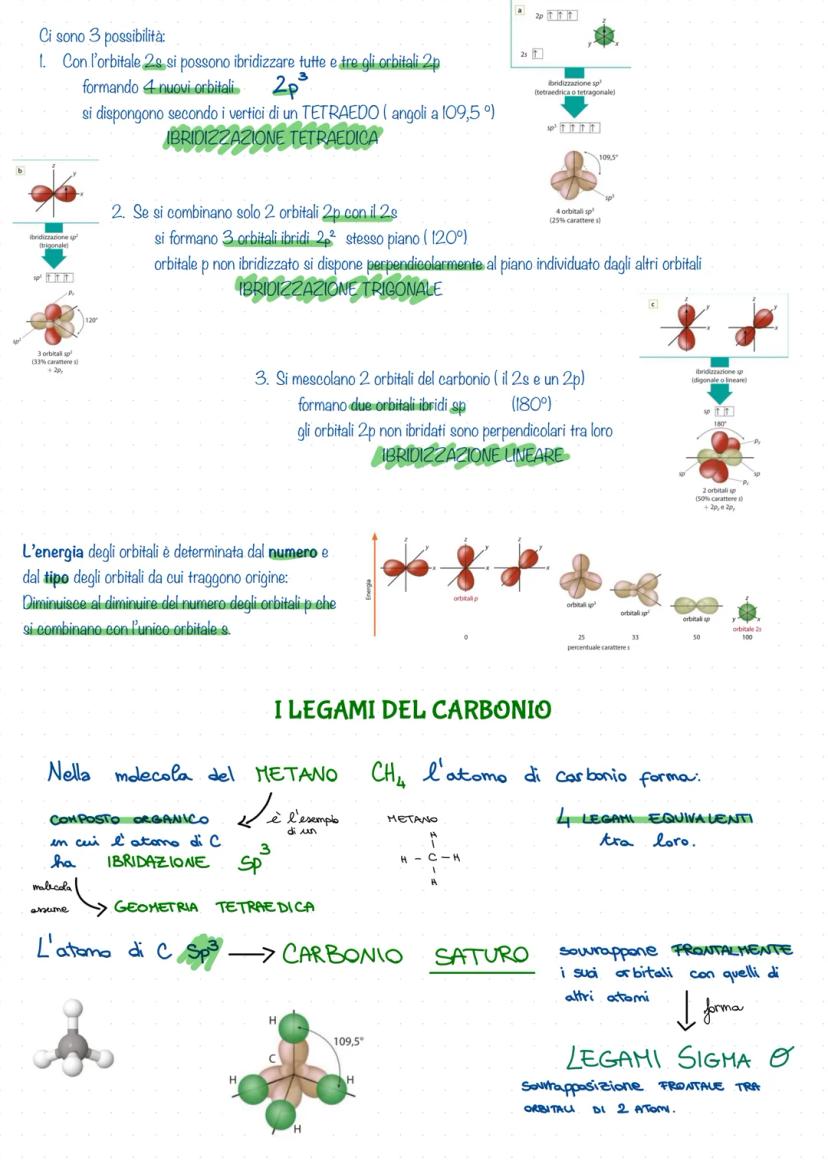
Ibridizzazione tetraedrica (sp³): Tutti e quattro gli orbitali si dispongono ai vertici di un tetraedro con angoli di 109,5°. È il caso del metano (CH₄).
Ibridizzazione trigonale (sp²): Tre orbitali si dispongono su un piano a 120°, mentre uno rimane perpendicolare. Questo permette la formazione di doppi legami.
Ibridizzazione lineare (sp): Solo due orbitali si allineano a 180°, lasciando due orbitali p perpendicolari. Qui nascono i tripli legami.
💡 Trucco per ricordare: Meno orbitali p si combinano, più energia hanno gli orbitali risultanti!

Legami Sigma e Pi Greco
Ora parliamo dei "mattoni" delle molecole organiche: i legami sigma (σ) e pi greco (π). Nel metano hai quattro legami sigma identici - è il carbonio saturo al massimo delle sue capacità.
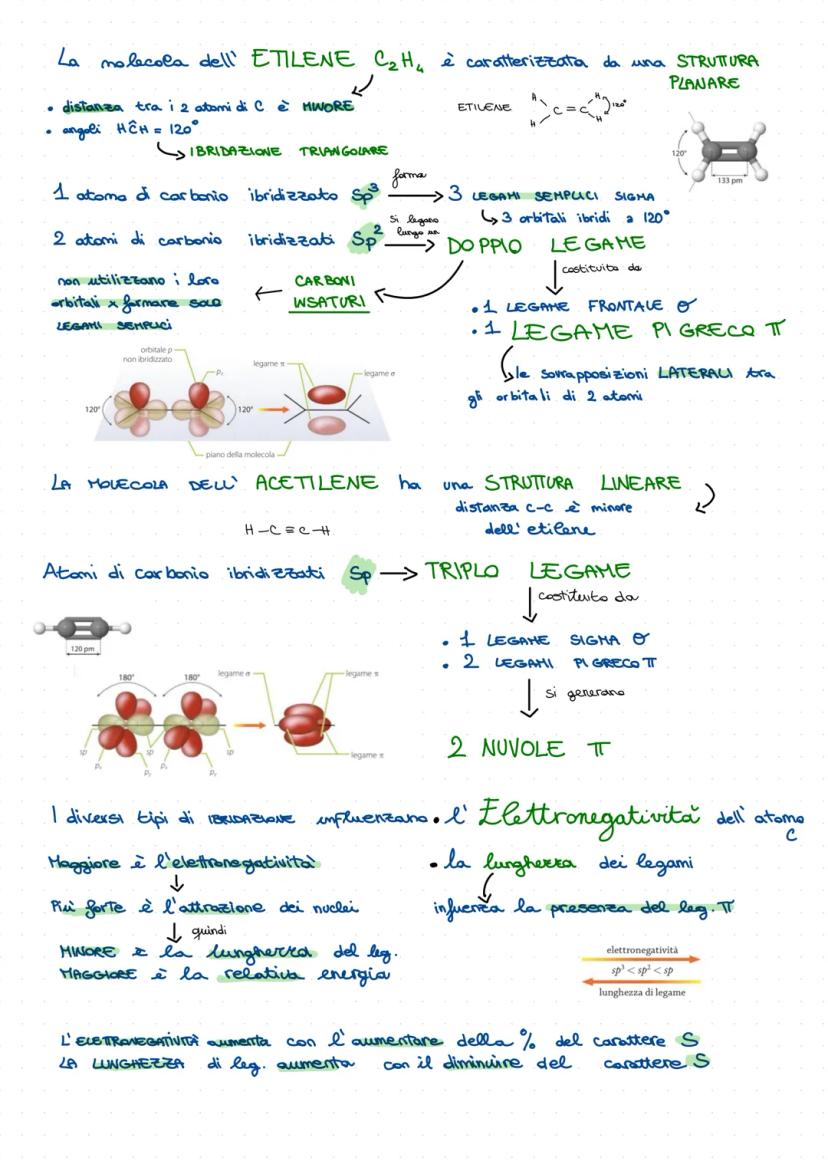
L'etilene (C₂H₄) è diverso: ha una struttura planare con angoli di 120°. Il doppio legame C=C è formato da un legame sigma (sovrapposizione frontale) e un legame pi greco (sovrapposizione laterale). Questi sono carboni insaturi.
L'acetilene è ancora più estremo con la sua struttura lineare. Il triplo legame contiene un sigma e due pi greco. Più legami ci sono, più corta è la distanza tra gli atomi!
Elettronegatività crescente: sp³ < sp² < sp. Più carattere "s" significa elettroni più vicini al nucleo e legami più corti ma più forti.
💡 Nota bene: I legami pi greco sono sempre più deboli dei sigma - ecco perché le reazioni spesso avvengono sui doppi legami!
L'Isomeria: Stessa Formula, Proprietà Diverse
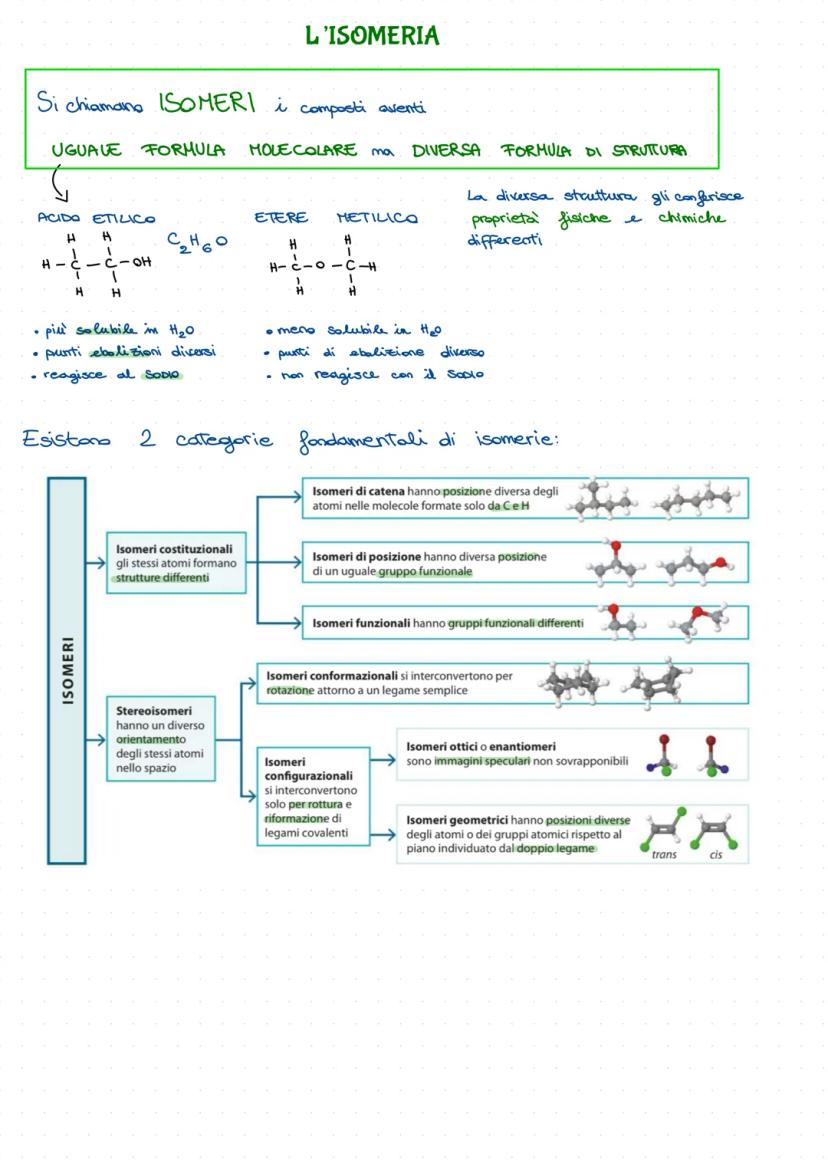
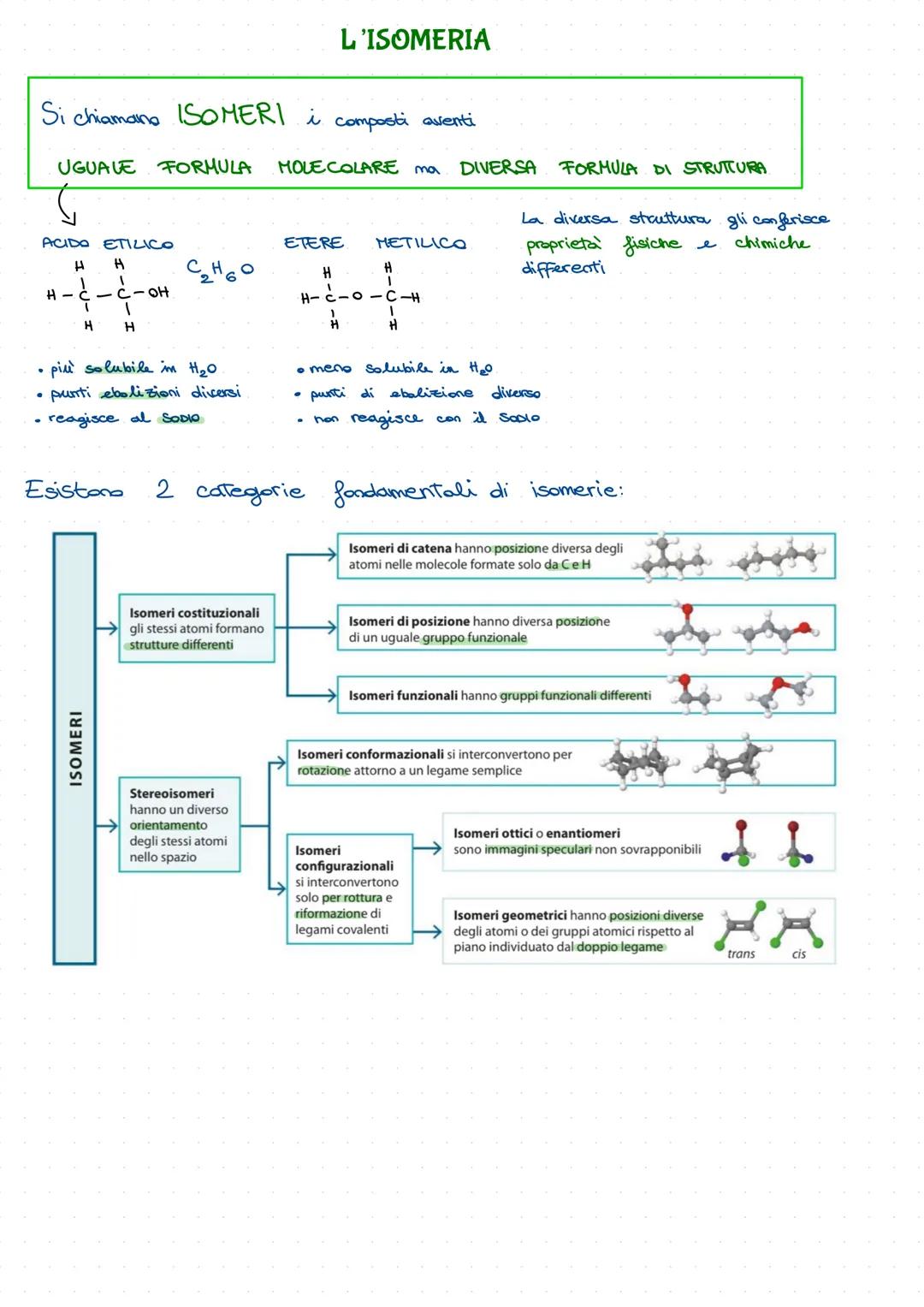
Immagina di avere gli stessi ingredienti ma di cucinare piatti completamente diversi - questo è il mondo dell'isomeria! Composti con la stessa formula molecolare ma strutture diverse hanno proprietà fisiche e chimiche completamente differenti.
L'acido etilico e l'etere metilico (entrambi C₂H₆O) sono l'esempio perfetto: uno reagisce con il sodio, l'altro no; uno è più solubile in acqua, l'altro meno.
Gli isomeri costituzionali hanno strutture diverse: di catena (ramificata vs lineare), di posizione (gruppo funzionale in posti diversi) o funzionali (gruppi funzionali diversi).
Gli stereoisomeri hanno la stessa connettività ma orientamenti diversi nello spazio. Si dividono in conformazionali (rotazione attorno a legami semplici) e configurazionali (serve rompere legami per interconvertirli).
💡 Pensaci così: È come avere la stessa casa ma arredata in modi completamente diversi!
Isomeri Costituzionali e Conformazionali
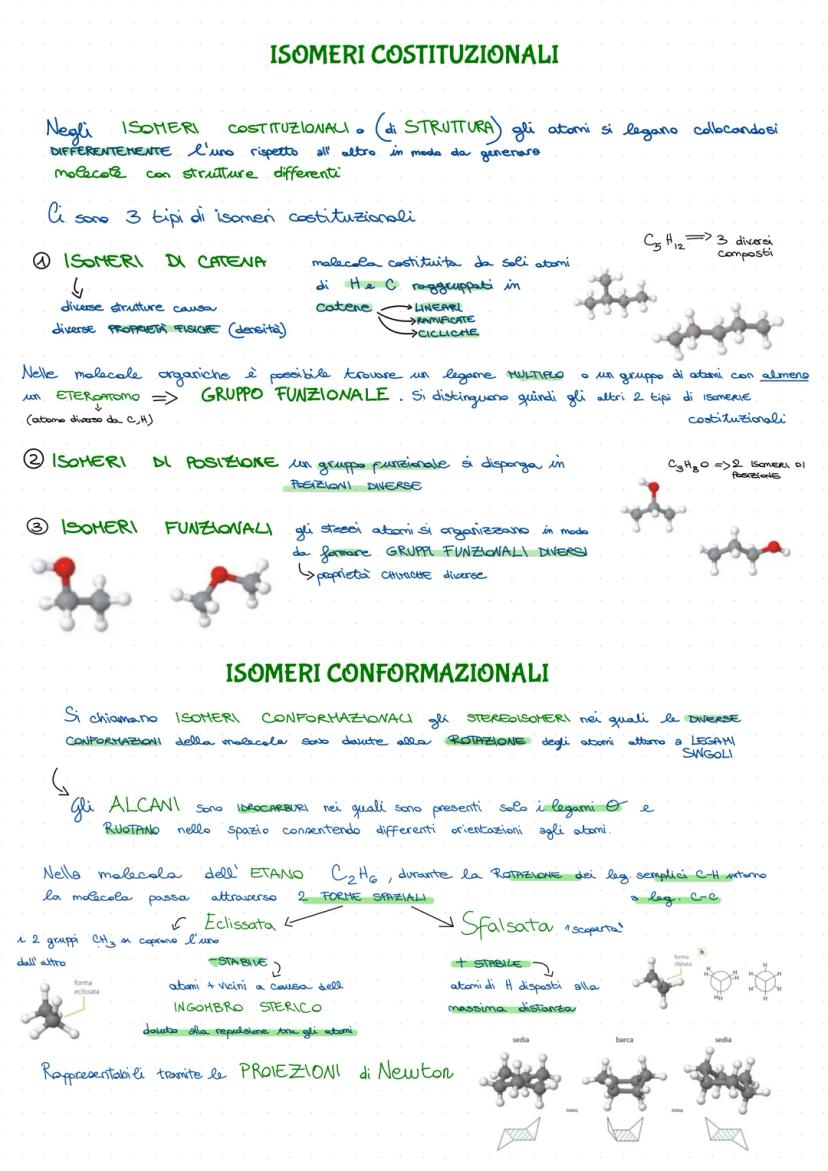
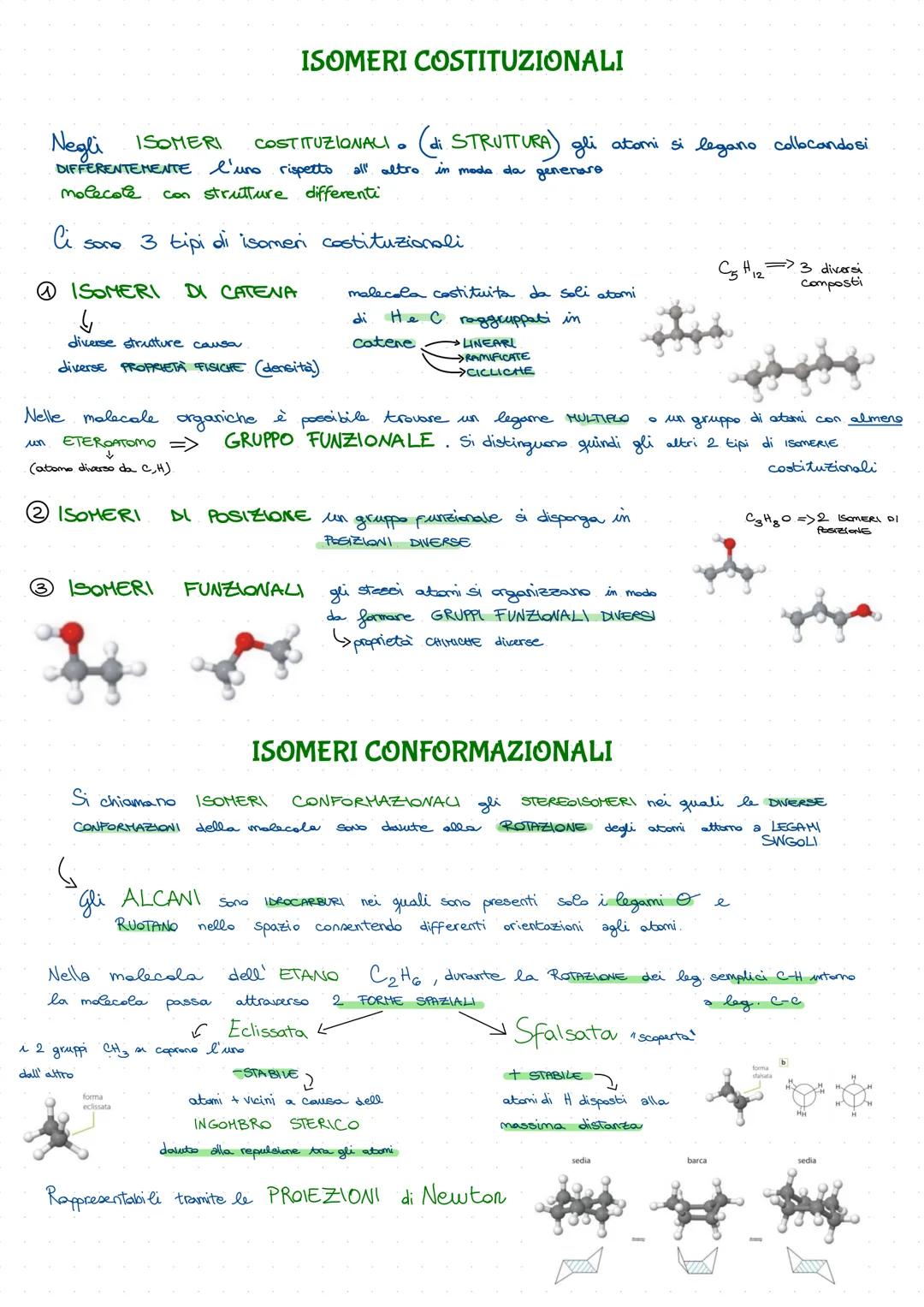
Gli isomeri costituzionali sono come fratelli con personalità diverse. Il C₅H₁₂ può formare tre composti diversi: lineare, ramificato o ciclico. Stessi atomi, proprietà fisiche completamente diverse!
Gli isomeri di posizione spostano i gruppi funzionali come pezzi su una scacchiera, mentre gli isomeri funzionali cambiano completamente il gruppo funzionale - proprietà chimiche totalmente diverse.
Gli isomeri conformazionali sono più dinamici: gli alcani possono ruotare attorno ai legami sigma, creando diverse conformazioni. Nell'etano (C₂H₆) passi dalla forma eclissata (meno stabile, atomi più vicini) alla sfalsata (più stabile, atomi alla massima distanza).
L'ingombro sterico è il "fastidio" che provano gli atomi quando sono troppo vicini - per questo la conformazione sfalsata è preferita.
💡 Ricorda: I conformeri si interconvertono facilmente per rotazione, non serve rompere legami!

Isomeri Geometrici e Regole CIP
Gli isomeri geometrici sono bloccati nella loro posizione dai doppi legami o dalle strutture cicliche - niente rotazione libera qui! Sono come gemelli che si assomigliano ma non sono identici.
I prefissi cis (stesso lato) e trans (lati opposti) funzionano bene per strutture semplici. Ma quando hai tre o più sostituenti diversi, servono le regole CIP - un sistema di priorità basato sul numero atomico.
La regola è semplice: numero atomico più alto = priorità più alta. Se due atomi sono uguali, continui nella catena fino a trovare la differenza. Per i legami multipli, li conti come legami singoli multipli.
Alla fine usi Z quando i gruppi a priorità più alta sono dallo stesso lato, ed E quando sono su lati opposti.
💡 Trucco mnemonico: Z come "Zame parte", E come "Estremi opposti"!
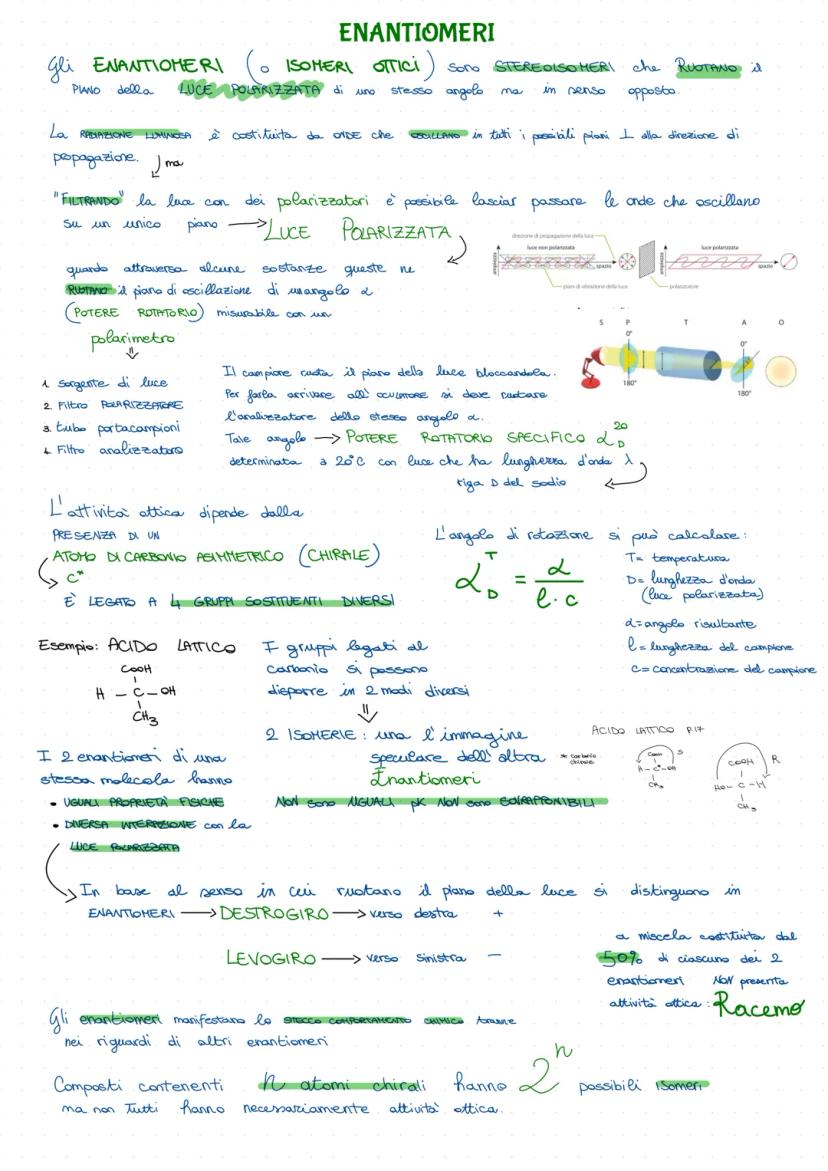
Enantiomeri e Attività Ottica
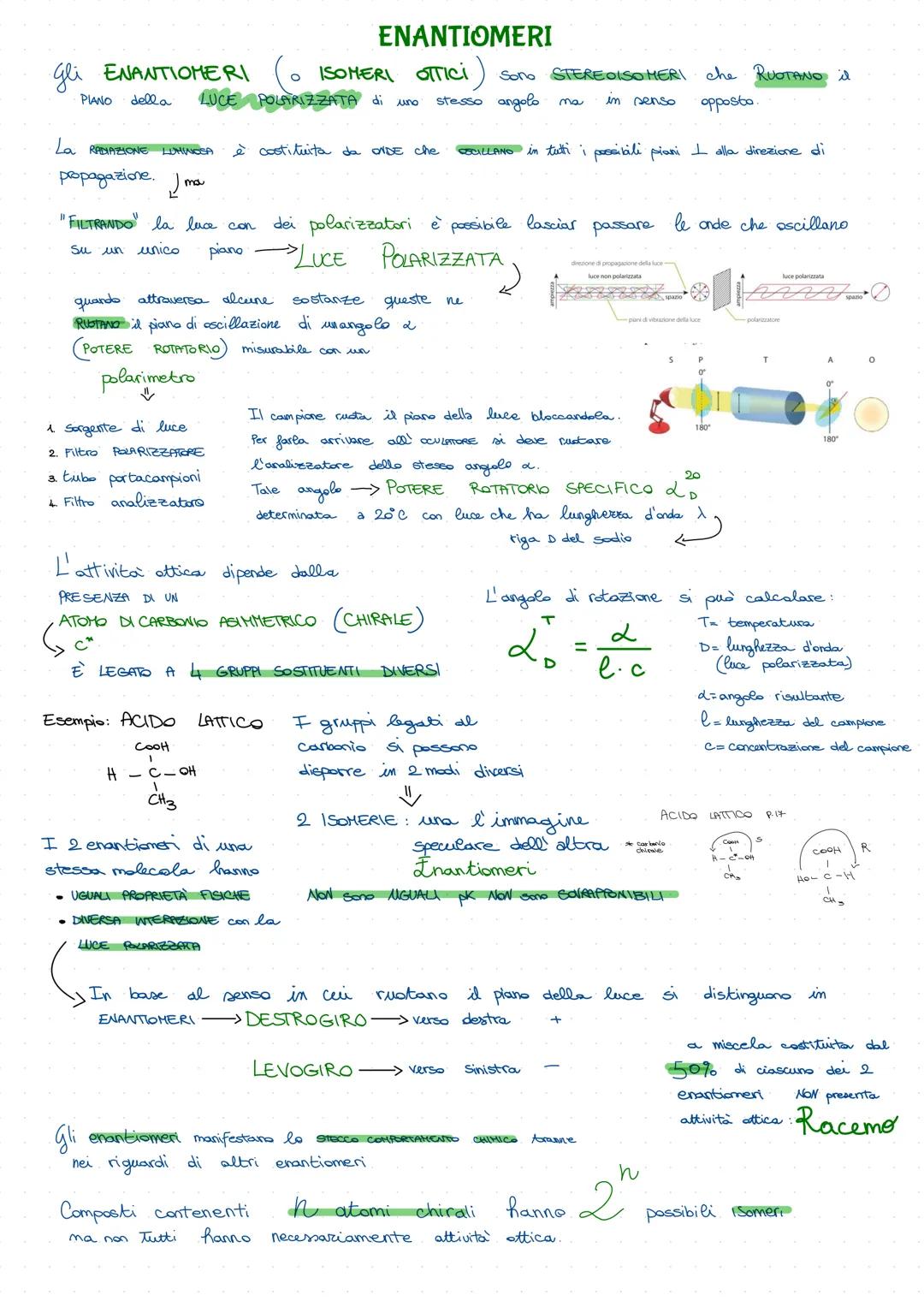
Gli enantiomeri sono come le tue mani: immagini speculari che non puoi sovrapporre! La chiave è il carbonio asimmetrico legato a quattro gruppi diversi.
Questi composti hanno una proprietà magica: ruotano la luce polarizzata. Un polarimetro misura questo potere rotatorio - destrogiro (+) ruota a destra, levogiro (-) a sinistra.
L'acido lattico è l'esempio perfetto: stesso atomo di carbonio, quattro sostituenti diversi (COOH, H, OH, CH₃), ma due disposizioni spaziali diverse. Proprietà fisiche identiche, ma interazione opposta con la luce!
Il racemo è una miscela 50:50 dei due enantiomeri - si annullano a vicenda e non mostrano attività ottica. È come avere due persone che camminano in direzioni opposte con la stessa velocità.
💡 Importante: Con n carboni chirali hai 2ⁿ possibili stereoisomeri!
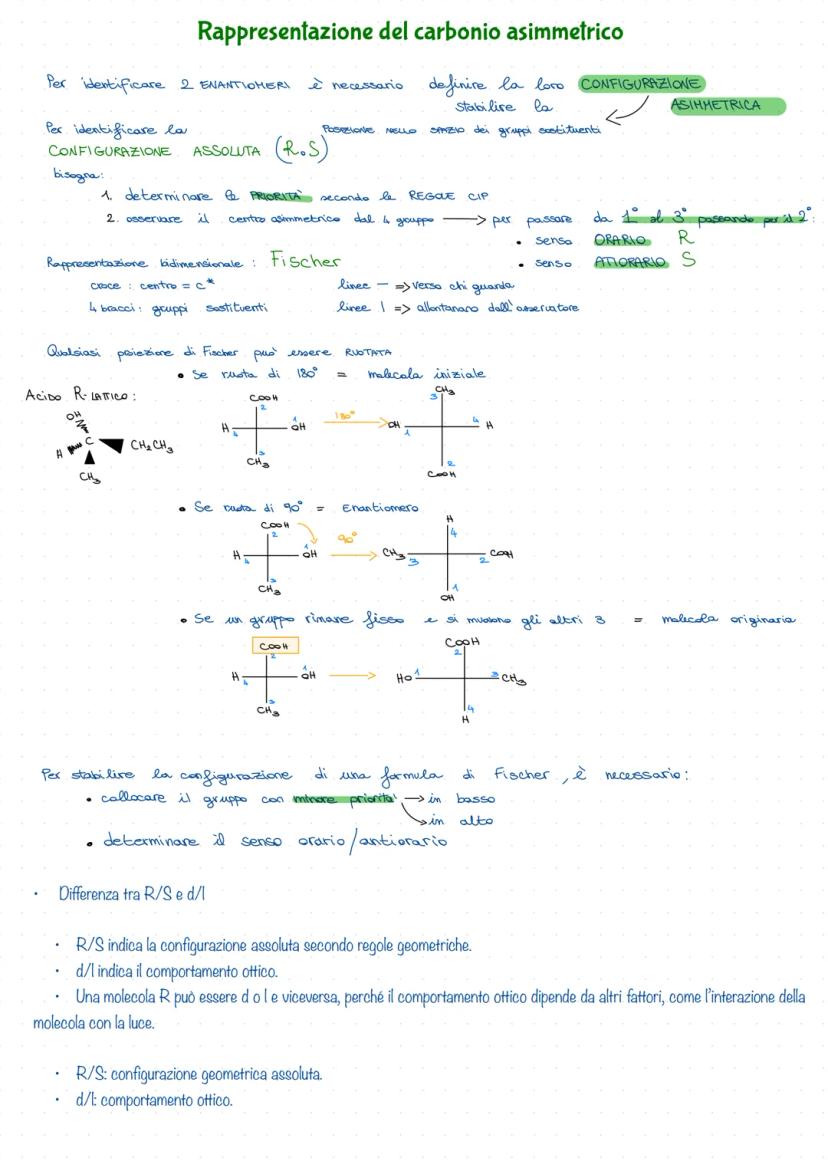
Configurazione R/S e Proiezioni di Fischer
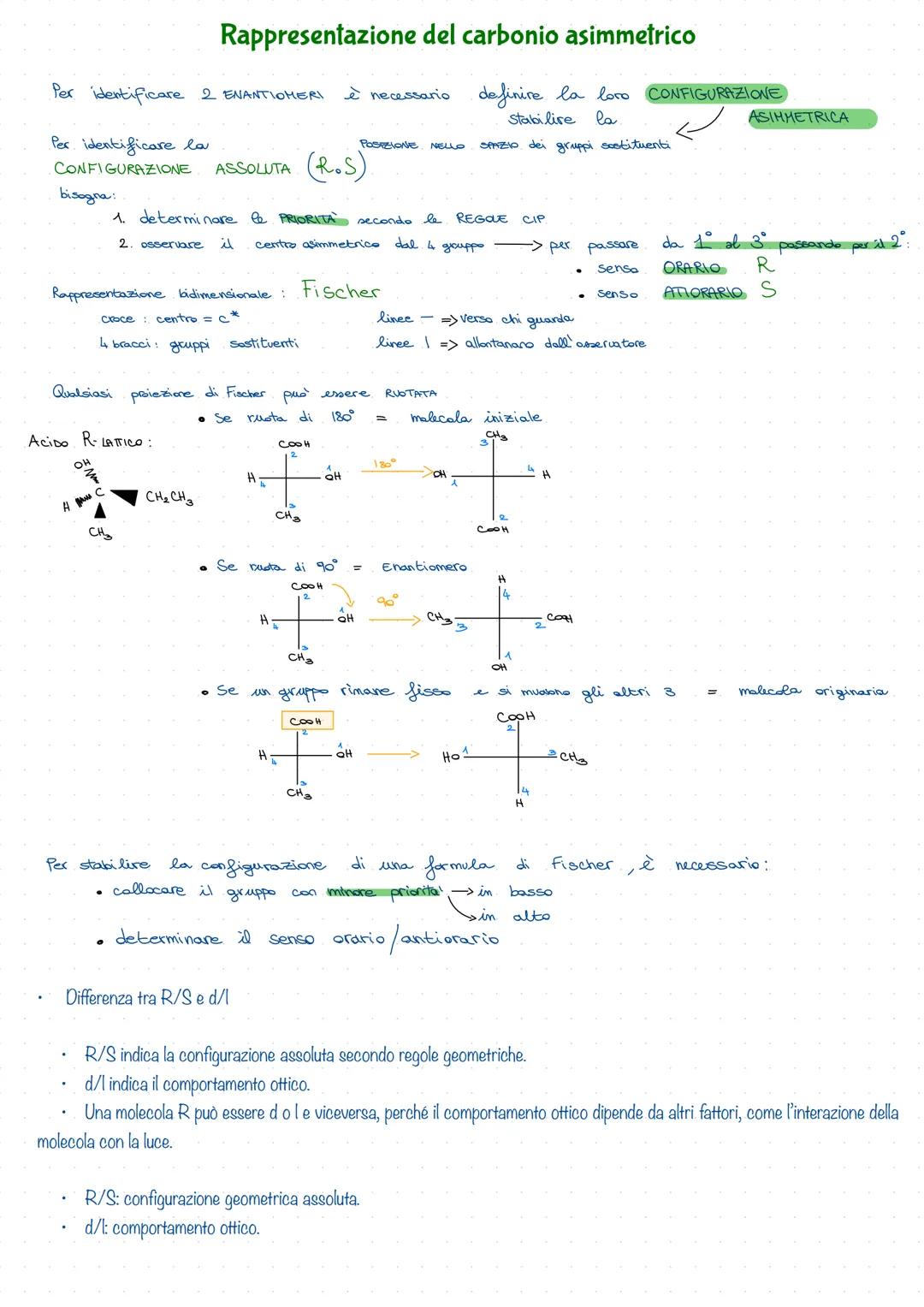
Per distinguere gli enantiomeri usi la configurazione assoluta R/S. Prima ordini i sostituenti secondo le regole CIP, poi guardi dal gruppo a priorità più bassa: senso orario = R, senso antiorario = S.
Le proiezioni di Fischer sono il tuo strumento per rappresentare i carboni chirali in 2D. La croce rappresenta il carbonio, le linee orizzontali vengono verso di te, quelle verticali si allontanano.
Attenzione alle rotazioni! Puoi ruotare di 180° e rimani con la stessa molecola, ma a 90° ottieni l'enantiomero. Se fissi un gruppo e muovi gli altri tre in senso orario, torni alla molecola originale.
R/S vs d/l: R e S descrivono la geometria assoluta, mentre d e l descrivono il comportamento ottico. Non sempre coincidono - una molecola R può essere destrogira o levogira!
💡 Ricorda: R/S = configurazione geometrica, d/l = comportamento con la luce!

Effetto Induttivo
I legami nelle molecole organiche non sono tutti uguali - alcuni sono più polari di altri! L'effetto induttivo spiega come un atomo o gruppo influenza la distribuzione elettronica nei legami vicini.
Effetto +I: Gruppi meno elettronegativi del carbonio (come metalli o gruppi alchilici) cedono elettroni e aumentano la densità elettronica sul carbonio. I gruppi alchilici seguono l'ordine: -CH₃ < -CH₂CH₃ < -CH(CH₃)₂ < -C(CH₃)₃.
Effetto -I: Gruppi più elettronegativi attraggono elettroni verso di sé, impoverendo il carbonio. Anche i carboni ibridizzati sp² e sp sono più elettronegativi del sp³.
L'effetto si propaga lungo la catena ma diminuisce con la distanza - è come l'eco di un suono che si affievolisce.
💡 Trucco: Pensa all'elettronegatività come a una "fame di elettroni" - chi ne ha più fame, li attira di più!
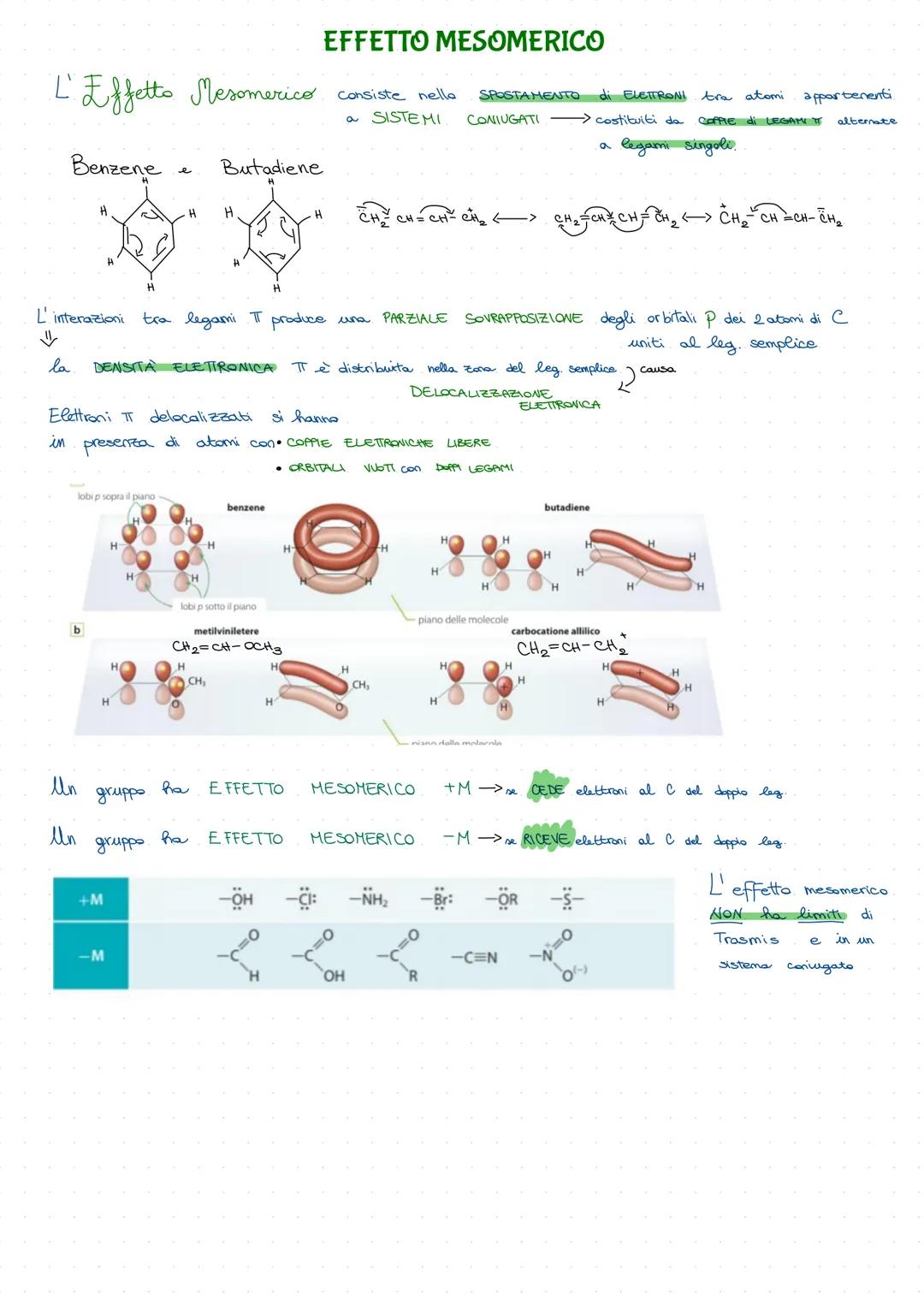
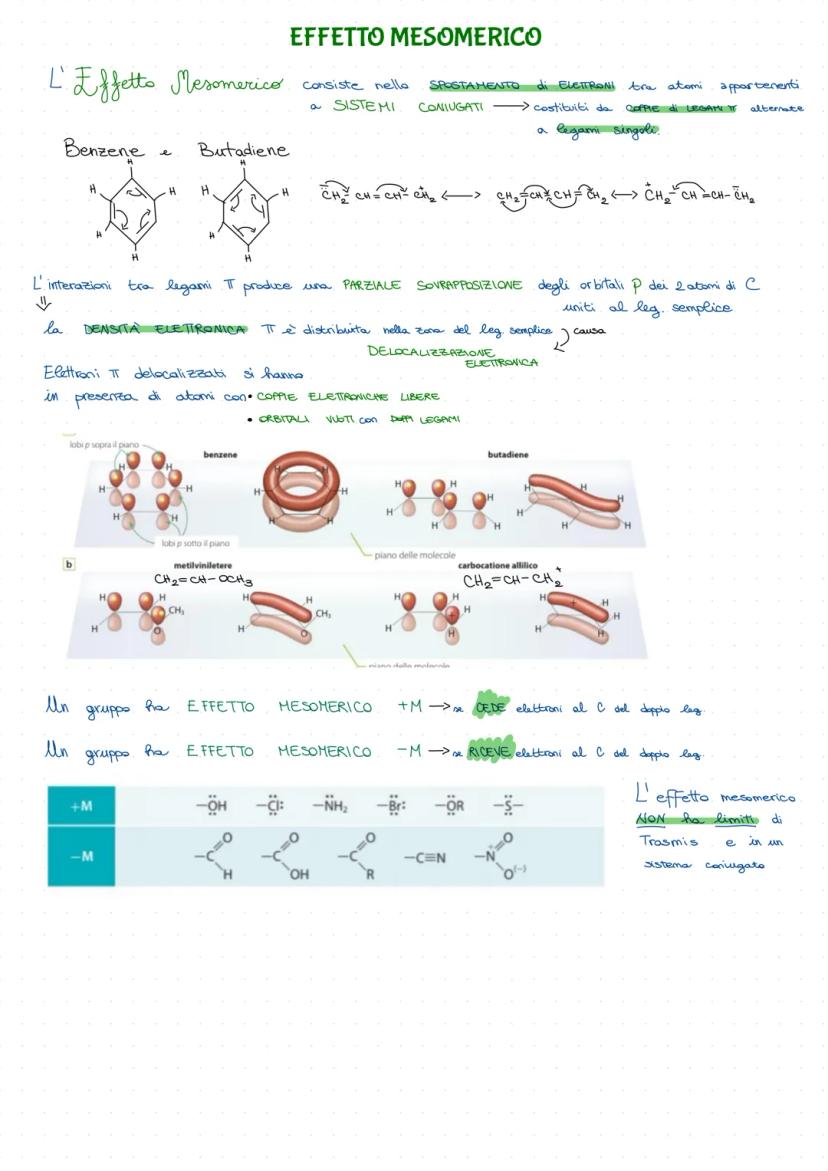
Effetto Mesomerico
L'effetto mesomerico è la delocalizzazione elettronica nei sistemi coniugati - catene con doppi legami alternati a legami semplici. È come una danza di elettroni che si muovono liberamente!
Nel butadiene gli elettroni π non restano fermi sui doppi legami ma si "spalmano" su tutta la molecola. Gli orbitali p si sovrappongono parzialmente, creando una nuvola elettronica delocalizzata.
Effetto +M: Gruppi come -OH, -OR, -NH₂ cedono elettroni al sistema π. Hanno coppie elettroniche libere che entrano nella danza.
Effetto -M: Gruppi come -C=O, -NO₂, -C≡N ricevono elettroni dal sistema π. Hanno orbitali vuoti che accettano la densità elettronica.
A differenza dell'effetto induttivo, quello mesomerico non ha limiti di trasmissione in un sistema coniugato - gli elettroni viaggiano per tutta la molecola!
💡 Visualizza: È come un'autostrada elettronica dove gli elettroni possono viaggiare liberamente!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: anidride carbonica (CO2)
8Trasformazioni chimiche
Trasformazioni chimiche legge dalton leggi ponderali
Ripasso Apparato Cardiocircolatorio
Ripasso (Cuore e Sangue inclusi)
Chimica organica, idrocarburi e composti aromatici
Idrocarburi: definizione, alcani/eni/ini, nomenclatura, formule, isomeri, proprietà fisiche, reazioni chimiche. Ibridazione Composti aromatici: definizione, reazioni chimiche, Benzene
Schemi di Chimica Organica
Definizione di Chimica Organica, Carbonio, Ibridazione, Saturazione ed Insaturazione, Alcani, Alcheni, Alchini, Cicloalcani, isomeria, nomenclatura, stereoisomeria geometrica ed ottica, formula bruta, formule condensate e struttura di Lewis
il cuore
appunti sul cuore
Leggi Ponderali
Legge Ponderali=Legge di Lavoisier,di Proust(o delle proporzioni definite)e di Dalton(o delle proporzio ni multiple),Enunciato della Legge di Dalton.
ANATOMIA apparato cardiovascolare, il cuore, vasi sanguigni, scambi e regolazione del flusso e composizione del sangue.
Top riassunti dell’apparato cardiovascolare,cuore,vasi sanguigni, scambi e regolazione del flusso e composizione del sangue.
I legami tra i ioni e tra gli atomi
I nn legami tra gli ioni e gli atomi (chimica)
Contenuti più popolari di Scienze
9Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Apparato respiratorio
fai un quiz
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Apparato Digerente
Presentazione sull’apparato digerente, con questa presentazione un buono voto è assicurato
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Platone
Riassunto dettagliato su Platone
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
La Chimica del Carbonio: Isomerie e Applicazioni
La chimica organica è il mondo affascinante dei composti del carbonio che ci circondano ogni giorno. Dal carbonio degli idrocarburi fino agli zuccheri che mangi, tutto ruota attorno alla capacità unica di questo elemento di formare catene e strutture complesse.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
La Chimica del Carbonio
Hai mai pensato a cosa rende il carbonio così speciale? È letteralmente l'elemento della vita! Il carbonio forma il 94% di tutti i composti conosciuti grazie alla sua capacità unica di legarsi con se stesso e altri elementi.
La sua forza sta nei quattro elettroni di valenza che gli permettono di creare quattro legami covalenti. Può legarsi con idrogeno, ossigeno, azoto e molti altri elementi (eteroelementi), formando catene lineari, ramificate o addirittura strutture cilindriche.
L'ibridizzazione è il trucco che il carbonio usa per massimizzare i suoi legami. Invece di usare solo due elettroni spaiati, "promuove" un elettrone e mescola i suoi orbitali per crearne di nuovi. È come riorganizzare una stanza per far entrare più persone - l'energia spesa vale la pena per i risultati ottenuti!
💡 Ricorda: L'ibridizzazione spiega perché il carbonio può formare quattro legami equivalenti invece di solo due.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Tipi di Ibridizzazione
Il carbonio ha tre "personalità" diverse a seconda di come organizza i suoi orbitali. Pensala come tre modi diversi di vestirsi per occasioni diverse!
Ibridizzazione tetraedrica (sp³): Tutti e quattro gli orbitali si dispongono ai vertici di un tetraedro con angoli di 109,5°. È il caso del metano (CH₄).
Ibridizzazione trigonale (sp²): Tre orbitali si dispongono su un piano a 120°, mentre uno rimane perpendicolare. Questo permette la formazione di doppi legami.
Ibridizzazione lineare (sp): Solo due orbitali si allineano a 180°, lasciando due orbitali p perpendicolari. Qui nascono i tripli legami.
💡 Trucco per ricordare: Meno orbitali p si combinano, più energia hanno gli orbitali risultanti!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Legami Sigma e Pi Greco
Ora parliamo dei "mattoni" delle molecole organiche: i legami sigma (σ) e pi greco (π). Nel metano hai quattro legami sigma identici - è il carbonio saturo al massimo delle sue capacità.
L'etilene (C₂H₄) è diverso: ha una struttura planare con angoli di 120°. Il doppio legame C=C è formato da un legame sigma (sovrapposizione frontale) e un legame pi greco (sovrapposizione laterale). Questi sono carboni insaturi.
L'acetilene è ancora più estremo con la sua struttura lineare. Il triplo legame contiene un sigma e due pi greco. Più legami ci sono, più corta è la distanza tra gli atomi!
Elettronegatività crescente: sp³ < sp² < sp. Più carattere "s" significa elettroni più vicini al nucleo e legami più corti ma più forti.
💡 Nota bene: I legami pi greco sono sempre più deboli dei sigma - ecco perché le reazioni spesso avvengono sui doppi legami!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
L'Isomeria: Stessa Formula, Proprietà Diverse
Immagina di avere gli stessi ingredienti ma di cucinare piatti completamente diversi - questo è il mondo dell'isomeria! Composti con la stessa formula molecolare ma strutture diverse hanno proprietà fisiche e chimiche completamente differenti.
L'acido etilico e l'etere metilico (entrambi C₂H₆O) sono l'esempio perfetto: uno reagisce con il sodio, l'altro no; uno è più solubile in acqua, l'altro meno.
Gli isomeri costituzionali hanno strutture diverse: di catena (ramificata vs lineare), di posizione (gruppo funzionale in posti diversi) o funzionali (gruppi funzionali diversi).
Gli stereoisomeri hanno la stessa connettività ma orientamenti diversi nello spazio. Si dividono in conformazionali (rotazione attorno a legami semplici) e configurazionali (serve rompere legami per interconvertirli).
💡 Pensaci così: È come avere la stessa casa ma arredata in modi completamente diversi!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Isomeri Costituzionali e Conformazionali
Gli isomeri costituzionali sono come fratelli con personalità diverse. Il C₅H₁₂ può formare tre composti diversi: lineare, ramificato o ciclico. Stessi atomi, proprietà fisiche completamente diverse!
Gli isomeri di posizione spostano i gruppi funzionali come pezzi su una scacchiera, mentre gli isomeri funzionali cambiano completamente il gruppo funzionale - proprietà chimiche totalmente diverse.
Gli isomeri conformazionali sono più dinamici: gli alcani possono ruotare attorno ai legami sigma, creando diverse conformazioni. Nell'etano (C₂H₆) passi dalla forma eclissata (meno stabile, atomi più vicini) alla sfalsata (più stabile, atomi alla massima distanza).
L'ingombro sterico è il "fastidio" che provano gli atomi quando sono troppo vicini - per questo la conformazione sfalsata è preferita.
💡 Ricorda: I conformeri si interconvertono facilmente per rotazione, non serve rompere legami!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Isomeri Geometrici e Regole CIP
Gli isomeri geometrici sono bloccati nella loro posizione dai doppi legami o dalle strutture cicliche - niente rotazione libera qui! Sono come gemelli che si assomigliano ma non sono identici.
I prefissi cis (stesso lato) e trans (lati opposti) funzionano bene per strutture semplici. Ma quando hai tre o più sostituenti diversi, servono le regole CIP - un sistema di priorità basato sul numero atomico.
La regola è semplice: numero atomico più alto = priorità più alta. Se due atomi sono uguali, continui nella catena fino a trovare la differenza. Per i legami multipli, li conti come legami singoli multipli.
Alla fine usi Z quando i gruppi a priorità più alta sono dallo stesso lato, ed E quando sono su lati opposti.
💡 Trucco mnemonico: Z come "Zame parte", E come "Estremi opposti"!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Enantiomeri e Attività Ottica
Gli enantiomeri sono come le tue mani: immagini speculari che non puoi sovrapporre! La chiave è il carbonio asimmetrico legato a quattro gruppi diversi.
Questi composti hanno una proprietà magica: ruotano la luce polarizzata. Un polarimetro misura questo potere rotatorio - destrogiro (+) ruota a destra, levogiro (-) a sinistra.
L'acido lattico è l'esempio perfetto: stesso atomo di carbonio, quattro sostituenti diversi (COOH, H, OH, CH₃), ma due disposizioni spaziali diverse. Proprietà fisiche identiche, ma interazione opposta con la luce!
Il racemo è una miscela 50:50 dei due enantiomeri - si annullano a vicenda e non mostrano attività ottica. È come avere due persone che camminano in direzioni opposte con la stessa velocità.
💡 Importante: Con n carboni chirali hai 2ⁿ possibili stereoisomeri!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Configurazione R/S e Proiezioni di Fischer
Per distinguere gli enantiomeri usi la configurazione assoluta R/S. Prima ordini i sostituenti secondo le regole CIP, poi guardi dal gruppo a priorità più bassa: senso orario = R, senso antiorario = S.
Le proiezioni di Fischer sono il tuo strumento per rappresentare i carboni chirali in 2D. La croce rappresenta il carbonio, le linee orizzontali vengono verso di te, quelle verticali si allontanano.
Attenzione alle rotazioni! Puoi ruotare di 180° e rimani con la stessa molecola, ma a 90° ottieni l'enantiomero. Se fissi un gruppo e muovi gli altri tre in senso orario, torni alla molecola originale.
R/S vs d/l: R e S descrivono la geometria assoluta, mentre d e l descrivono il comportamento ottico. Non sempre coincidono - una molecola R può essere destrogira o levogira!
💡 Ricorda: R/S = configurazione geometrica, d/l = comportamento con la luce!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Effetto Induttivo
I legami nelle molecole organiche non sono tutti uguali - alcuni sono più polari di altri! L'effetto induttivo spiega come un atomo o gruppo influenza la distribuzione elettronica nei legami vicini.
Effetto +I: Gruppi meno elettronegativi del carbonio (come metalli o gruppi alchilici) cedono elettroni e aumentano la densità elettronica sul carbonio. I gruppi alchilici seguono l'ordine: -CH₃ < -CH₂CH₃ < -CH(CH₃)₂ < -C(CH₃)₃.
Effetto -I: Gruppi più elettronegativi attraggono elettroni verso di sé, impoverendo il carbonio. Anche i carboni ibridizzati sp² e sp sono più elettronegativi del sp³.
L'effetto si propaga lungo la catena ma diminuisce con la distanza - è come l'eco di un suono che si affievolisce.
💡 Trucco: Pensa all'elettronegatività come a una "fame di elettroni" - chi ne ha più fame, li attira di più!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Effetto Mesomerico
L'effetto mesomerico è la delocalizzazione elettronica nei sistemi coniugati - catene con doppi legami alternati a legami semplici. È come una danza di elettroni che si muovono liberamente!
Nel butadiene gli elettroni π non restano fermi sui doppi legami ma si "spalmano" su tutta la molecola. Gli orbitali p si sovrappongono parzialmente, creando una nuvola elettronica delocalizzata.
Effetto +M: Gruppi come -OH, -OR, -NH₂ cedono elettroni al sistema π. Hanno coppie elettroniche libere che entrano nella danza.
Effetto -M: Gruppi come -C=O, -NO₂, -C≡N ricevono elettroni dal sistema π. Hanno orbitali vuoti che accettano la densità elettronica.
A differenza dell'effetto induttivo, quello mesomerico non ha limiti di trasmissione in un sistema coniugato - gli elettroni viaggiano per tutta la molecola!
💡 Visualizza: È come un'autostrada elettronica dove gli elettroni possono viaggiare liberamente!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: anidride carbonica (CO2)
8Trasformazioni chimiche
Trasformazioni chimiche legge dalton leggi ponderali
Ripasso Apparato Cardiocircolatorio
Ripasso (Cuore e Sangue inclusi)
Chimica organica, idrocarburi e composti aromatici
Idrocarburi: definizione, alcani/eni/ini, nomenclatura, formule, isomeri, proprietà fisiche, reazioni chimiche. Ibridazione Composti aromatici: definizione, reazioni chimiche, Benzene
Schemi di Chimica Organica
Definizione di Chimica Organica, Carbonio, Ibridazione, Saturazione ed Insaturazione, Alcani, Alcheni, Alchini, Cicloalcani, isomeria, nomenclatura, stereoisomeria geometrica ed ottica, formula bruta, formule condensate e struttura di Lewis
il cuore
appunti sul cuore
Leggi Ponderali
Legge Ponderali=Legge di Lavoisier,di Proust(o delle proporzioni definite)e di Dalton(o delle proporzio ni multiple),Enunciato della Legge di Dalton.
ANATOMIA apparato cardiovascolare, il cuore, vasi sanguigni, scambi e regolazione del flusso e composizione del sangue.
Top riassunti dell’apparato cardiovascolare,cuore,vasi sanguigni, scambi e regolazione del flusso e composizione del sangue.
I legami tra i ioni e tra gli atomi
I nn legami tra gli ioni e gli atomi (chimica)
Contenuti più popolari di Scienze
9Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Apparato respiratorio
fai un quiz
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Apparato Digerente
Presentazione sull’apparato digerente, con questa presentazione un buono voto è assicurato
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Platone
Riassunto dettagliato su Platone
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.