La chimica organica è il mondo affascinante delle molecole che... Mostra di più
Chimica Organica: La Scienza del Carbonio









La Chimica del Carbonio
Pensa a tutto quello che ti circonda: dalla plastica del tuo smartphone alle proteine nei tuoi muscoli. Tutti questi materiali hanno una cosa in comune: contengono carbonio. I composti organici sono semplicemente molecole che hanno carbonio legato ad almeno un atomo di idrogeno.
Non tutti i composti con carbonio sono organici però! La CO₂ che espiri è inorganica perché manca il legame carbonio-idrogeno. Gli elementi che formano composti organici sono principalmente carbonio, idrogeno, ossigeno, azoto, fosforo e zolfo - tutti con raggi atomici piccoli e elettronegatività medio-alta.
Il segreto del carbonio sta nella sua elettronegatività intermedia (2,5) che gli permette di formare legami covalenti poco polari e molto stabili. Quando si lega con altri carboni o con l'idrogeno forma legami praticamente apolari, quindi super stabili. Inoltre ha un'incredibile capacità di concatenazione - può legarsi con altri atomi di carbonio formando catene lunghissime e ramificazioni complesse.
💡 Ricorda: Un legame poco polare è più stabile perché gli elettroni sono condivisi equamente, mentre nei legami polari c'è uno sbilanciamento che rende la molecola meno stabile.

L'Ibridazione del Carbonio
Ecco dove diventa interessante! Nel suo stato fondamentale, il carbonio dovrebbe fare solo 2 legami. Ma fornendo un po' di energia, il doppietto 2s si separa e otteniamo 4 elettroni spaiati che possono formare 4 legami. Questo processo si chiama ibridazione.
Gli orbitali s e p si "mescolano" creando nuovi orbitali ibridi sp³ con forma intermedia tra quella sferica (s) e quella a otto (p). Questi 4 orbitali si dispongono nello spazio con angoli di 109,5° ai vertici di un tetraedro - la disposizione più stabile possibile.
L'ibridazione sp³ crea solo legami sigma (σ) - i più forti e stabili. Questi legami permettono la rotazione attorno all'asse di legame, rendendo le molecole flessibili. I legami sigma si formano per sovrapposizione frontale degli orbitali lungo la linea che unisce i nuclei.
💡 Curiosità: Gli orbitali ibridi sp³ sono isoenergetici - hanno tutti la stessa energia, distribuita equamente tra loro!

Tipi di Ibridazione e Legami
Il carbonio può ibridarsi in tre modi diversi a seconda del tipo di legami che deve formare. L'ibridazione sp³ (109,5°) forma solo legami singoli ed è la più stabile. L'ibridazione sp² (120°) permette la formazione di legami doppi, mentre l'ibridazione sp (180°) crea legami tripli.
Nei legami multipli, il primo legame è sempre sigma (σ), mentre gli altri sono pigreco (π). I legami π si formano per sovrapposizione laterale degli orbitali e sono più deboli di quelli σ. La presenza di legami π impedisce la rotazione attorno all'asse, rendendo la molecola più rigida.
Un carbonio sp³ viene chiamato saturo perché è legato al massimo numero di atomi possibili e non può formare altri legami. I composti con solo carboni saturi sono i più stabili perché hanno solo legami σ e nessun legame π.
Le concatenazioni carboniose possono essere lineari, ramificate o cicliche. I legami C-C e C-H sono molto forti perché poco polari, dando stabilità alle molecole organiche.
💡 Tip per l'esame: Ricorda che maggiore ibridazione s = maggiore stabilità!

Gruppi Funzionali
I gruppi funzionali sono la parte più importante delle molecole organiche - sono loro che determinano le proprietà chimiche e fisiche! Possono essere legami multipli, atomi diversi da C e H, o gruppi di atomi specifici.
Durante una reazione chimica, è sempre il gruppo funzionale che reagisce - è la parte reattiva della molecola. Il resto della molecola (lo scheletro carbonioso) di solito rimane inalterato.
I gruppi funzionali più importanti includono: ossidrile negli alcoli, carbonile in aldeidi e chetoni, carbossile negli acidi, e amminico nelle ammine. Ogni gruppo conferisce proprietà specifiche: gli alcoli sono polari e solubili in acqua, gli acidi sono... acidi!
La nomenclatura segue regole precise: trova la catena più lunga contenente il gruppo funzionale, identifica il gruppo, numera partendo dall'estremità più vicina al gruppo funzionale, e indica eventuali ramificazioni.
💡 Trucco: Per ricordare i prefissi usa "MET ET PROP BUT PENT ES EPT" - come una filastrocca!

Isomeria di Struttura
L'isomeria è uno dei concetti più fighi della chimica organica! Gli isomeri hanno la stessa formula bruta ma strutture diverse - è come avere gli stessi mattoncini Lego ma costruire case completamente diverse.
L'isomeria di catena cambia la concatenazione dei carboni: puoi avere una catena lineare o ramificata con la stessa formula C₅H₁₂. L'isomeria di posizione sposta il gruppo funzionale lungo la catena - immagina di spostare una finestra da una parte all'altra della casa.
L'isomeria di gruppo funzionale è ancora più interessante: con C₃H₈O puoi ottenere sia un alcol che un etere . Stessa formula, famiglie chimiche completamente diverse con proprietà totalmente differenti!
Ogni tipo di isomeria produce composti con proprietà fisiche e chimiche diverse. Gli alcoli sono polari e si sciolgono in acqua, gli eteri sono meno polari. È incredibile come la stessa "ricetta" atomica possa dare risultati così diversi!
💡 Metodo di studio: Disegna sempre le strutture - vedere gli isomeri ti aiuta a capirli meglio delle formule!

Stereoisomeria
La stereoisomeria è diversa dall'isomeria strutturale perché riguarda come gli atomi sono orientati nello spazio, non come sono connessi. È come guardare la stessa molecola da angolazioni diverse!
L'isomeria conformazionale si verifica attorno ai legami semplici σ che possono ruotare liberamente. Nell'etano, i gruppi possono essere sfalsati (più stabili) o eclissati (meno stabili) - ma possono passare dall'una all'altra forma senza rompere legami.
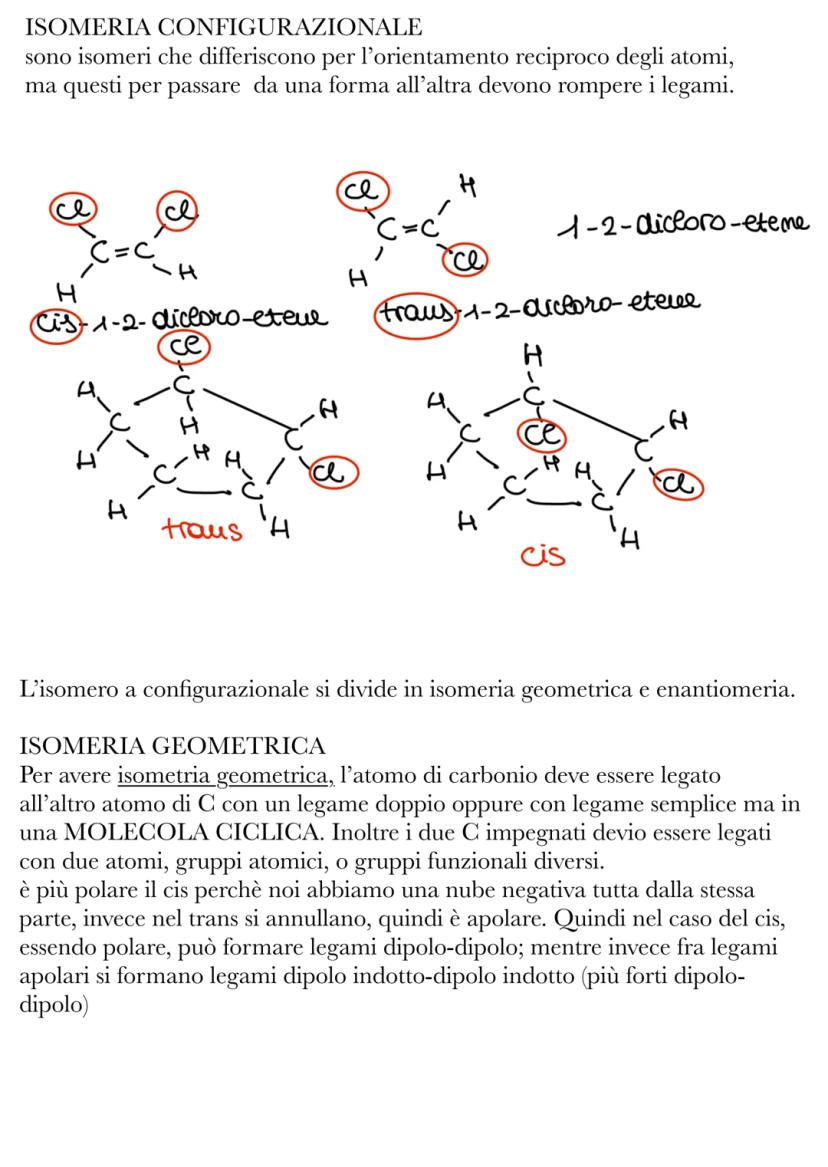
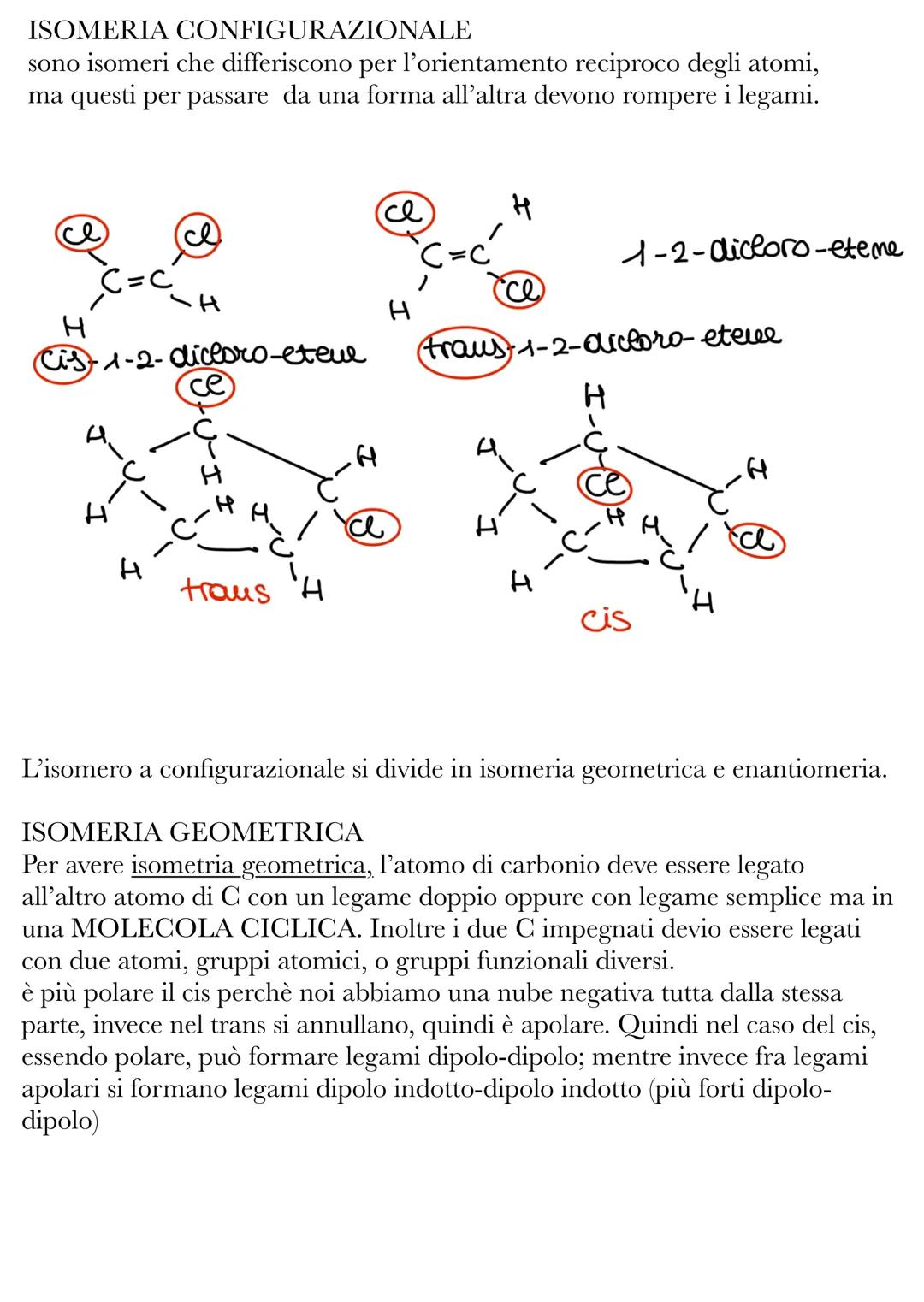
L'isomeria configurazionale è più interessante perché per cambiare forma devi rompere i legami! L'isomeria geometrica si ha con legami doppi dove i gruppi possono stare dalla stessa parte (cis) o da parti opposte (trans) del doppio legame.
Gli isomeri cis sono più polari perché hanno i gruppi uguali dalla stessa parte, creando un dipolo. Gli isomeri trans sono più simmetrici e quindi apolari. Questa differenza influenza le proprietà fisiche come punti di fusione ed ebollizione.
💡 Visualizza: I legami doppi sono come cerniere bloccate - non possono ruotare!
Enantiomeria e Chiralità
L'enantiomeria è probabilmente il tipo di isomeria più affascinante! Due molecole sono enantiomeri quando sono l'immagine speculare l'una dell'altra, come le tue mani - simili ma non sovrapponibili.
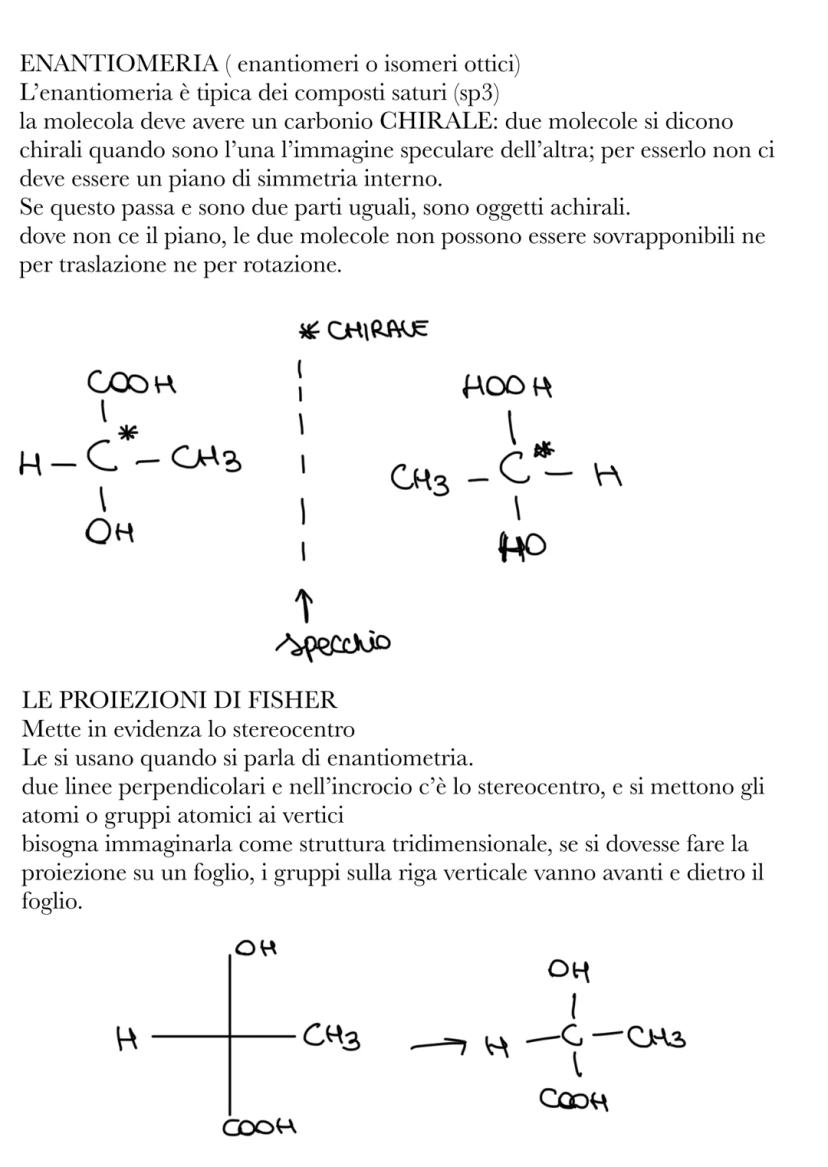
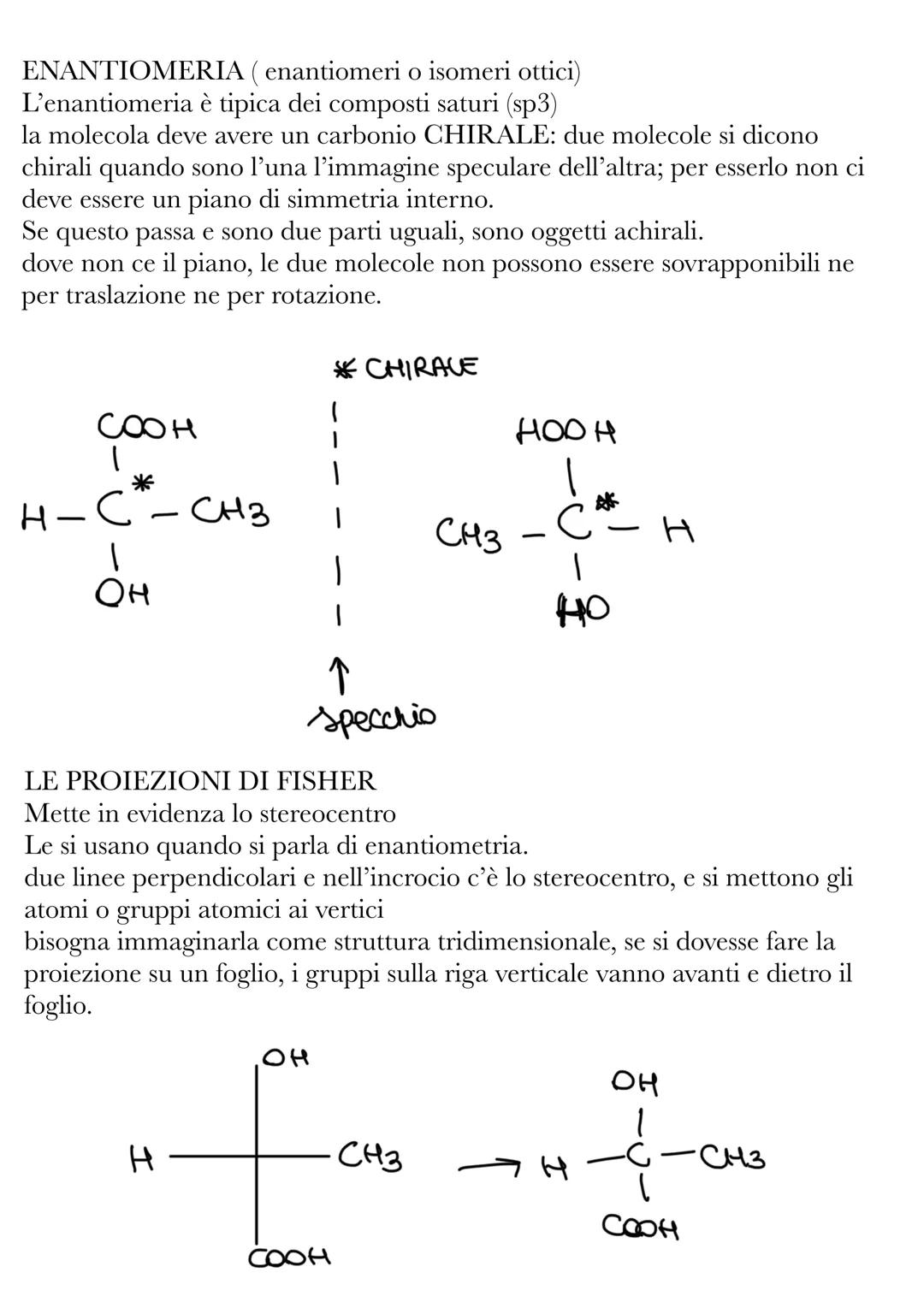
Perché questo accada, serve un carbonio chirale (o stereocentro) - un carbonio sp³ legato a 4 gruppi diversi. Se riesci a tracciare un piano di simmetria nella molecola, allora non è chirale.
La cosa incredibile degli enantiomeri è che hanno l'attività ottica - fanno ruotare il piano della luce polarizzata! Un enantiomero la ruota verso destra (destrogiro), l'altro verso sinistra (levogiro). Si misura con il polarimetro.
Le proiezioni di Fischer sono un modo pratico per rappresentare gli enantiomeri su carta. Si disegnano come una croce con lo stereocentro al centro - i gruppi verticali vanno dietro/davanti al foglio, quelli orizzontali restano sul piano.
💡 Applicazione real-world: Molti farmaci sono chirali - solo un enantiomero è attivo, l'altro può essere inutile o addirittura dannoso!
Proprietà e Reattività
Gli enantiomeri sono gemelli quasi identici! Hanno le stesse proprietà achirali: punto di fusione, ebollizione, densità e solubilità. Quello che cambia è la reattività con agenti chirali - come enzimi che riconoscono solo un enantiomero.
Una miscela racemica (50:50 dei due enantiomeri) non mostra attività ottica perché gli effetti si annullano. È come avere due persone che spingono una porta in direzioni opposte con la stessa forza.
Le proprietà fisiche dei composti organici dipendono dalla polarità. Molecole apolari hanno forze di London deboli, sono idrofobe e hanno punti di fusione/ebollizione bassi. Molecole polari formano legami più forti, sono idrofile e più difficili da fondere/far bollire.
La catena carboniosa influenza molto le proprietà: più è lunga, più alta è la temperatura di ebollizione. Le ramificazioni riducono i contatti intermolecolari, abbassando i punti di fusione ed ebollizione.
La reattività dipende dal gruppo funzionale (parte reattiva), dal grado di insaturazione e dalla presenza di legami polari.
💡 Regola pratica: Molecola più stabile = meno reattiva. La stabilità è nemica della reattività!


Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari di Scienze
9Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Apparato respiratorio
fai un quiz
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Apparato Digerente
Presentazione sull’apparato digerente, con questa presentazione un buono voto è assicurato
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Platone
Riassunto dettagliato su Platone
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Chimica Organica: La Scienza del Carbonio
La chimica organica è il mondo affascinante delle molecole che contengono carbonio, dagli idrocarburi più semplici alle complesse biomolecole del nostro corpo. Il carbonio, con la sua capacità unica di formare catene e legami stabili, è il protagonista di milioni... Mostra di più

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
La Chimica del Carbonio
Pensa a tutto quello che ti circonda: dalla plastica del tuo smartphone alle proteine nei tuoi muscoli. Tutti questi materiali hanno una cosa in comune: contengono carbonio. I composti organici sono semplicemente molecole che hanno carbonio legato ad almeno un atomo di idrogeno.
Non tutti i composti con carbonio sono organici però! La CO₂ che espiri è inorganica perché manca il legame carbonio-idrogeno. Gli elementi che formano composti organici sono principalmente carbonio, idrogeno, ossigeno, azoto, fosforo e zolfo - tutti con raggi atomici piccoli e elettronegatività medio-alta.
Il segreto del carbonio sta nella sua elettronegatività intermedia (2,5) che gli permette di formare legami covalenti poco polari e molto stabili. Quando si lega con altri carboni o con l'idrogeno forma legami praticamente apolari, quindi super stabili. Inoltre ha un'incredibile capacità di concatenazione - può legarsi con altri atomi di carbonio formando catene lunghissime e ramificazioni complesse.
💡 Ricorda: Un legame poco polare è più stabile perché gli elettroni sono condivisi equamente, mentre nei legami polari c'è uno sbilanciamento che rende la molecola meno stabile.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
L'Ibridazione del Carbonio
Ecco dove diventa interessante! Nel suo stato fondamentale, il carbonio dovrebbe fare solo 2 legami. Ma fornendo un po' di energia, il doppietto 2s si separa e otteniamo 4 elettroni spaiati che possono formare 4 legami. Questo processo si chiama ibridazione.
Gli orbitali s e p si "mescolano" creando nuovi orbitali ibridi sp³ con forma intermedia tra quella sferica (s) e quella a otto (p). Questi 4 orbitali si dispongono nello spazio con angoli di 109,5° ai vertici di un tetraedro - la disposizione più stabile possibile.
L'ibridazione sp³ crea solo legami sigma (σ) - i più forti e stabili. Questi legami permettono la rotazione attorno all'asse di legame, rendendo le molecole flessibili. I legami sigma si formano per sovrapposizione frontale degli orbitali lungo la linea che unisce i nuclei.
💡 Curiosità: Gli orbitali ibridi sp³ sono isoenergetici - hanno tutti la stessa energia, distribuita equamente tra loro!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Tipi di Ibridazione e Legami
Il carbonio può ibridarsi in tre modi diversi a seconda del tipo di legami che deve formare. L'ibridazione sp³ (109,5°) forma solo legami singoli ed è la più stabile. L'ibridazione sp² (120°) permette la formazione di legami doppi, mentre l'ibridazione sp (180°) crea legami tripli.
Nei legami multipli, il primo legame è sempre sigma (σ), mentre gli altri sono pigreco (π). I legami π si formano per sovrapposizione laterale degli orbitali e sono più deboli di quelli σ. La presenza di legami π impedisce la rotazione attorno all'asse, rendendo la molecola più rigida.
Un carbonio sp³ viene chiamato saturo perché è legato al massimo numero di atomi possibili e non può formare altri legami. I composti con solo carboni saturi sono i più stabili perché hanno solo legami σ e nessun legame π.
Le concatenazioni carboniose possono essere lineari, ramificate o cicliche. I legami C-C e C-H sono molto forti perché poco polari, dando stabilità alle molecole organiche.
💡 Tip per l'esame: Ricorda che maggiore ibridazione s = maggiore stabilità!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Gruppi Funzionali
I gruppi funzionali sono la parte più importante delle molecole organiche - sono loro che determinano le proprietà chimiche e fisiche! Possono essere legami multipli, atomi diversi da C e H, o gruppi di atomi specifici.
Durante una reazione chimica, è sempre il gruppo funzionale che reagisce - è la parte reattiva della molecola. Il resto della molecola (lo scheletro carbonioso) di solito rimane inalterato.
I gruppi funzionali più importanti includono: ossidrile negli alcoli, carbonile in aldeidi e chetoni, carbossile negli acidi, e amminico nelle ammine. Ogni gruppo conferisce proprietà specifiche: gli alcoli sono polari e solubili in acqua, gli acidi sono... acidi!
La nomenclatura segue regole precise: trova la catena più lunga contenente il gruppo funzionale, identifica il gruppo, numera partendo dall'estremità più vicina al gruppo funzionale, e indica eventuali ramificazioni.
💡 Trucco: Per ricordare i prefissi usa "MET ET PROP BUT PENT ES EPT" - come una filastrocca!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Isomeria di Struttura
L'isomeria è uno dei concetti più fighi della chimica organica! Gli isomeri hanno la stessa formula bruta ma strutture diverse - è come avere gli stessi mattoncini Lego ma costruire case completamente diverse.
L'isomeria di catena cambia la concatenazione dei carboni: puoi avere una catena lineare o ramificata con la stessa formula C₅H₁₂. L'isomeria di posizione sposta il gruppo funzionale lungo la catena - immagina di spostare una finestra da una parte all'altra della casa.
L'isomeria di gruppo funzionale è ancora più interessante: con C₃H₈O puoi ottenere sia un alcol che un etere . Stessa formula, famiglie chimiche completamente diverse con proprietà totalmente differenti!
Ogni tipo di isomeria produce composti con proprietà fisiche e chimiche diverse. Gli alcoli sono polari e si sciolgono in acqua, gli eteri sono meno polari. È incredibile come la stessa "ricetta" atomica possa dare risultati così diversi!
💡 Metodo di studio: Disegna sempre le strutture - vedere gli isomeri ti aiuta a capirli meglio delle formule!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Stereoisomeria
La stereoisomeria è diversa dall'isomeria strutturale perché riguarda come gli atomi sono orientati nello spazio, non come sono connessi. È come guardare la stessa molecola da angolazioni diverse!
L'isomeria conformazionale si verifica attorno ai legami semplici σ che possono ruotare liberamente. Nell'etano, i gruppi possono essere sfalsati (più stabili) o eclissati (meno stabili) - ma possono passare dall'una all'altra forma senza rompere legami.
L'isomeria configurazionale è più interessante perché per cambiare forma devi rompere i legami! L'isomeria geometrica si ha con legami doppi dove i gruppi possono stare dalla stessa parte (cis) o da parti opposte (trans) del doppio legame.
Gli isomeri cis sono più polari perché hanno i gruppi uguali dalla stessa parte, creando un dipolo. Gli isomeri trans sono più simmetrici e quindi apolari. Questa differenza influenza le proprietà fisiche come punti di fusione ed ebollizione.
💡 Visualizza: I legami doppi sono come cerniere bloccate - non possono ruotare!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Enantiomeria e Chiralità
L'enantiomeria è probabilmente il tipo di isomeria più affascinante! Due molecole sono enantiomeri quando sono l'immagine speculare l'una dell'altra, come le tue mani - simili ma non sovrapponibili.
Perché questo accada, serve un carbonio chirale (o stereocentro) - un carbonio sp³ legato a 4 gruppi diversi. Se riesci a tracciare un piano di simmetria nella molecola, allora non è chirale.
La cosa incredibile degli enantiomeri è che hanno l'attività ottica - fanno ruotare il piano della luce polarizzata! Un enantiomero la ruota verso destra (destrogiro), l'altro verso sinistra (levogiro). Si misura con il polarimetro.
Le proiezioni di Fischer sono un modo pratico per rappresentare gli enantiomeri su carta. Si disegnano come una croce con lo stereocentro al centro - i gruppi verticali vanno dietro/davanti al foglio, quelli orizzontali restano sul piano.
💡 Applicazione real-world: Molti farmaci sono chirali - solo un enantiomero è attivo, l'altro può essere inutile o addirittura dannoso!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Proprietà e Reattività
Gli enantiomeri sono gemelli quasi identici! Hanno le stesse proprietà achirali: punto di fusione, ebollizione, densità e solubilità. Quello che cambia è la reattività con agenti chirali - come enzimi che riconoscono solo un enantiomero.
Una miscela racemica (50:50 dei due enantiomeri) non mostra attività ottica perché gli effetti si annullano. È come avere due persone che spingono una porta in direzioni opposte con la stessa forza.
Le proprietà fisiche dei composti organici dipendono dalla polarità. Molecole apolari hanno forze di London deboli, sono idrofobe e hanno punti di fusione/ebollizione bassi. Molecole polari formano legami più forti, sono idrofile e più difficili da fondere/far bollire.
La catena carboniosa influenza molto le proprietà: più è lunga, più alta è la temperatura di ebollizione. Le ramificazioni riducono i contatti intermolecolari, abbassando i punti di fusione ed ebollizione.
La reattività dipende dal gruppo funzionale (parte reattiva), dal grado di insaturazione e dalla presenza di legami polari.
💡 Regola pratica: Molecola più stabile = meno reattiva. La stabilità è nemica della reattività!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari di Scienze
9Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Apparato respiratorio
fai un quiz
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Apparato Digerente
Presentazione sull’apparato digerente, con questa presentazione un buono voto è assicurato
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Platone
Riassunto dettagliato su Platone
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.