Benvenuto nel mondo della chimica quantistica! Scoprirai come la luce... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
1,137
•
Aggiornato Mar 21, 2026
•
alessia
@alessiapani
Benvenuto nel mondo della chimica quantistica! Scoprirai come la luce... Mostra di più










Immagina di lanciare un sasso in uno stagno: le onde elettromagnetiche funzionano in modo simile, ma invece di muovere l'acqua, fanno oscillare campi elettrici e magnetici nello spazio. Queste onde trasportano energia ma non materia - proprio come la luce del sole che arriva fino a te senza portare particelle fisiche.
Ogni onda ha delle caratteristiche specifiche: la lunghezza d'onda (distanza tra due creste), la frequenza (quante oscillazioni fa al secondo) e l'ampiezza (quanto è intensa). Nel vuoto, tutte viaggiano alla velocità della luce usando la formula c = λ × ν (lunghezza d'onda per frequenza).
Quando attraversano materiali diversi dall'aria, rallentano a causa dell'indice di rifrazione - ecco perché una cannuccia sembra spezzata nell'acqua! La velocità diventa v = c/n, dove n è sempre maggiore di 1 nei materiali.
💡 Ricorda: Se un'onda ha lunghezza d'onda grande, avrà frequenza piccola - sono inversamente proporzionali!
I tuoi occhi possono vedere solo una piccola parte delle onde elettromagnetiche - quella che chiamiamo luce visibile. Gli oggetti hanno colori diversi perché assorbono alcune frequenze e ne riflettono altre verso i tuoi occhi.
La luce ha una doppia natura: si comporta sia come un'onda che come un fascio di particelle chiamate fotoni. Ogni fotone è come un "pacchetto di energia" senza massa che viaggia alla velocità della luce, con energia calcolabile tramite E = h × ν.
Quando riscaldi un gas puro, emette uno spettro a righe - linee colorate specifiche su sfondo nero che funzionano come un'impronta digitale per identificare l'elemento. Al contrario, lo spettro di assorbimento mostra righe nere su sfondo colorato quando la luce passa attraverso un gas che assorbe certe frequenze.

Alla fine dell'800, uno strano esperimento mise in crisi tutta la fisica conosciuta. Gli scienziati studiavano il corpo nero - un oggetto teorico che assorbe tutta la radiazione senza riflettere nulla, come un buco nero perfetto.
Il problema era che la legge di Rayleigh-Jeans prediceva che questo corpo dovesse emettere energia infinita alle lunghezze d'onda piccole - una situazione impossibile chiamata "catastrofe ultravioletta". Era come dire che ogni oggetto caldo dovrebbe brillare con intensità infinita!
Nel 1900, Max Planck risolse brillantemente il mistero introducendo un'idea rivoluzionaria: l'energia non viene scambiata in modo continuo, ma a "pacchetti" discreti chiamati quanti. La formula E = h × ν divenne la base della fisica quantistica.
💡 Curiosità: Questa scoperta cambiò per sempre la nostra comprensione dell'universo - da quel momento sappiamo che l'energia viene "venduta" solo in porzioni specifiche!

Niels Bohr nel 1913 propose un modello rivoluzionario dell'atomo. Immaginò l'elettrone come un pianeta che orbita attorno al nucleo-sole, mantenuto in equilibrio tra l'attrazione elettrica e la forza centrifuga. Ma con una differenza cruciale: solo certe orbite sono permesse!
Secondo Bohr, l'elettrone può esistere solo in stati stazionari specifici senza perdere energia. L'energia viene emessa solo quando salta da un'orbita più esterna a una più interna, come scendere i gradini di una scala quantistica.
Il momento angolare è quantizzato - l'elettrone può muoversi solo a certe velocità e distanze specifiche dal nucleo. Il raggio delle orbite segue la formula r = n²/z × a₀, dove n è il numero quantico principale.
Nonostante il successo, questo modello funziona solo per l'idrogeno e gli atomi idrogenoidi. I postulati sembrano arbitrari e manca una giustificazione teorica solida - problemi che portarono allo sviluppo della meccanica quantistica.
💡 Nota bene: Bohr introdusse la quantizzazione "a forza" - la meccanica quantistica la farà emergere naturalmente dalle equazioni!

La meccanica quantistica cambia completamente la nostra visione dell'atomo. L'elettrone non ha una posizione precisa, ma solo una probabilità di trovarsi in certi luoghi - nasce il famoso dualismo onda-particella di De Broglie.
Lo stato di un sistema è descritto dalla funzione d'onda ψ (psi), che contiene tutte le informazioni possibili su una particella. Per trovarla, devi risolvere l'equazione di Schrödinger: Hψ = iℏ ∂ψ/∂t, dove H è l'operatore hamiltoniano.
La funzione d'onda in sé non ha significato fisico - è solo matematica. Quello che conta è ψ², che ti dice la probabilità di trovare la particella in un certo volume di spazio.
Due esempi chiariscono tutto: una particella libera si muove come un'onda sinusoidale, mentre una particella "nella scatola" (confinata tra due pareti) sviluppa automaticamente livelli energetici quantizzati - senza imposizioni arbitrarie come in Bohr!
💡 Rivoluzione mentale: La quantizzazione non viene imposta dall'esterno, ma emerge naturalmente quando vincoli il moto di una particella!

Nell'atomo di idrogeno hai un protone al centro e un elettrone che si muove nello spazio tridimensionale, soggetto sia all'energia cinetica che a quella potenziale (negativa per l'attrazione elettrica).
Risolvendo l'equazione di Schrödinger emergono spontaneamente tre numeri quantici che descrivono completamente il moto dell'elettrone:
Per l'idrogeno, l'energia dipende solo da n, ma per ogni valore di n esistono diversi stati con la stessa energia - sono chiamati stati degeneri. Per esempio, con n=2 hai quattro modi diversi per l'elettrone di muoversi, tutti con identica energia.
💡 Concetto chiave: Maggiore è il valore negativo dell'energia, più l'elettrone è "legato" al nucleo - come essere in fondo a un pozzo gravitazionale!

Gli orbitali sono le regioni di spazio dove hai la massima probabilità di trovare un elettrone. Per descriverli usiamo coordinate sferiche (r, θ, φ) invece di quelle cartesiane, perché l'atomo ha simmetria sferica.
La funzione d'onda può essere separata in due parti: una parte radiale che dipende solo dalla distanza dal nucleo (r), e una parte angolare che dipende dall'orientamento nello spazio (θ, φ).
Quello che ha significato fisico è ψ²dV - ti dice la probabilità di trovare l'elettrone in un piccolo volume dV attorno a un punto specifico. È come avere una mappa delle probabilità tridimensionale!
La funzione d'onda ψ può essere positiva o negativa (come le onde che oscillano sopra e sotto il livello del mare), ma ψ² è sempre positiva perché rappresenta una probabilità.
💡 Visualizza: Pensa agli orbitali come a "nuvole elettroniche" - più dense dove la probabilità è alta, più rade dove è bassa!

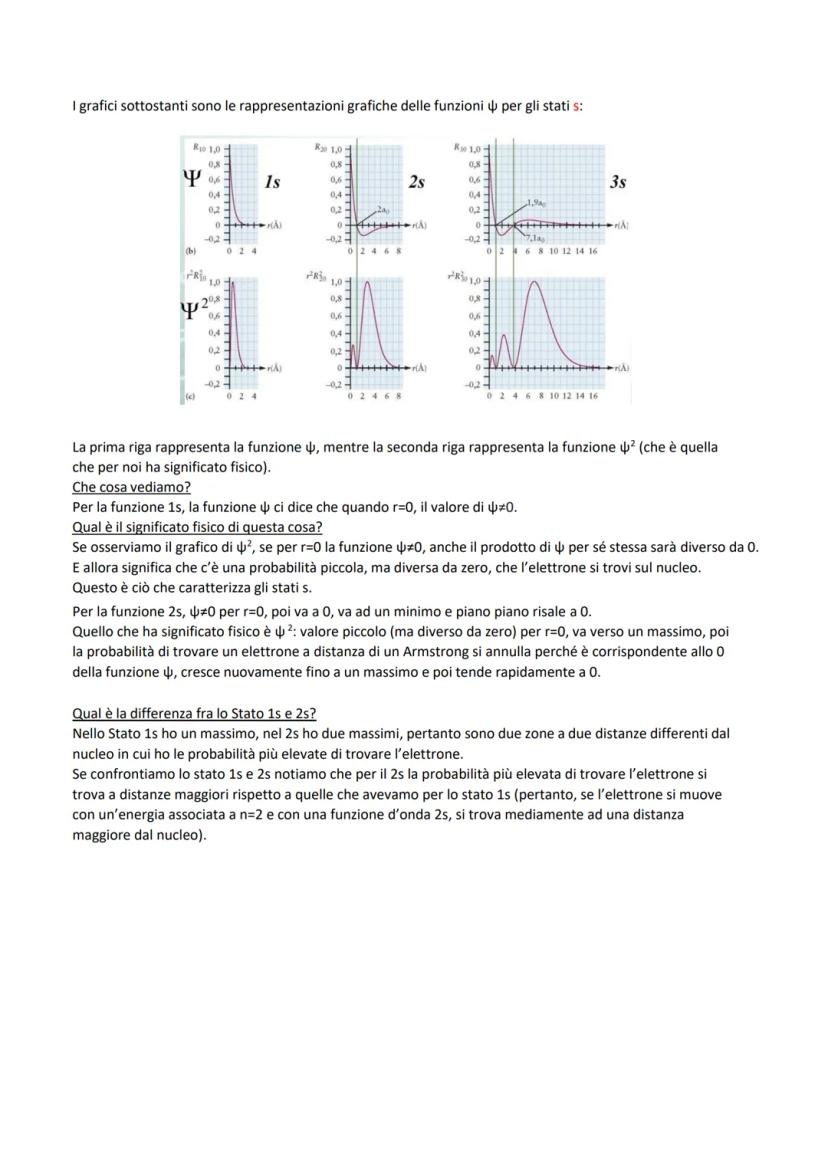
I grafici mostrano come varia la funzione d'onda ψ e la probabilità ψ² con la distanza dal nucleo per gli orbitali s.
Per l'orbitale 1s: ψ ha valore massimo al centro e decresce esponenzialmente. Questo significa che c'è una piccola ma reale probabilità di trovare l'elettrone proprio sul nucleo - caratteristica unica degli stati s!
Per l'orbitale 2s: la situazione si complica. ψ parte diversa da zero, va a zero (creando un nodo), diventa negativa, poi torna a zero. Il grafico di ψ² mostra due massimi - due "zone preferite" a distanze diverse dal nucleo.
La differenza cruciale: l'elettrone 2s si trova mediamente più lontano dal nucleo rispetto al 1s, e ha due regioni di alta probabilità invece di una sola. Più aumenta n, più l'elettrone si allontana dal nucleo.
💡 Osservazione: Gli zeri della funzione d'onda sono chiamati "nodi" - punti dove la probabilità di trovare l'elettrone è esattamente zero!

Gli orbitali s hanno simmetria sferica - sembrano sfere concentriche attorno al nucleo. Ogni livello s può contenere massimo 2 elettroni e la probabilità di trovarli sul nucleo non è zero.
Gli orbitali p hanno forma completamente diversa: due "gocce" simmetriche che si toccano al centro, dove la probabilità di trovare l'elettrone è zero. Esistono tre orbitali p orientati lungo gli assi x, y, z, per un totale di 6 elettroni massimi.
Gli orbitali d sono ancora più complessi, con forme che ricordano quadrifogli o ciambelle. Il sottolivello d può ospitare fino a 10 elettroni.
I colori diversi negli orbitali p e d rappresentano i segni positivo e negativo della funzione d'onda ψ - ma ricorda che ψ² (la probabilità) è sempre positiva!
💡 Regola pratica: Ogni tipo di orbitale ha una capacità specifica: s→2, p→6, d→10, f→14 elettroni!

Oltre ai tre numeri quantici spaziali, gli elettroni possiedono una quarta proprietà chiamata spin. Questa scoperta arrivò da un esperimento sorprendente: atomi di idrogeno neutri deviavano in un campo magnetico!
Se l'atomo è neutro, perché subisce deviazioni? Perché gli elettroni si comportano come piccoli magneti che possono orientarsi in due modi opposti. Il fascio di atomi si separa in due parti distinte.
Gli elettroni possono avere spin +1/2 o spin -1/2 - li rappresentiamo con frecce verso l'alto ↑ o verso il basso ↓. Non è un movimento fisico di rotazione, ma una proprietà quantistica fondamentale.
Per descrivere completamente un elettrone servono quindi quattro numeri quantici: n, l, m e spin. Questa quaterna è come un "indirizzo completo" che identifica univocamente lo stato di ogni elettrone.
💡 Analogia: Lo spin è come avere un interruttore che può essere solo "su" o "giù" - non esistono posizioni intermedie!

Gli atomi con più elettroni sono molto più complicati dell'idrogeno, ma usiamo gli stessi principi base. Ogni elettrone si muove in un campo efficace creato dal nucleo (attrazione) e dagli altri elettroni (repulsione).
Gli orbitali mantengono forme simili a quelli dell'idrogeno, ma sono più piccoli perché il nucleo più carico attrae più forte. L'energia ora dipende sia da n che da l - si perde la degenerazione tra s, p, d, f.
Per costruire la configurazione elettronica dello stato fondamentale segui queste regole:
💡 Strategia: Pensa agli elettroni come persone che salgono su un autobus - prima si siedono da soli, poi si affiancano!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
alessia
@alessiapani
Benvenuto nel mondo della chimica quantistica! Scoprirai come la luce e gli elettroni si comportano in modi che spesso contraddicono quello che vedi nella vita quotidiana, e come questi fenomeni spiegano la struttura degli atomi che compongono tutto ciò che... Mostra di più

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Immagina di lanciare un sasso in uno stagno: le onde elettromagnetiche funzionano in modo simile, ma invece di muovere l'acqua, fanno oscillare campi elettrici e magnetici nello spazio. Queste onde trasportano energia ma non materia - proprio come la luce del sole che arriva fino a te senza portare particelle fisiche.
Ogni onda ha delle caratteristiche specifiche: la lunghezza d'onda (distanza tra due creste), la frequenza (quante oscillazioni fa al secondo) e l'ampiezza (quanto è intensa). Nel vuoto, tutte viaggiano alla velocità della luce usando la formula c = λ × ν (lunghezza d'onda per frequenza).
Quando attraversano materiali diversi dall'aria, rallentano a causa dell'indice di rifrazione - ecco perché una cannuccia sembra spezzata nell'acqua! La velocità diventa v = c/n, dove n è sempre maggiore di 1 nei materiali.
💡 Ricorda: Se un'onda ha lunghezza d'onda grande, avrà frequenza piccola - sono inversamente proporzionali!
I tuoi occhi possono vedere solo una piccola parte delle onde elettromagnetiche - quella che chiamiamo luce visibile. Gli oggetti hanno colori diversi perché assorbono alcune frequenze e ne riflettono altre verso i tuoi occhi.
La luce ha una doppia natura: si comporta sia come un'onda che come un fascio di particelle chiamate fotoni. Ogni fotone è come un "pacchetto di energia" senza massa che viaggia alla velocità della luce, con energia calcolabile tramite E = h × ν.
Quando riscaldi un gas puro, emette uno spettro a righe - linee colorate specifiche su sfondo nero che funzionano come un'impronta digitale per identificare l'elemento. Al contrario, lo spettro di assorbimento mostra righe nere su sfondo colorato quando la luce passa attraverso un gas che assorbe certe frequenze.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Alla fine dell'800, uno strano esperimento mise in crisi tutta la fisica conosciuta. Gli scienziati studiavano il corpo nero - un oggetto teorico che assorbe tutta la radiazione senza riflettere nulla, come un buco nero perfetto.
Il problema era che la legge di Rayleigh-Jeans prediceva che questo corpo dovesse emettere energia infinita alle lunghezze d'onda piccole - una situazione impossibile chiamata "catastrofe ultravioletta". Era come dire che ogni oggetto caldo dovrebbe brillare con intensità infinita!
Nel 1900, Max Planck risolse brillantemente il mistero introducendo un'idea rivoluzionaria: l'energia non viene scambiata in modo continuo, ma a "pacchetti" discreti chiamati quanti. La formula E = h × ν divenne la base della fisica quantistica.
💡 Curiosità: Questa scoperta cambiò per sempre la nostra comprensione dell'universo - da quel momento sappiamo che l'energia viene "venduta" solo in porzioni specifiche!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Niels Bohr nel 1913 propose un modello rivoluzionario dell'atomo. Immaginò l'elettrone come un pianeta che orbita attorno al nucleo-sole, mantenuto in equilibrio tra l'attrazione elettrica e la forza centrifuga. Ma con una differenza cruciale: solo certe orbite sono permesse!
Secondo Bohr, l'elettrone può esistere solo in stati stazionari specifici senza perdere energia. L'energia viene emessa solo quando salta da un'orbita più esterna a una più interna, come scendere i gradini di una scala quantistica.
Il momento angolare è quantizzato - l'elettrone può muoversi solo a certe velocità e distanze specifiche dal nucleo. Il raggio delle orbite segue la formula r = n²/z × a₀, dove n è il numero quantico principale.
Nonostante il successo, questo modello funziona solo per l'idrogeno e gli atomi idrogenoidi. I postulati sembrano arbitrari e manca una giustificazione teorica solida - problemi che portarono allo sviluppo della meccanica quantistica.
💡 Nota bene: Bohr introdusse la quantizzazione "a forza" - la meccanica quantistica la farà emergere naturalmente dalle equazioni!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La meccanica quantistica cambia completamente la nostra visione dell'atomo. L'elettrone non ha una posizione precisa, ma solo una probabilità di trovarsi in certi luoghi - nasce il famoso dualismo onda-particella di De Broglie.
Lo stato di un sistema è descritto dalla funzione d'onda ψ (psi), che contiene tutte le informazioni possibili su una particella. Per trovarla, devi risolvere l'equazione di Schrödinger: Hψ = iℏ ∂ψ/∂t, dove H è l'operatore hamiltoniano.
La funzione d'onda in sé non ha significato fisico - è solo matematica. Quello che conta è ψ², che ti dice la probabilità di trovare la particella in un certo volume di spazio.
Due esempi chiariscono tutto: una particella libera si muove come un'onda sinusoidale, mentre una particella "nella scatola" (confinata tra due pareti) sviluppa automaticamente livelli energetici quantizzati - senza imposizioni arbitrarie come in Bohr!
💡 Rivoluzione mentale: La quantizzazione non viene imposta dall'esterno, ma emerge naturalmente quando vincoli il moto di una particella!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Nell'atomo di idrogeno hai un protone al centro e un elettrone che si muove nello spazio tridimensionale, soggetto sia all'energia cinetica che a quella potenziale (negativa per l'attrazione elettrica).
Risolvendo l'equazione di Schrödinger emergono spontaneamente tre numeri quantici che descrivono completamente il moto dell'elettrone:
Per l'idrogeno, l'energia dipende solo da n, ma per ogni valore di n esistono diversi stati con la stessa energia - sono chiamati stati degeneri. Per esempio, con n=2 hai quattro modi diversi per l'elettrone di muoversi, tutti con identica energia.
💡 Concetto chiave: Maggiore è il valore negativo dell'energia, più l'elettrone è "legato" al nucleo - come essere in fondo a un pozzo gravitazionale!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Gli orbitali sono le regioni di spazio dove hai la massima probabilità di trovare un elettrone. Per descriverli usiamo coordinate sferiche (r, θ, φ) invece di quelle cartesiane, perché l'atomo ha simmetria sferica.
La funzione d'onda può essere separata in due parti: una parte radiale che dipende solo dalla distanza dal nucleo (r), e una parte angolare che dipende dall'orientamento nello spazio (θ, φ).
Quello che ha significato fisico è ψ²dV - ti dice la probabilità di trovare l'elettrone in un piccolo volume dV attorno a un punto specifico. È come avere una mappa delle probabilità tridimensionale!
La funzione d'onda ψ può essere positiva o negativa (come le onde che oscillano sopra e sotto il livello del mare), ma ψ² è sempre positiva perché rappresenta una probabilità.
💡 Visualizza: Pensa agli orbitali come a "nuvole elettroniche" - più dense dove la probabilità è alta, più rade dove è bassa!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
I grafici mostrano come varia la funzione d'onda ψ e la probabilità ψ² con la distanza dal nucleo per gli orbitali s.
Per l'orbitale 1s: ψ ha valore massimo al centro e decresce esponenzialmente. Questo significa che c'è una piccola ma reale probabilità di trovare l'elettrone proprio sul nucleo - caratteristica unica degli stati s!
Per l'orbitale 2s: la situazione si complica. ψ parte diversa da zero, va a zero (creando un nodo), diventa negativa, poi torna a zero. Il grafico di ψ² mostra due massimi - due "zone preferite" a distanze diverse dal nucleo.
La differenza cruciale: l'elettrone 2s si trova mediamente più lontano dal nucleo rispetto al 1s, e ha due regioni di alta probabilità invece di una sola. Più aumenta n, più l'elettrone si allontana dal nucleo.
💡 Osservazione: Gli zeri della funzione d'onda sono chiamati "nodi" - punti dove la probabilità di trovare l'elettrone è esattamente zero!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Gli orbitali s hanno simmetria sferica - sembrano sfere concentriche attorno al nucleo. Ogni livello s può contenere massimo 2 elettroni e la probabilità di trovarli sul nucleo non è zero.
Gli orbitali p hanno forma completamente diversa: due "gocce" simmetriche che si toccano al centro, dove la probabilità di trovare l'elettrone è zero. Esistono tre orbitali p orientati lungo gli assi x, y, z, per un totale di 6 elettroni massimi.
Gli orbitali d sono ancora più complessi, con forme che ricordano quadrifogli o ciambelle. Il sottolivello d può ospitare fino a 10 elettroni.
I colori diversi negli orbitali p e d rappresentano i segni positivo e negativo della funzione d'onda ψ - ma ricorda che ψ² (la probabilità) è sempre positiva!
💡 Regola pratica: Ogni tipo di orbitale ha una capacità specifica: s→2, p→6, d→10, f→14 elettroni!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Oltre ai tre numeri quantici spaziali, gli elettroni possiedono una quarta proprietà chiamata spin. Questa scoperta arrivò da un esperimento sorprendente: atomi di idrogeno neutri deviavano in un campo magnetico!
Se l'atomo è neutro, perché subisce deviazioni? Perché gli elettroni si comportano come piccoli magneti che possono orientarsi in due modi opposti. Il fascio di atomi si separa in due parti distinte.
Gli elettroni possono avere spin +1/2 o spin -1/2 - li rappresentiamo con frecce verso l'alto ↑ o verso il basso ↓. Non è un movimento fisico di rotazione, ma una proprietà quantistica fondamentale.
Per descrivere completamente un elettrone servono quindi quattro numeri quantici: n, l, m e spin. Questa quaterna è come un "indirizzo completo" che identifica univocamente lo stato di ogni elettrone.
💡 Analogia: Lo spin è come avere un interruttore che può essere solo "su" o "giù" - non esistono posizioni intermedie!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Gli atomi con più elettroni sono molto più complicati dell'idrogeno, ma usiamo gli stessi principi base. Ogni elettrone si muove in un campo efficace creato dal nucleo (attrazione) e dagli altri elettroni (repulsione).
Gli orbitali mantengono forme simili a quelli dell'idrogeno, ma sono più piccoli perché il nucleo più carico attrae più forte. L'energia ora dipende sia da n che da l - si perde la degenerazione tra s, p, d, f.
Per costruire la configurazione elettronica dello stato fondamentale segui queste regole:
💡 Strategia: Pensa agli elettroni come persone che salgono su un autobus - prima si siedono da soli, poi si affiancano!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
25
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS