La forma delle molecole determina le loro proprietà chimiche e... Mostra di più
La Forma delle Molecole e le Forze Intermolecolari




La Geometria Molecolare e la Teoria VSEPR
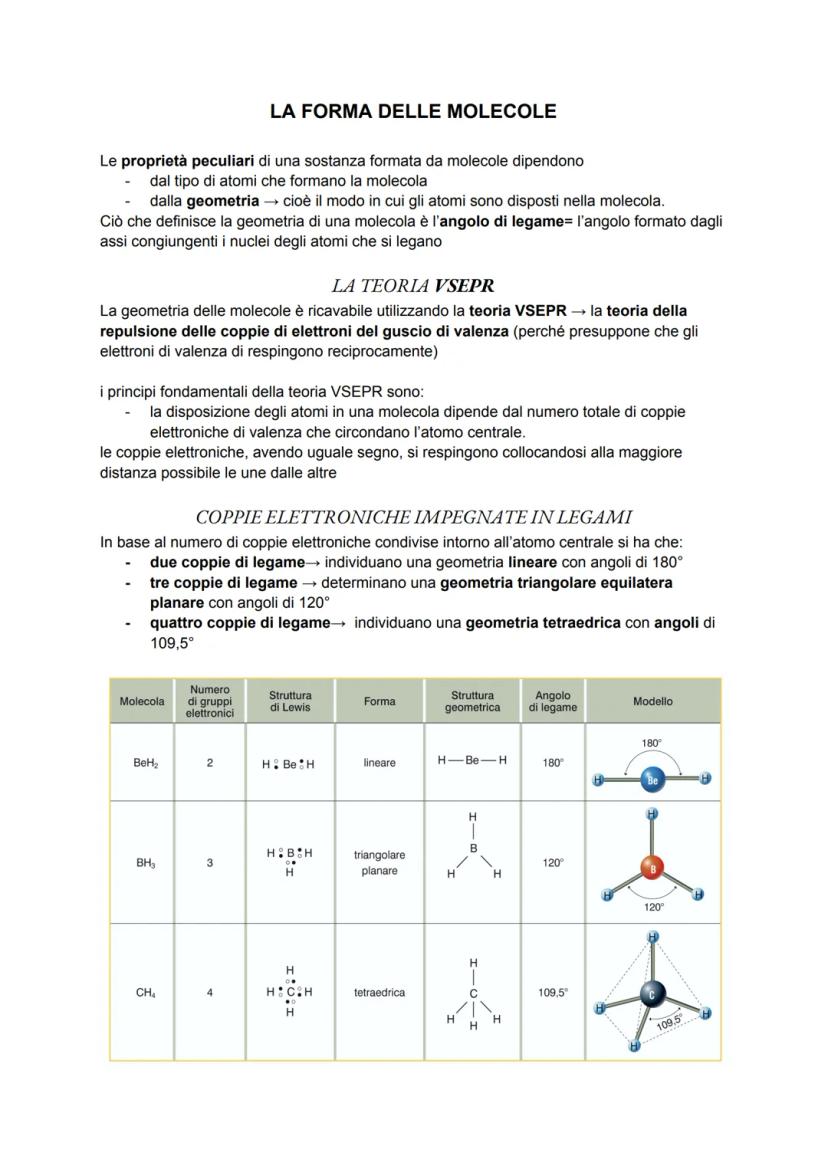
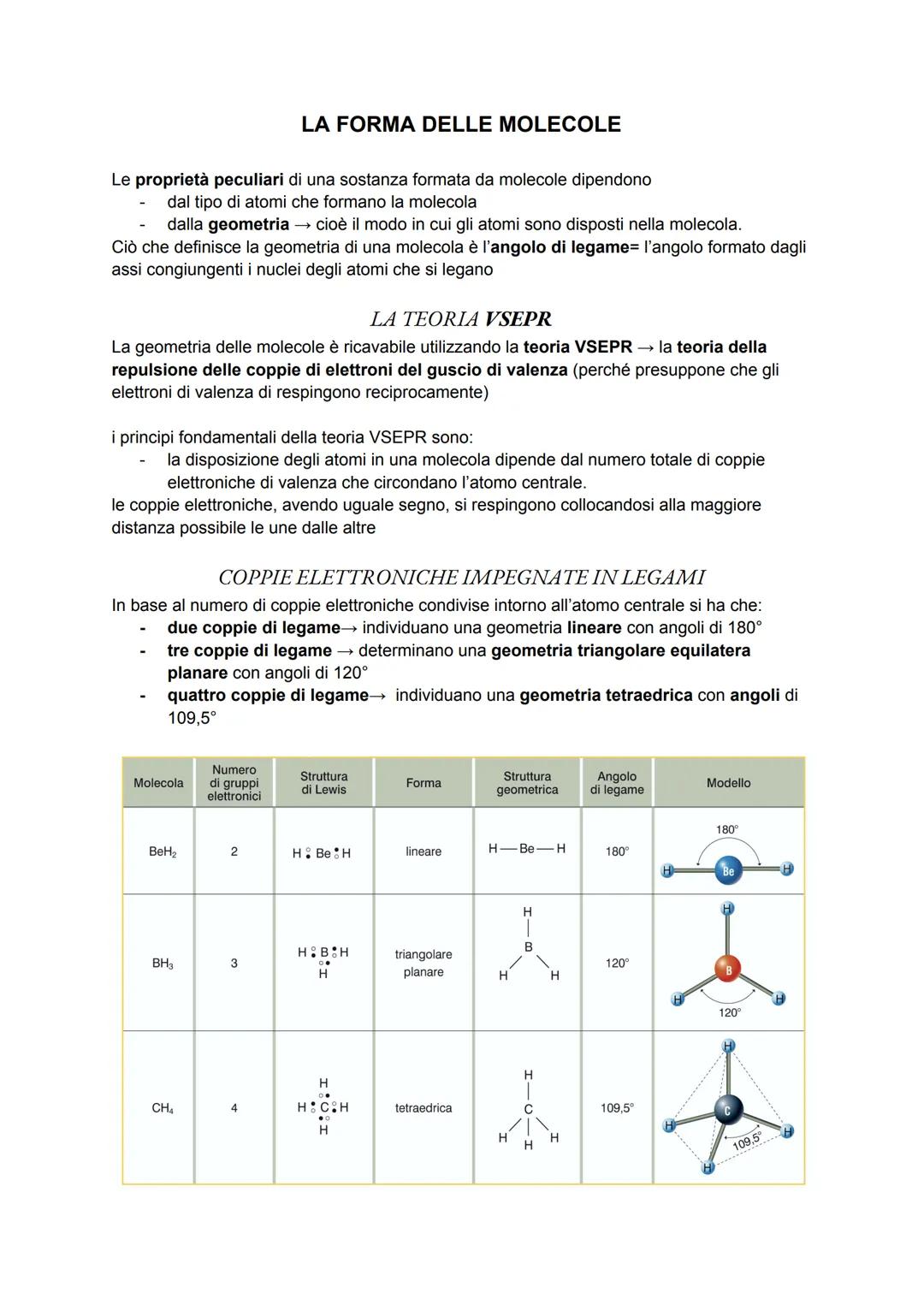
Sai perché l'acqua ha proprietà così diverse dal metano? Tutto dipende dalla geometria molecolare, cioè come gli atomi sono disposti nello spazio. La forma di una molecola dipende dagli angoli di legame tra gli atomi.
La teoria VSEPR (repulsione delle coppie elettroniche) ci spiega come prevedere queste forme. Il principio è semplice: gli elettroni si respingono e cercano di stare il più lontano possibile tra loro.
Con due coppie di elettroni ottieni una geometria lineare (180°), come in BeH₂. Tre coppie formano una struttura triangolare planare (120°), come BH₃. Quattro coppie creano una geometria tetraedrica (109,5°), come nel metano CH₄.
💡 Ricorda: Più coppie elettroniche = geometrie più complesse!

Coppie Libere e Polarità delle Molecole
Le coppie elettroniche libere cambiano tutto! Essendo attratte da un solo nucleo, occupano più spazio e "schiacciano" gli angoli di legame. Per questo l'ammoniaca NH₃ ha angoli più piccoli del tetraedro perfetto.
Anche i legami doppi e tripli influenzano la geometria, comportandosi come un'unica unità geometrica.
Una molecola può essere polare o apolare. Il momento dipolare misura questa polarità: è come una freccia che punta verso l'atomo più elettronegativo. Molecole simmetriche come CO₂ e CCl₄ sono apolari perché i dipoli si annullano.
💡 Trucco: Geometria simmetrica + atomi uguali = molecola apolare!
Molecole come H₂O e CHCl₃ sono polari perché i dipoli non si annullano e creano una risultante.

Forze Intermolecolari
Ora che conosci la polarità, scopri cosa tiene unite le molecole! Le forze intermolecolari sono attrazioni elettrostatiche tra molecole diverse, molto più deboli dei legami covalenti.
Le più forti sono i legami a idrogeno, che si formano quando l'idrogeno è legato a N, O o F. Poi ci sono le forze di Van der Waals: le forze dipolo-dipolo tra molecole polari, che si orientano con poli opposti vicini.
Le forze dipolo-dipolo indotto si creano quando una molecola polare "induce" un dipolo temporaneo in una molecola apolare vicina.
💡 Ordine di intensità: Legami a idrogeno > dipolo-dipolo > dipolo indotto > forze di London

Forze di London e Legami a Idrogeno
Le forze di London sono le più deboli ma universali. Esistono anche tra molecole apolari come H₂ e gas nobili! Gli elettroni si muovono continuamente, creando dipoli temporanei che si attraggono.
Queste forze aumentano con le dimensioni della molecola e diminuiscono rapidamente con la distanza.
I legami a idrogeno sono forze dipolo-dipolo super intense. Si formano solo quando H è legato a N, O o F - atomi piccoli ed elettronegativi con coppie libere.
💡 Ricorda: H-N, H-O, H-F = legami a idrogeno garantiti!
Questi legami si formano e si spezzano continuamente, dando proprietà uniche alle sostanze che li contengono.

L'Acqua: Un Caso Speciale
L'acqua è il perfetto esempio di come i legami a idrogeno cambino tutto! Ogni molecola H₂O può formare 4 legami a idrogeno: ogni H ne forma 1, ogni O ne forma 2.
Nel ghiaccio tutti e 4 si formano stabilmente, nell'acqua liquida si spezzano e riformano continuamente.
Questo spiega le proprietà anomale dell'acqua: temperatura di ebollizione alta (serve energia per spezzare i legami), elevato calore specifico (parte dell'energia serve per rompere i legami), e minor densità da solida (il reticolo cristallino occupa più spazio).
💡 Pensaci: Senza legami a idrogeno, l'acqua bollirebbe a -80°C!
La forza dei legami decresce così: covalente > ionico > metallico > idrogeno > Van der Waals.
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari di Scienze
9ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Apparato respiratorio
fai un quiz
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Cellula procariote ed eucariote.
Descrizione delle diverse tipologie di microscopi ottici ed elettronici e la struttura della cellula procariote ed eucariote. Composizione delle cellule ed organuli cellulari.
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
La Forma delle Molecole e le Forze Intermolecolari
La forma delle molecole determina le loro proprietà chimiche e fisiche. Capire come gli atomi si dispongono nello spazio e come le molecole interagiscono tra loro ti aiuterà a prevedere il comportamento delle sostanze che studi ogni giorno.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
La Geometria Molecolare e la Teoria VSEPR
Sai perché l'acqua ha proprietà così diverse dal metano? Tutto dipende dalla geometria molecolare, cioè come gli atomi sono disposti nello spazio. La forma di una molecola dipende dagli angoli di legame tra gli atomi.
La teoria VSEPR (repulsione delle coppie elettroniche) ci spiega come prevedere queste forme. Il principio è semplice: gli elettroni si respingono e cercano di stare il più lontano possibile tra loro.
Con due coppie di elettroni ottieni una geometria lineare (180°), come in BeH₂. Tre coppie formano una struttura triangolare planare (120°), come BH₃. Quattro coppie creano una geometria tetraedrica (109,5°), come nel metano CH₄.
💡 Ricorda: Più coppie elettroniche = geometrie più complesse!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Coppie Libere e Polarità delle Molecole
Le coppie elettroniche libere cambiano tutto! Essendo attratte da un solo nucleo, occupano più spazio e "schiacciano" gli angoli di legame. Per questo l'ammoniaca NH₃ ha angoli più piccoli del tetraedro perfetto.
Anche i legami doppi e tripli influenzano la geometria, comportandosi come un'unica unità geometrica.
Una molecola può essere polare o apolare. Il momento dipolare misura questa polarità: è come una freccia che punta verso l'atomo più elettronegativo. Molecole simmetriche come CO₂ e CCl₄ sono apolari perché i dipoli si annullano.
💡 Trucco: Geometria simmetrica + atomi uguali = molecola apolare!
Molecole come H₂O e CHCl₃ sono polari perché i dipoli non si annullano e creano una risultante.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Forze Intermolecolari
Ora che conosci la polarità, scopri cosa tiene unite le molecole! Le forze intermolecolari sono attrazioni elettrostatiche tra molecole diverse, molto più deboli dei legami covalenti.
Le più forti sono i legami a idrogeno, che si formano quando l'idrogeno è legato a N, O o F. Poi ci sono le forze di Van der Waals: le forze dipolo-dipolo tra molecole polari, che si orientano con poli opposti vicini.
Le forze dipolo-dipolo indotto si creano quando una molecola polare "induce" un dipolo temporaneo in una molecola apolare vicina.
💡 Ordine di intensità: Legami a idrogeno > dipolo-dipolo > dipolo indotto > forze di London

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Forze di London e Legami a Idrogeno
Le forze di London sono le più deboli ma universali. Esistono anche tra molecole apolari come H₂ e gas nobili! Gli elettroni si muovono continuamente, creando dipoli temporanei che si attraggono.
Queste forze aumentano con le dimensioni della molecola e diminuiscono rapidamente con la distanza.
I legami a idrogeno sono forze dipolo-dipolo super intense. Si formano solo quando H è legato a N, O o F - atomi piccoli ed elettronegativi con coppie libere.
💡 Ricorda: H-N, H-O, H-F = legami a idrogeno garantiti!
Questi legami si formano e si spezzano continuamente, dando proprietà uniche alle sostanze che li contengono.

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
L'Acqua: Un Caso Speciale
L'acqua è il perfetto esempio di come i legami a idrogeno cambino tutto! Ogni molecola H₂O può formare 4 legami a idrogeno: ogni H ne forma 1, ogni O ne forma 2.
Nel ghiaccio tutti e 4 si formano stabilmente, nell'acqua liquida si spezzano e riformano continuamente.
Questo spiega le proprietà anomale dell'acqua: temperatura di ebollizione alta (serve energia per spezzare i legami), elevato calore specifico (parte dell'energia serve per rompere i legami), e minor densità da solida (il reticolo cristallino occupa più spazio).
💡 Pensaci: Senza legami a idrogeno, l'acqua bollirebbe a -80°C!
La forza dei legami decresce così: covalente > ionico > metallico > idrogeno > Van der Waals.
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari di Scienze
9ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Apparato respiratorio
fai un quiz
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Cellula procariote ed eucariote.
Descrizione delle diverse tipologie di microscopi ottici ed elettronici e la struttura della cellula procariote ed eucariote. Composizione delle cellule ed organuli cellulari.
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.