I legami chimici sono il "collante" che tiene insieme gli... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
1,198
•
Aggiornato Mar 19, 2026
•
Simona Nardulli
@simonanardulli
I legami chimici sono il "collante" che tiene insieme gli... Mostra di più






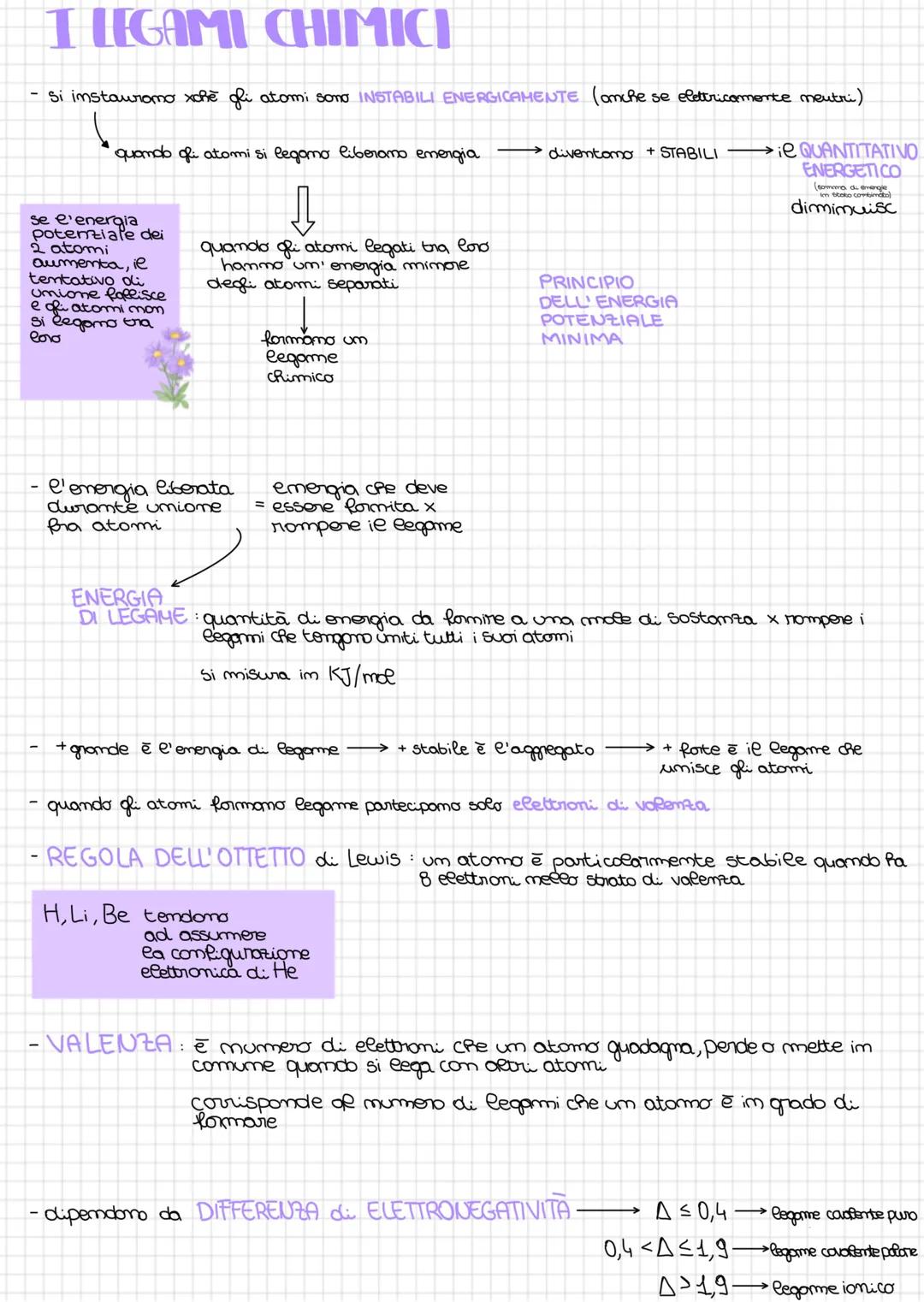
Sai perché gli atomi si uniscono tra loro? La risposta è semplice: sono instabili energeticamente quando sono da soli! Quando si legano, liberano energia e diventano più stabili, seguendo il principio dell'energia potenziale minima.
L'energia di legame è la quantità di energia che devi fornire per spezzare un legame chimico. Si misura in KJ/mol e ti dice quanto è forte un legame: più energia serve per romperlo, più il legame è stabile e resistente.
Solo gli elettroni di valenza partecipano ai legami chimici. La regola dell'ottetto di Lewis spiega che gli atomi sono particolarmente stabili quando hanno 8 elettroni nel guscio esterno (tranne idrogeno, litio e berillio che preferiscono 2 elettroni come l'elio).
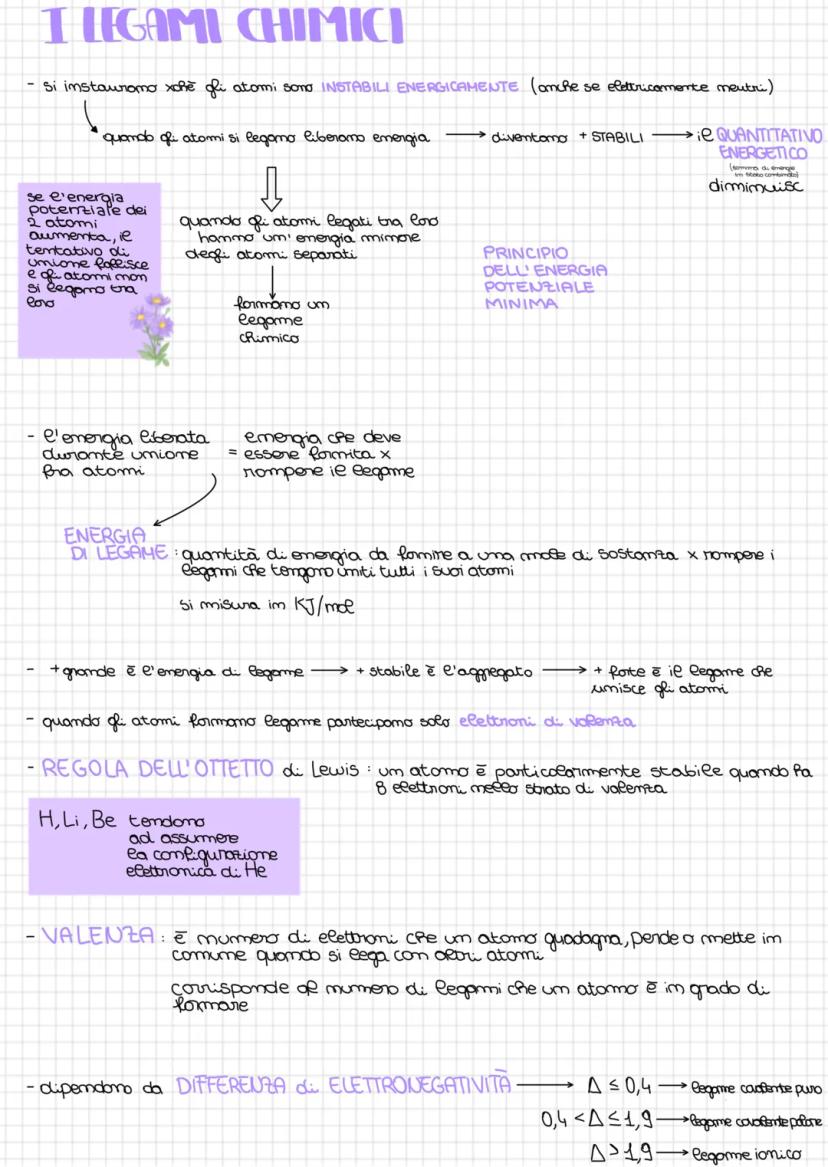
💡 Ricorda: La forza del legame dipende dalla differenza di elettronegatività tra gli atomi: Δ ≤ 0,4 = covalente puro; 0,4 < Δ ≤ 1,9 = covalente polare; Δ > 1,9 = ionico.

Immagina un metallo generoso che cede elettroni e un non metallo avido che li accetta: ecco come nasce il legame ionico! I due atomi diventano ioni con cariche opposte che si attraggono grazie alla forza elettrostatica.
Gli ioni non rimangono isolati ma formano un reticolo cristallino, una struttura ordinata e ripetitiva dove ogni ione è circondato da ioni di carica opposta. È come un puzzle tridimensionale perfettamente organizzato!
I metalli dei gruppi I, II e III tendono a perdere elettroni (diventando ioni positivi), mentre i non metalli dei gruppi VI, VII e VIII li acquistano (diventando ioni negativi). I metalli di transizione come ferro e argento possono perdere quantità diverse di elettroni.
I composti ionici hanno caratteristiche distintive: sono solidi a temperatura ambiente, hanno punti di fusione elevati e conducono elettricità quando sono sciolti in acqua (ma non da solidi, perché gli ioni sono "bloccati" nel reticolo).
⚡ Curiosità: L'elettricità nei composti ionici viaggia attraverso il movimento degli ioni, non degli elettroni come nei metalli!

Nel mondo dei metalli succede qualcosa di affascinante: si forma una nube elettronica dove gli elettroni più esterni si muovono liberamente! È come avere una "piscina" di elettroni condivisa tra tutti gli atomi metallici.
Gli ioni metallici positivi si dispongono in modo ordinato formando un reticolo cristallino, mentre gli elettroni mobili li circondano creando una struttura compatta che riduce al minimo gli spazi vuoti.
Questa particolare struttura spiega le proprietà tipiche dei metalli: conducibilità elettrica e termica elevata proprio perché gli elettroni sono già in movimento e possono trasportare facilmente energia.
La forza del legame metallico varia lungo un periodo della tavola periodica, influenzando proprietà come durezza e punto di fusione dei diversi metalli.
🔧 Applicazione pratica: La mobilità degli elettroni nei metalli è il principio che rende possibili tutti i circuiti elettrici che usi ogni giorno!
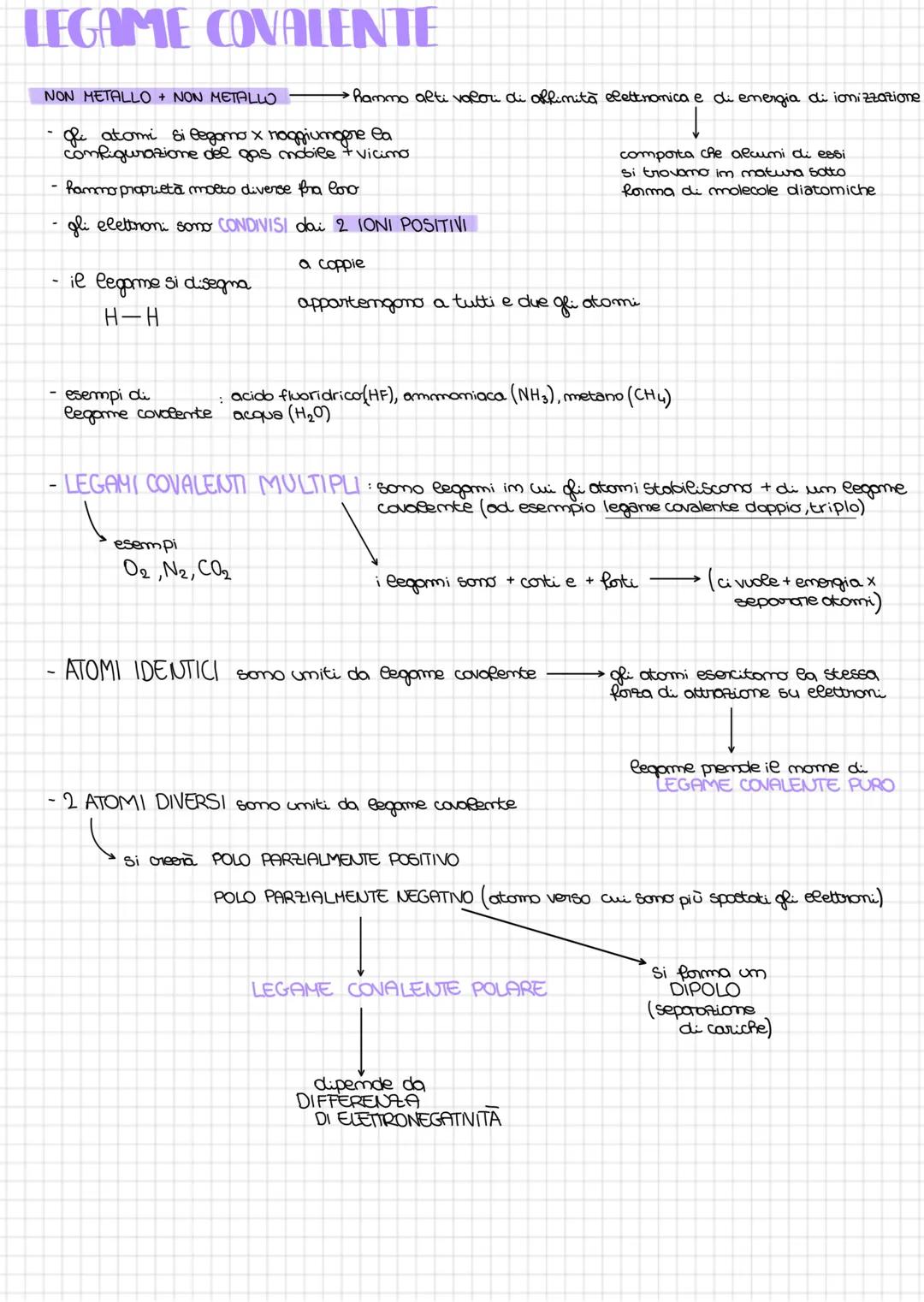
Quando due non metalli si incontrano, non si "rubano" elettroni come nel legame ionico: li condividono! Questo è il legame covalente, dove gli elettroni appartengono a entrambi gli atomi contemporaneamente.
Puoi avere legami covalenti multipli: doppi o tripli, che sono più corti e più forti dei legami singoli. Esempi comuni sono O₂, N₂ e CO₂. Più legami ci sono, più energia serve per separare gli atomi!
Esistono due tipi principali: il legame covalente puro (tra atomi identici) e il legame covalente polare (tra atomi diversi). Nel secondo caso si forma un dipolo con un polo parzialmente positivo e uno negativo.
La polarità dipende dalla differenza di elettronegatività: l'atomo più elettronegativo attira di più gli elettroni condivisi, creando quella separazione di cariche che chiamiamo dipolo.
🧪 Esempi quotidiani: L'acqua (H₂O), l'ammoniaca (NH₃) e il metano (CH₄) sono tutti composti con legami covalenti che usi nella vita di tutti i giorni!

Hai mai sentito parlare di atomi "generosi" che donano una coppia di elettroni già completa? È esattamente quello che succede nel legame covalente dativo! Un atomo che ha già raggiunto l'ottetto dona una coppia di elettroni a un altro atomo.
Si indica con una freccia (→) che va dal donatore all'accettore. La particolarità è che entrambi gli elettroni del legame provengono da un solo atomo, non uno per ciascuno come nel covalente normale.
Esempi tipici sono gli acidi del cloro: HClO (acido ipocloroso), HClO₂ (acido cloroso), HClO₃ (acido clorico) e HClO₄ (acido perclorico).
I composti con legami dativi si chiamano complessi o composti di coordinazione: sono formati da un metallo centrale circondato da atomi donatori chiamati "leganti", mentre il metallo è detto "coordinante".
🎯 Trucco per ricordare: Nel legame dativo c'è sempre un "donatore" generoso e un "accettore" bisognoso - come prestare gli appunti a un compagno!

Scrivere le formule di struttura è come risolvere un puzzle: devi seguire alcune regole precise! Prima di tutto, metti al centro l'atomo più elettronegativo (eccetto l'idrogeno, che fa sempre eccezione).
Ogni atomo ha un numero preferito di legami: l'idrogeno forma sempre 1 legame, il carbonio 4, l'azoto 3 e l'ossigeno 2. È come se ognuno avesse la sua "firma" chimica!
Completa sempre gli ottetti di tutti gli atomi intorno all'atomo centrale. Gli atomi coinvolti nei legami multipli sono principalmente C, N, O e S.
Il trucco è considerare prima i legami singoli per soddisfare le esigenze base di ogni atomo, poi aggiungere legami multipli se necessario per completare gli ottetti.
✏️ Strategia di studio: Esercitati partendo dalle molecole più semplici come H₂O e CH₄, poi passa gradualmente a quelle più complesse!
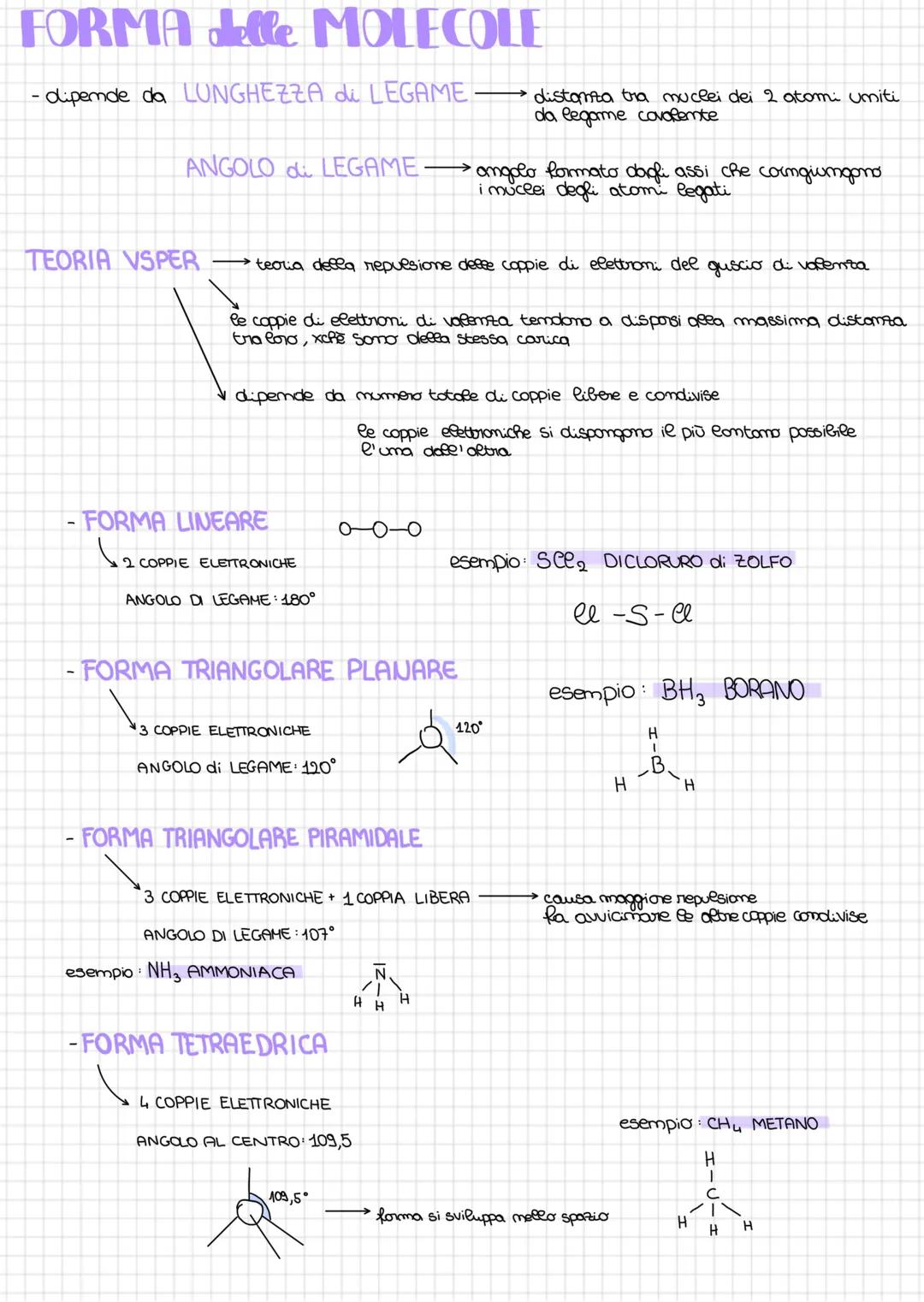
Le molecole non sono piatte come le disegniamo sul foglio: hanno forme tridimensionali precise! La forma dipende dalla lunghezza di legame (distanza tra i nuclei) e dall'angolo di legame tra gli assi che collegano i nuclei.
La teoria VSEPR spiega tutto: le coppie di elettroni si respingono perché hanno la stessa carica, quindi si dispongono alla massima distanza possibile. È come persone che cercano di stare il più lontano possibile in una stanza!
Ecco le forme principali: lineare (2 coppie, 180°), triangolare piana (3 coppie, 120°), tetraedrica (4 coppie, 109,5°). L'ammoniaca (NH₃) ha forma piramidale (107°) perché ha una coppia libera che "spinge" di più.
L'acqua (H₂O) ha forma piegata con angolo di 104,5° perché le sue due coppie libere esercitano una repulsione extra forte sulle coppie condivise.
🏗️ Visualizza: Immagina gli elettroni come magneti con la stessa polarità che si respingono - questo ti aiuterà a capire le forme molecolari!
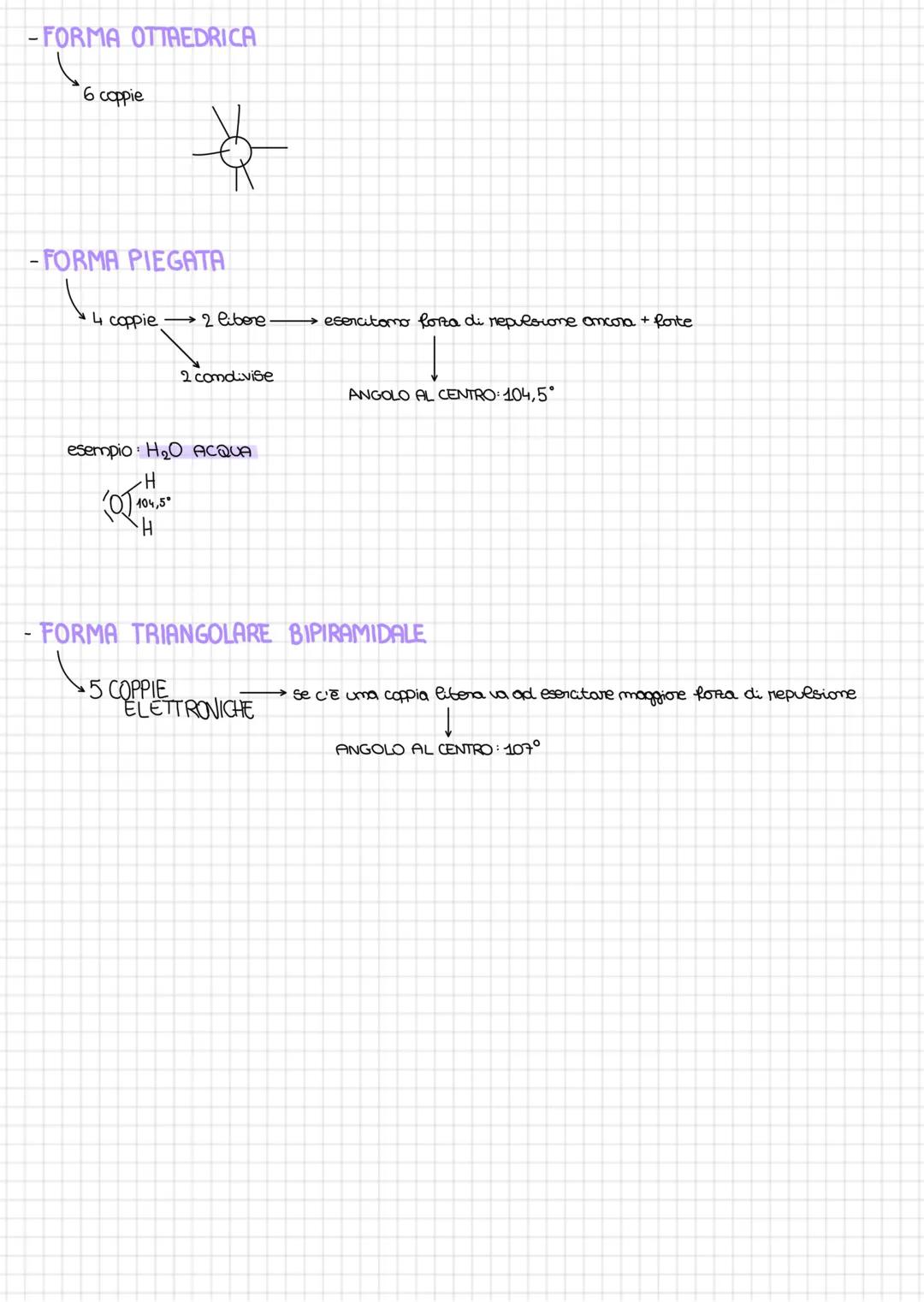
Oltre alle forme base, esistono geometrie più complesse! La forma ottaedrica si ha con 6 coppie elettroniche, mentre la forma triangolare bipiramidale coinvolge 5 coppie con angolo di 107°.
Quando hai coppie libere, ricorda che esercitano sempre una forza di repulsione più forte delle coppie condivise. Questo "spinge" gli altri elettroni modificando gli angoli di legame.
La forma piegata dell'acqua (H₂O) con i suoi 104,5° è un perfetto esempio di come 2 coppie libere possano influenzare drasticamente la geometria molecolare.
🔍 Osservazione: Le coppie libere sono come "pesi invisibili" che modificano la forma delle molecole anche se non le vediamo nelle formule!
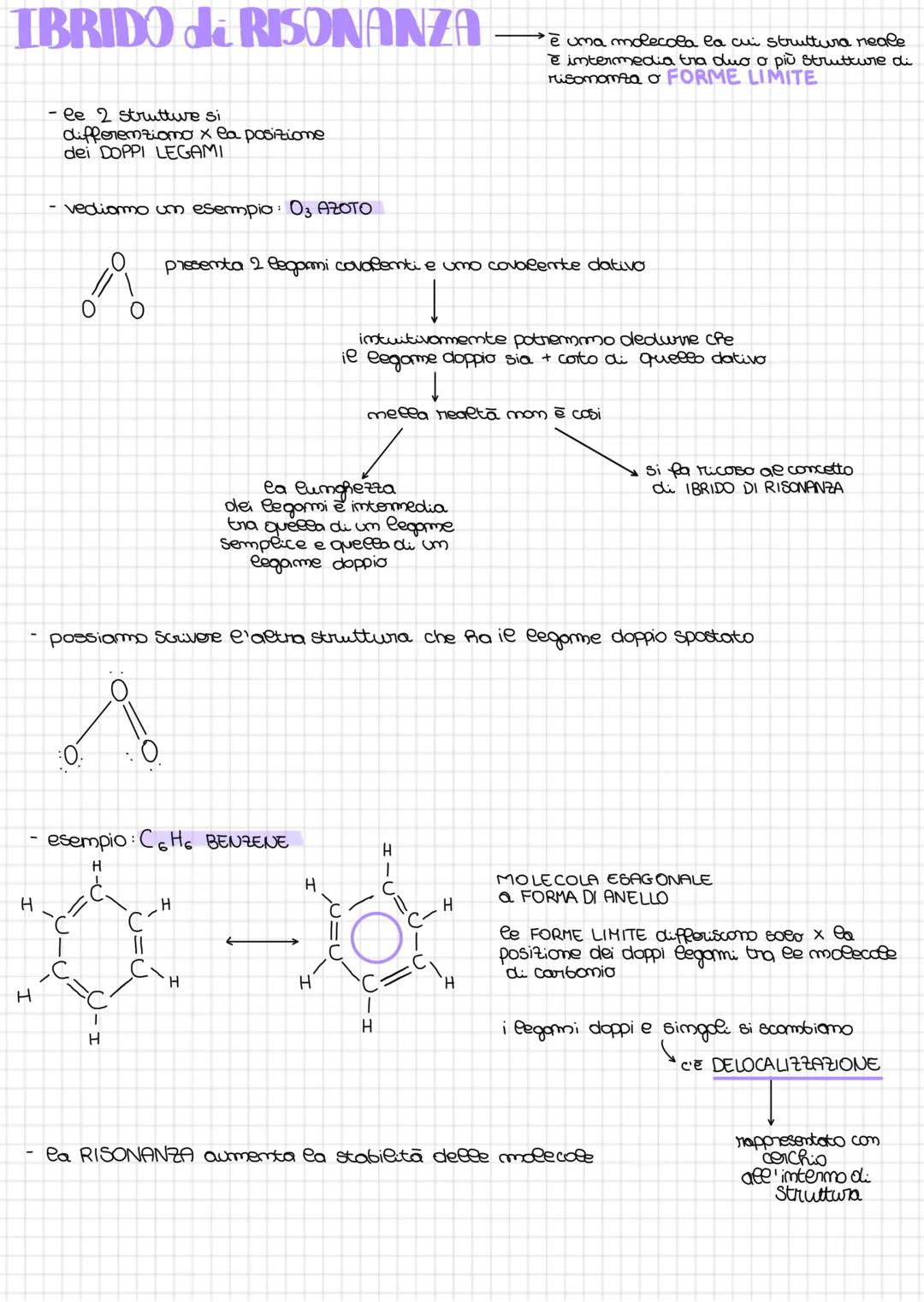
Alcune molecole sono come "camaleoni" chimici: la loro struttura reale è intermedia tra due o più forme limite! Questo fenomeno si chiama ibrido di risonanza.
Prendiamo l'ozono (O₃): teoricamente dovrebbe avere un legame doppio e uno dativo di lunghezze diverse, ma in realtà entrambi i legami hanno la stessa lunghezza intermedia. I doppi legami si "scambiano" continuamente posizione!
Il benzene (C₆H₆) è l'esempio più famoso: è una molecola esagonale dove i legami doppi e singoli tra i carboni si delocalizzano. Si rappresenta con un cerchio all'interno dell'esagono per indicare questa delocalizzazione.
La risonanza aumenta la stabilità delle molecole perché gli elettroni sono distribuiti su una superficie maggiore, come spalmare il peso su una base più ampia.
🎨 Analogia: È come un disegno che cambia continuamente tra due versioni, ma quello che vedi è sempre una via di mezzo tra le due!

Linus Pauling ha ideato la teoria VB per spiegare come si formano concretamente i legami. L'idea è che gli orbitali atomici contenenti elettroni spaiati si sovrappongono parzialmente, condividendo una coppia di elettroni con spin opposti.
Più è grande la sovrapposizione degli orbitali, più forte è il legame e più stabile è la molecola. È come due cerchi che si intersecano: maggiore è l'area di intersezione, più forte è il "collegamento".
Nell'idrogeno (H₂), i due orbitali 1s si sovrappongono e gli elettroni hanno maggiori probabilità di trovarsi nello spazio tra i due nuclei. Questo crea il legame!
Esempi più complessi: nel fluoro (F₂) si sovrappongono due orbitali 2p con elettroni spaiati, mentre nell'acido fluoridrico (HF) si sovrappongono l'orbitale 1s dell'idrogeno e l'orbitale 2p del fluoro.
⚛️ Concetto chiave: I legami chimici nascono dalla "collaborazione" tra orbitali atomici che si sovrappongono per condividere elettroni!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
Simona Nardulli
@simonanardulli
I legami chimici sono il "collante" che tiene insieme gli atomi per formare le molecole. Gli atomi si uniscono perché da soli sono energeticamente instabili, e legandosi raggiungono uno stato più stabile liberando energia.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Sai perché gli atomi si uniscono tra loro? La risposta è semplice: sono instabili energeticamente quando sono da soli! Quando si legano, liberano energia e diventano più stabili, seguendo il principio dell'energia potenziale minima.
L'energia di legame è la quantità di energia che devi fornire per spezzare un legame chimico. Si misura in KJ/mol e ti dice quanto è forte un legame: più energia serve per romperlo, più il legame è stabile e resistente.
Solo gli elettroni di valenza partecipano ai legami chimici. La regola dell'ottetto di Lewis spiega che gli atomi sono particolarmente stabili quando hanno 8 elettroni nel guscio esterno (tranne idrogeno, litio e berillio che preferiscono 2 elettroni come l'elio).
💡 Ricorda: La forza del legame dipende dalla differenza di elettronegatività tra gli atomi: Δ ≤ 0,4 = covalente puro; 0,4 < Δ ≤ 1,9 = covalente polare; Δ > 1,9 = ionico.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Immagina un metallo generoso che cede elettroni e un non metallo avido che li accetta: ecco come nasce il legame ionico! I due atomi diventano ioni con cariche opposte che si attraggono grazie alla forza elettrostatica.
Gli ioni non rimangono isolati ma formano un reticolo cristallino, una struttura ordinata e ripetitiva dove ogni ione è circondato da ioni di carica opposta. È come un puzzle tridimensionale perfettamente organizzato!
I metalli dei gruppi I, II e III tendono a perdere elettroni (diventando ioni positivi), mentre i non metalli dei gruppi VI, VII e VIII li acquistano (diventando ioni negativi). I metalli di transizione come ferro e argento possono perdere quantità diverse di elettroni.
I composti ionici hanno caratteristiche distintive: sono solidi a temperatura ambiente, hanno punti di fusione elevati e conducono elettricità quando sono sciolti in acqua (ma non da solidi, perché gli ioni sono "bloccati" nel reticolo).
⚡ Curiosità: L'elettricità nei composti ionici viaggia attraverso il movimento degli ioni, non degli elettroni come nei metalli!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Nel mondo dei metalli succede qualcosa di affascinante: si forma una nube elettronica dove gli elettroni più esterni si muovono liberamente! È come avere una "piscina" di elettroni condivisa tra tutti gli atomi metallici.
Gli ioni metallici positivi si dispongono in modo ordinato formando un reticolo cristallino, mentre gli elettroni mobili li circondano creando una struttura compatta che riduce al minimo gli spazi vuoti.
Questa particolare struttura spiega le proprietà tipiche dei metalli: conducibilità elettrica e termica elevata proprio perché gli elettroni sono già in movimento e possono trasportare facilmente energia.
La forza del legame metallico varia lungo un periodo della tavola periodica, influenzando proprietà come durezza e punto di fusione dei diversi metalli.
🔧 Applicazione pratica: La mobilità degli elettroni nei metalli è il principio che rende possibili tutti i circuiti elettrici che usi ogni giorno!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Quando due non metalli si incontrano, non si "rubano" elettroni come nel legame ionico: li condividono! Questo è il legame covalente, dove gli elettroni appartengono a entrambi gli atomi contemporaneamente.
Puoi avere legami covalenti multipli: doppi o tripli, che sono più corti e più forti dei legami singoli. Esempi comuni sono O₂, N₂ e CO₂. Più legami ci sono, più energia serve per separare gli atomi!
Esistono due tipi principali: il legame covalente puro (tra atomi identici) e il legame covalente polare (tra atomi diversi). Nel secondo caso si forma un dipolo con un polo parzialmente positivo e uno negativo.
La polarità dipende dalla differenza di elettronegatività: l'atomo più elettronegativo attira di più gli elettroni condivisi, creando quella separazione di cariche che chiamiamo dipolo.
🧪 Esempi quotidiani: L'acqua (H₂O), l'ammoniaca (NH₃) e il metano (CH₄) sono tutti composti con legami covalenti che usi nella vita di tutti i giorni!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Hai mai sentito parlare di atomi "generosi" che donano una coppia di elettroni già completa? È esattamente quello che succede nel legame covalente dativo! Un atomo che ha già raggiunto l'ottetto dona una coppia di elettroni a un altro atomo.
Si indica con una freccia (→) che va dal donatore all'accettore. La particolarità è che entrambi gli elettroni del legame provengono da un solo atomo, non uno per ciascuno come nel covalente normale.
Esempi tipici sono gli acidi del cloro: HClO (acido ipocloroso), HClO₂ (acido cloroso), HClO₃ (acido clorico) e HClO₄ (acido perclorico).
I composti con legami dativi si chiamano complessi o composti di coordinazione: sono formati da un metallo centrale circondato da atomi donatori chiamati "leganti", mentre il metallo è detto "coordinante".
🎯 Trucco per ricordare: Nel legame dativo c'è sempre un "donatore" generoso e un "accettore" bisognoso - come prestare gli appunti a un compagno!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Scrivere le formule di struttura è come risolvere un puzzle: devi seguire alcune regole precise! Prima di tutto, metti al centro l'atomo più elettronegativo (eccetto l'idrogeno, che fa sempre eccezione).
Ogni atomo ha un numero preferito di legami: l'idrogeno forma sempre 1 legame, il carbonio 4, l'azoto 3 e l'ossigeno 2. È come se ognuno avesse la sua "firma" chimica!
Completa sempre gli ottetti di tutti gli atomi intorno all'atomo centrale. Gli atomi coinvolti nei legami multipli sono principalmente C, N, O e S.
Il trucco è considerare prima i legami singoli per soddisfare le esigenze base di ogni atomo, poi aggiungere legami multipli se necessario per completare gli ottetti.
✏️ Strategia di studio: Esercitati partendo dalle molecole più semplici come H₂O e CH₄, poi passa gradualmente a quelle più complesse!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
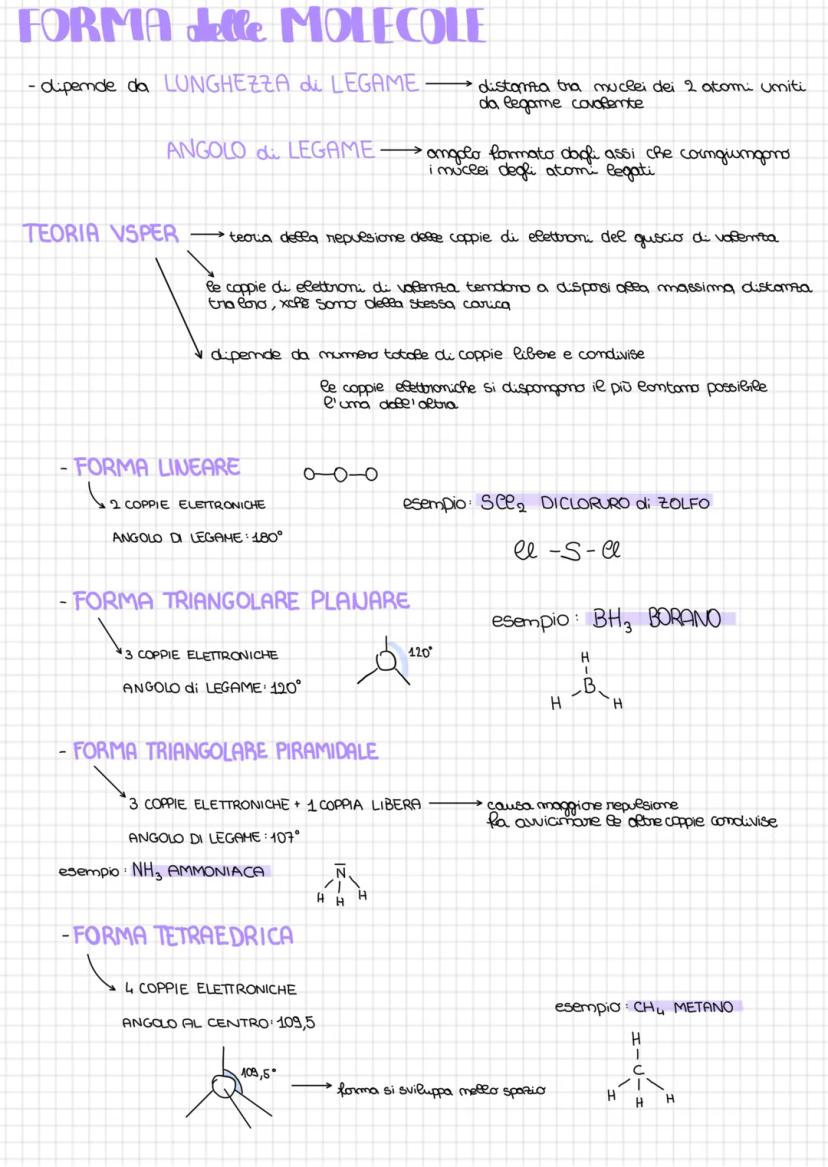
Le molecole non sono piatte come le disegniamo sul foglio: hanno forme tridimensionali precise! La forma dipende dalla lunghezza di legame (distanza tra i nuclei) e dall'angolo di legame tra gli assi che collegano i nuclei.
La teoria VSEPR spiega tutto: le coppie di elettroni si respingono perché hanno la stessa carica, quindi si dispongono alla massima distanza possibile. È come persone che cercano di stare il più lontano possibile in una stanza!
Ecco le forme principali: lineare (2 coppie, 180°), triangolare piana (3 coppie, 120°), tetraedrica (4 coppie, 109,5°). L'ammoniaca (NH₃) ha forma piramidale (107°) perché ha una coppia libera che "spinge" di più.
L'acqua (H₂O) ha forma piegata con angolo di 104,5° perché le sue due coppie libere esercitano una repulsione extra forte sulle coppie condivise.
🏗️ Visualizza: Immagina gli elettroni come magneti con la stessa polarità che si respingono - questo ti aiuterà a capire le forme molecolari!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
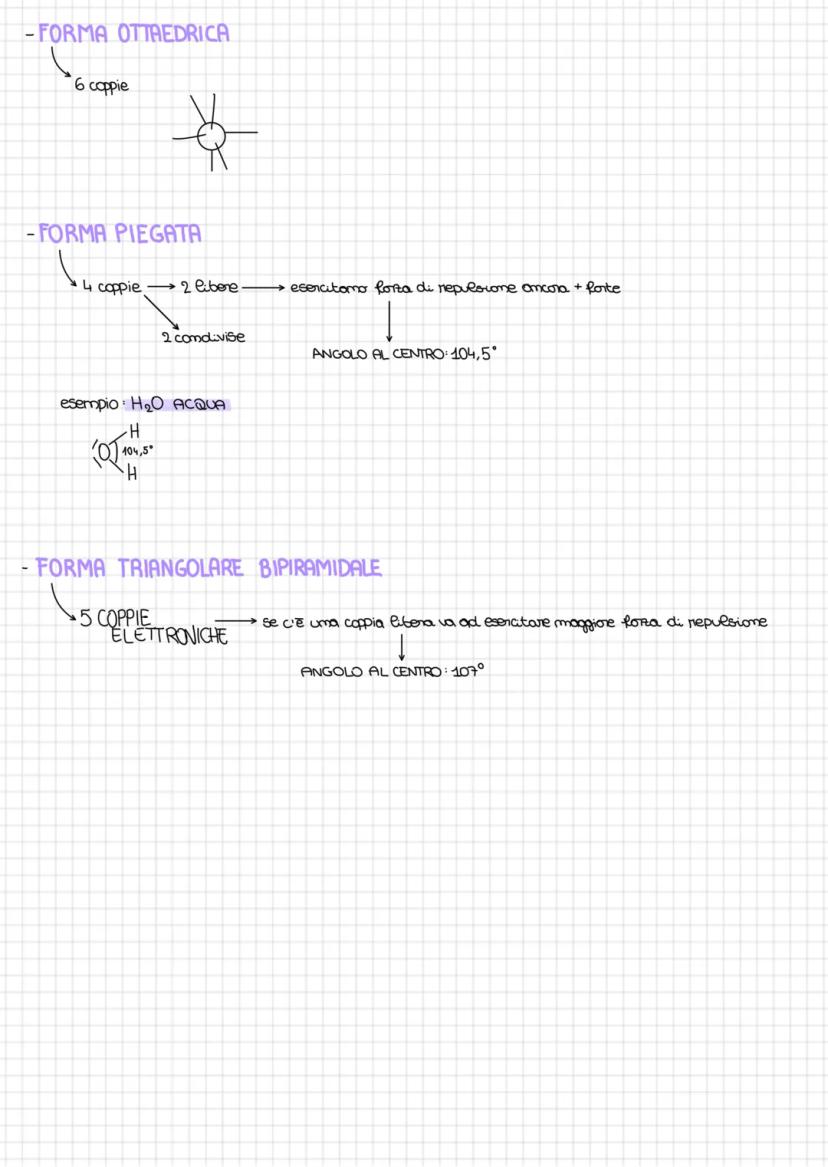
Oltre alle forme base, esistono geometrie più complesse! La forma ottaedrica si ha con 6 coppie elettroniche, mentre la forma triangolare bipiramidale coinvolge 5 coppie con angolo di 107°.
Quando hai coppie libere, ricorda che esercitano sempre una forza di repulsione più forte delle coppie condivise. Questo "spinge" gli altri elettroni modificando gli angoli di legame.
La forma piegata dell'acqua (H₂O) con i suoi 104,5° è un perfetto esempio di come 2 coppie libere possano influenzare drasticamente la geometria molecolare.
🔍 Osservazione: Le coppie libere sono come "pesi invisibili" che modificano la forma delle molecole anche se non le vediamo nelle formule!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
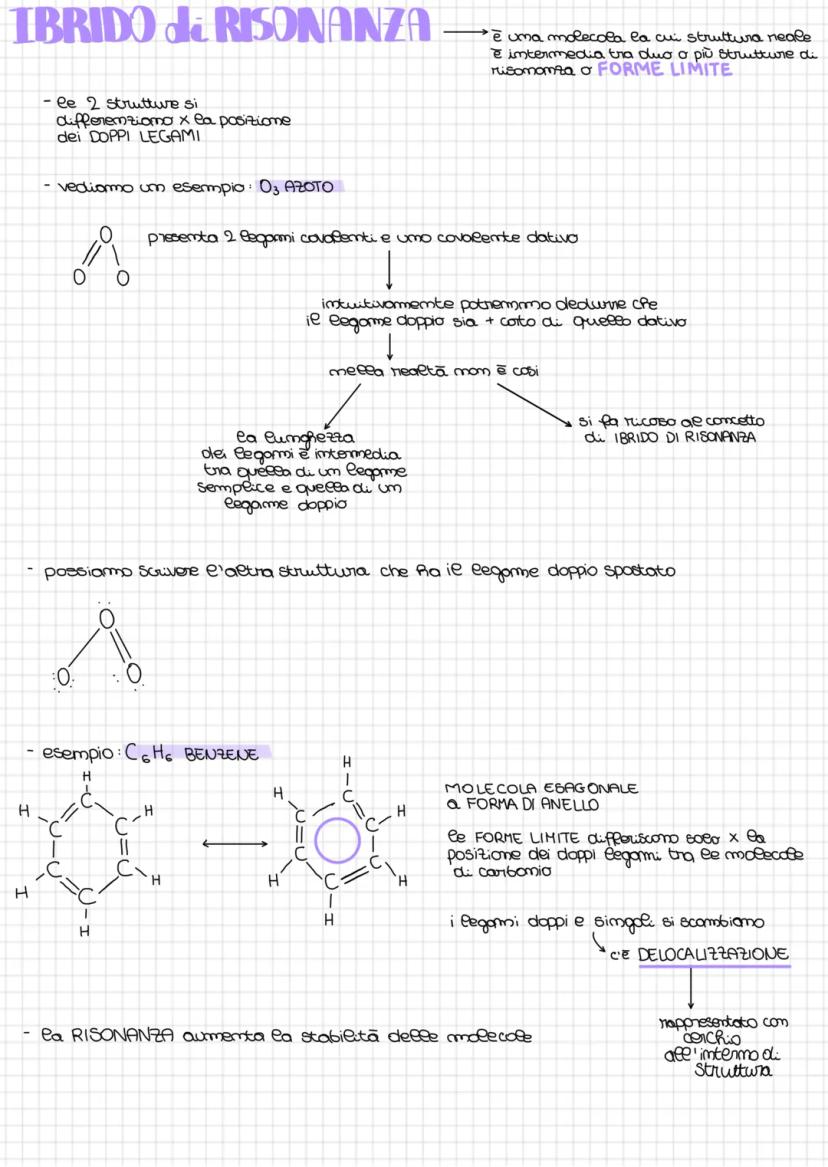
Alcune molecole sono come "camaleoni" chimici: la loro struttura reale è intermedia tra due o più forme limite! Questo fenomeno si chiama ibrido di risonanza.
Prendiamo l'ozono (O₃): teoricamente dovrebbe avere un legame doppio e uno dativo di lunghezze diverse, ma in realtà entrambi i legami hanno la stessa lunghezza intermedia. I doppi legami si "scambiano" continuamente posizione!
Il benzene (C₆H₆) è l'esempio più famoso: è una molecola esagonale dove i legami doppi e singoli tra i carboni si delocalizzano. Si rappresenta con un cerchio all'interno dell'esagono per indicare questa delocalizzazione.
La risonanza aumenta la stabilità delle molecole perché gli elettroni sono distribuiti su una superficie maggiore, come spalmare il peso su una base più ampia.
🎨 Analogia: È come un disegno che cambia continuamente tra due versioni, ma quello che vedi è sempre una via di mezzo tra le due!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Linus Pauling ha ideato la teoria VB per spiegare come si formano concretamente i legami. L'idea è che gli orbitali atomici contenenti elettroni spaiati si sovrappongono parzialmente, condividendo una coppia di elettroni con spin opposti.
Più è grande la sovrapposizione degli orbitali, più forte è il legame e più stabile è la molecola. È come due cerchi che si intersecano: maggiore è l'area di intersezione, più forte è il "collegamento".
Nell'idrogeno (H₂), i due orbitali 1s si sovrappongono e gli elettroni hanno maggiori probabilità di trovarsi nello spazio tra i due nuclei. Questo crea il legame!
Esempi più complessi: nel fluoro (F₂) si sovrappongono due orbitali 2p con elettroni spaiati, mentre nell'acido fluoridrico (HF) si sovrappongono l'orbitale 1s dell'idrogeno e l'orbitale 2p del fluoro.
⚛️ Concetto chiave: I legami chimici nascono dalla "collaborazione" tra orbitali atomici che si sovrappongono per condividere elettroni!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
22
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS