La chimica è ovunque intorno a te! Studia la materia... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
607
•
Aggiornato Apr 5, 2026
•
elle tortelli
@elletortelli_oogm
La chimica è ovunque intorno a te! Studia la materia... Mostra di più
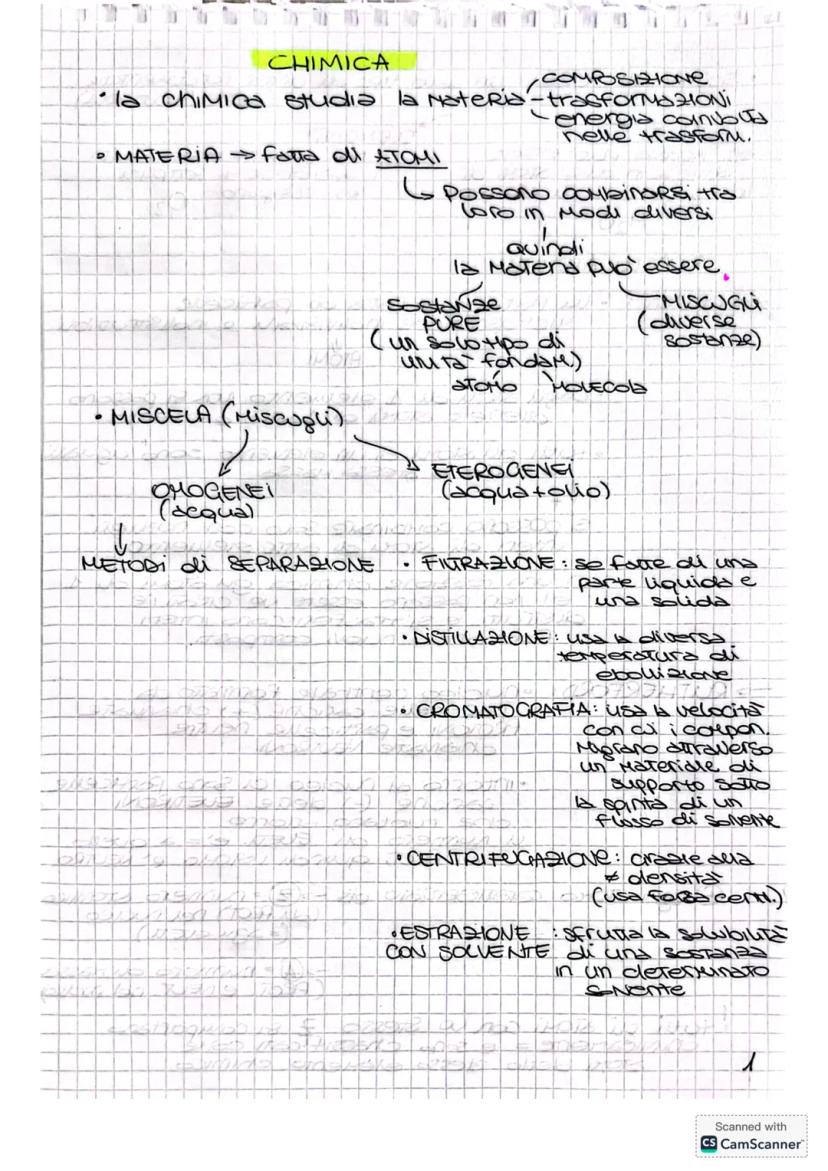








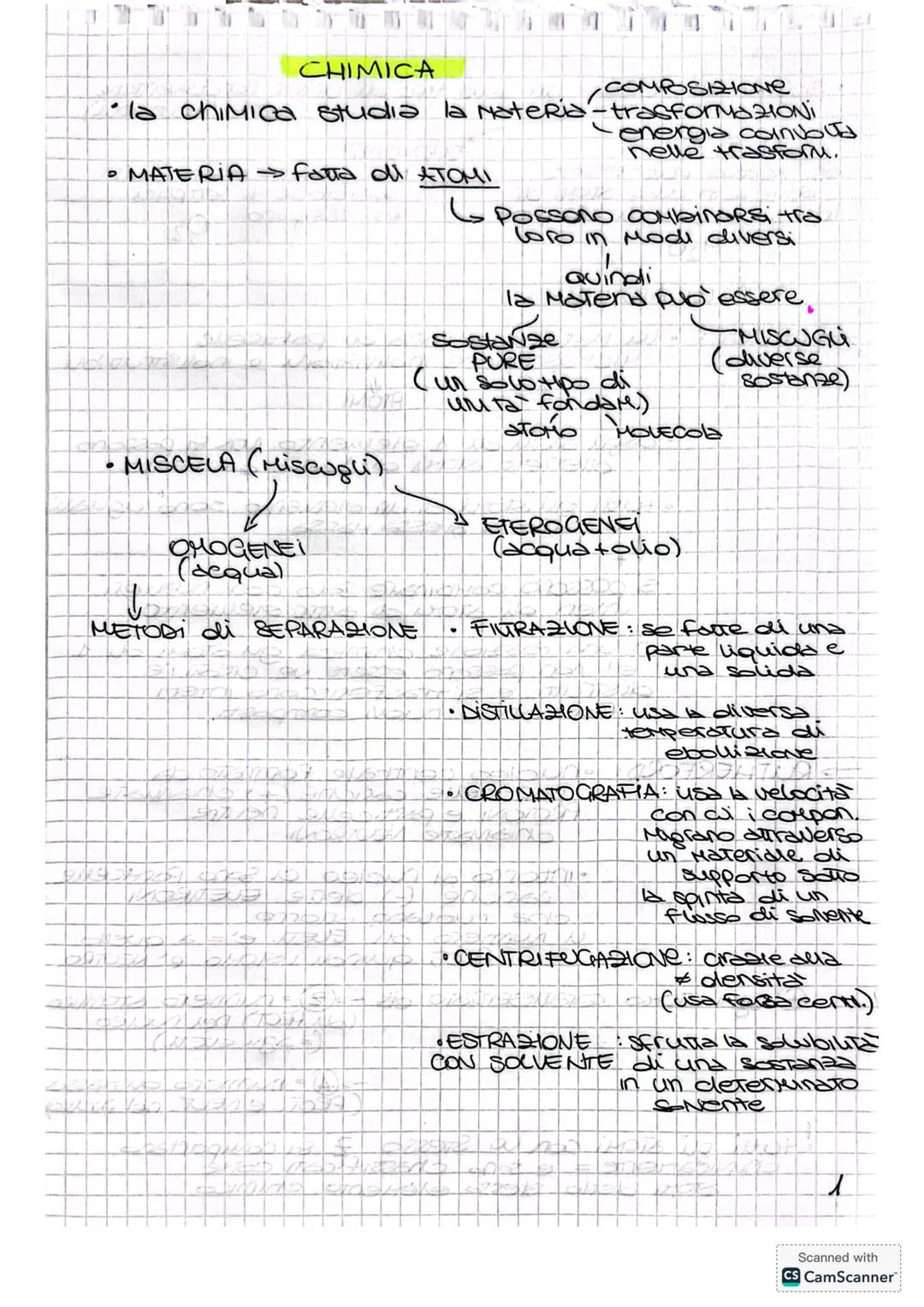
Tutto quello che vedi è fatto di atomi - dalle gocce d'acqua al tuo smartphone. La materia si divide principalmente in due categorie: le sostanze pure (un solo tipo di componente) e le miscele (più sostanze mescolate insieme).
Le miscele possono essere omogenee (come l'acqua salata, dove non distingui i componenti) o eterogenee (come acqua e olio, che rimangono separati). Quando devi separare i componenti di una miscela, hai diversi trucchi a disposizione.
I metodi di separazione sfruttano le diverse proprietà delle sostanze. La filtrazione separa solidi da liquidi, la distillazione usa le diverse temperature di ebollizione, e la centrifugazione sfrutta la densità. La cromatografia è come una gara di velocità tra molecole!
💡 Ricorda: Ogni metodo di separazione sfrutta una proprietà fisica diversa - temperatura, dimensione, densità o velocità di movimento.

Le sostanze pure si dividono in elementi (come l'ossigeno O₂, che non puoi scomporre ulteriormente) e composti (come l'acqua H₂O, formata da idrogeno e ossigeno). Gli elementi sono i mattoncini base di tutto!
Dalton per primo immaginò gli atomi come palline indivisibili e indistruttibili. Secondo lui, tutti gli atomi dello stesso elemento sono identici e si combinano sempre in proporzioni fisse - un'idea geniale per l'epoca!
Rutherford scoprì che l'atomo non è pieno: c'è un nucleo centrale con protoni (+) e neutroni, mentre gli elettroni (-) girano intorno. Il numero di protoni ed elettroni è uguale, quindi l'atomo è neutro.
Ogni elemento ha un numero atomico (Z) che indica i protoni nel nucleo. Il numero di massa (A) conta protoni più neutroni. Questi numeri sono come la carta d'identità di ogni atomo!
💡 Trucco per ricordare: Z = Protoni = Elettroni (in un atomo neutro), A = Protoni + Neutroni

Quando un atomo perde o acquista elettroni, diventa uno ione. Se perde elettroni diventa positivo (catione), se li acquista diventa negativo (anione). È come perdere o guadagnare soldi - cambia il tuo "saldo"!
Bohr migliorò il modello atomico introducendo le orbite stazionarie. Gli elettroni si muovono in orbite fisse senza perdere energia, come i pianeti intorno al Sole. Più l'orbita è lontana dal nucleo, più energia ha l'elettrone.
Il passaggio tra orbite avviene tramite assorbimento o emissione di fotoni. Quando un elettrone "salta" da un'orbita all'altra, l'atomo scambia energia con l'ambiente circostante.
Il modello ondulatorio moderno è più preciso: gli elettroni non seguono orbite fisse ma si comportano come nuvole elettroniche. Gli orbitali sono le regioni dove è più probabile trovarli.
💡 Pensaci così: Gli elettroni sono come api intorno all'alveare - sai dove è probabile trovarle, ma non la loro posizione esatta!

Heisenberg dimostrò che è impossibile conoscere contemporaneamente posizione e velocità di una particella. Per gli elettroni questo significa che possiamo solo calcolare la probabilità di trovarli in una certa zona.
Un orbitale è definito da una funzione d'onda che dipende da quattro numeri quantici. È come avere le coordinate GPS di una regione nello spazio atomico!
I numeri quantici sono: n (livello energetico principale), l (forma dell'orbitale), m (orientamento nello spazio) e s (spin dell'elettrone). Ogni orbitale può contenere massimo due elettroni con spin opposto.
Pensalo come un sistema di indirizzi: il numero quantico principale è la strada, quello angolare è il tipo di edificio, quello magnetico è l'orientamento, e lo spin indica se l'elettrone "gira" in senso orario o antiorario.
💡 Regola d'oro: Ogni orbitale ha un "indirizzo" unico dato da n, l, m e può ospitare al massimo 2 elettroni con spin opposto.

La configurazione elettronica descrive come gli elettroni si distribuiscono negli orbitali. Segue tre regole fondamentali che determinano l'"ordine di riempimento" degli orbitali.
Il Principio di Aufbau dice che gli elettroni occupano prima gli orbitali a energia più bassa (1s, 2s, 2p, 3s...). Il Principio di Esclusione di Pauli stabilisce che in ogni orbitale ci possono essere al massimo due elettroni con spin opposto.
La Regola di Hund è come trovare posto in autobus: negli orbitali della stessa energia, gli elettroni si siedono prima da soli, poi si accoppiano. Questo minimizza la repulsione elettronica.
Per scrivere la configurazione elettronica, prendi il numero atomico (numero di elettroni) e riempi gli orbitali seguendo lo schema energetico. È come compilare una lista in ordine di priorità!
💡 Schema da ricordare: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p... Segui sempre l'ordine crescente di energia!
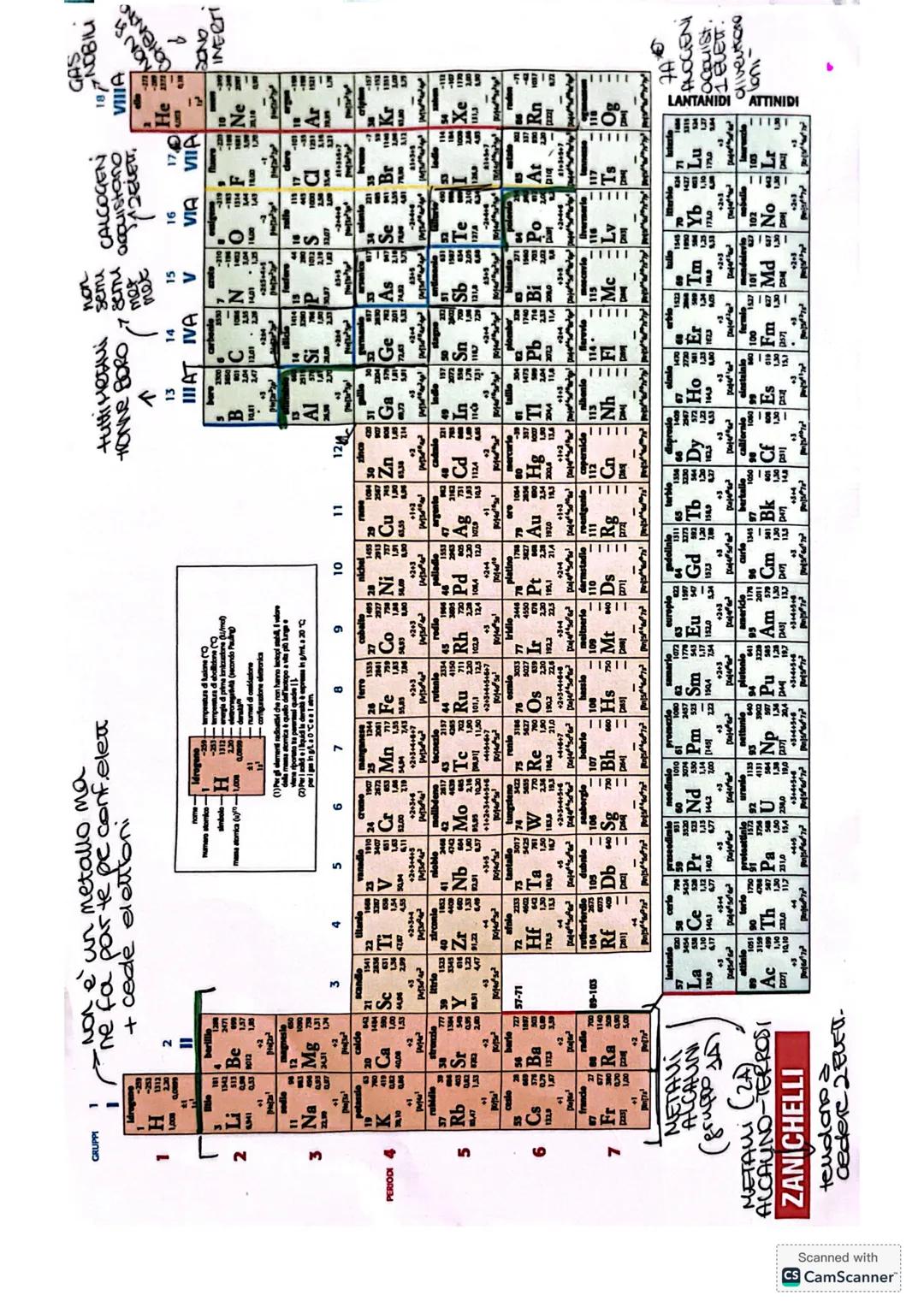
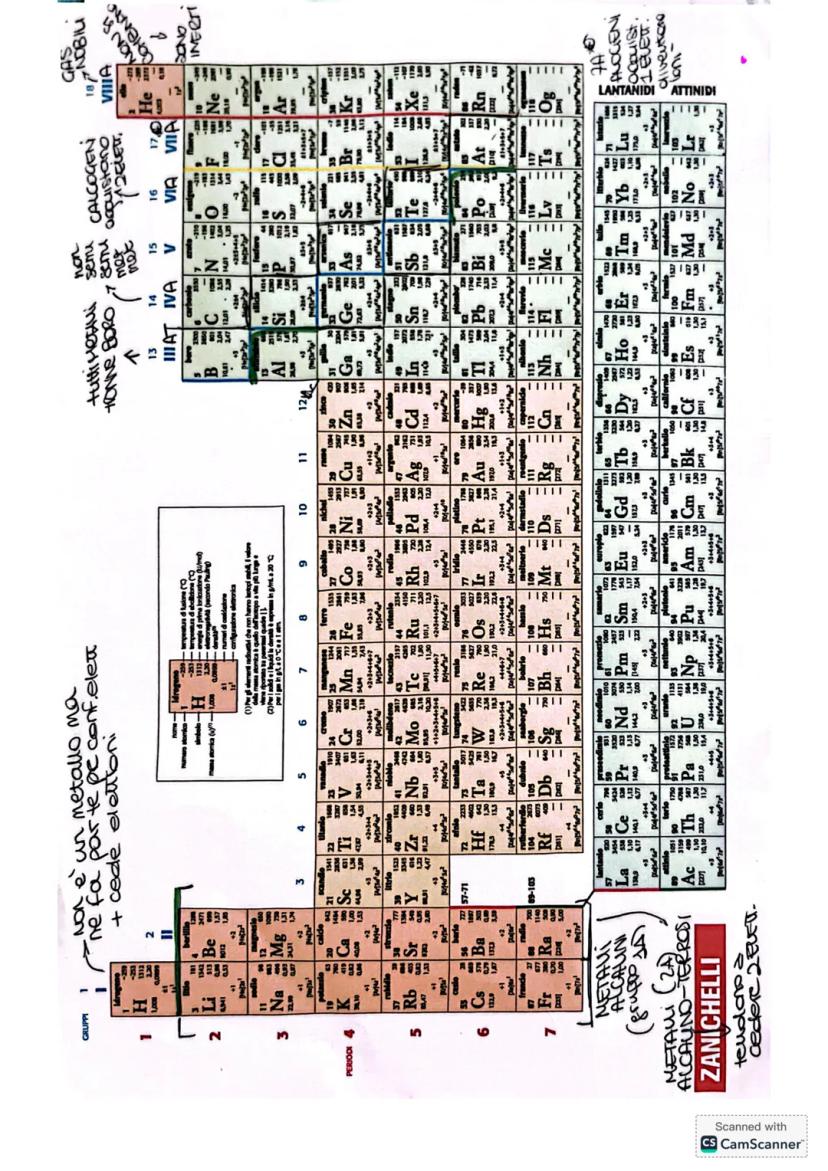
La Tavola Periodica organizza tutti gli elementi in base alle loro proprietà. Le colonne verticali sono i gruppi (elementi con caratteristiche simili), le righe orizzontali sono i periodi (stesso numero di livelli elettronici).
La tavola si divide in tre zone principali: metalli a sinistra, non metalli a destra, e semimetalli lungo la linea di separazione. Ogni zona ha proprietà caratteristiche specifiche.
I metalli sono malleabili, duttili, conducono elettricità e calore, e tendono a perdere elettroni formando ioni positivi. I non metalli hanno proprietà opposte e tendono ad acquistare elettroni.
La tavola può essere divisa in blocchi (s, p, d, f) in base al tipo di orbitale che si sta riempiendo. Gli elettroni di valenza (quelli esterni) determinano le proprietà chimiche di ogni elemento.
💡 Trucco utile: Il numero del gruppo indica quanti elettroni di valenza ha l'elemento - è la sua "firma chimica"!

Le proprietà periodiche cambiano in modo prevedibile lungo i periodi e i gruppi. L'elettronegatività misura quanto un atomo attira gli elettroni di legame - cresce da sinistra a destra e dal basso verso l'alto.
Il potenziale di ionizzazione è l'energia necessaria per "strappare" un elettrone all'atomo. L'affinità elettronica è l'energia liberata quando un atomo acquista un elettrone. Entrambe seguono trend opposti al raggio atomico.
Il raggio atomico diminuisce lungo il periodo (più protoni attraggono più forte) e aumenta lungo il gruppo (più livelli elettronici). È come gonfiare o sgonfiare un palloncino!
Questi trend ti permettono di prevedere il comportamento chimico degli elementi. Conoscendo la posizione nella tavola periodica, puoi indovinare molte proprietà senza memorizzarle!
💡 Memoria visiva: Elettronegatività e potenziale di ionizzazione crescono verso l'angolo in alto a destra (fluoro), il raggio atomico verso il basso a sinistra (cesio).

I legami chimici sono le forze che tengono uniti gli atomi. Gli atomi si legano per raggiungere una configurazione elettronica stabile, di solito con 8 elettroni nello strato esterno (regola dell'ottetto).
Esistono tre tipi principali di legami forti. Il legame ionico nasce dal trasferimento di elettroni tra un metallo e un non metallo, formando ioni di carica opposta che si attraggono (differenza di elettronegatività > 1,7).
Il legame covalente si forma quando due non metalli condividono una coppia di elettroni. Se la differenza di elettronegatività è < 1,7, gli elettroni sono condivisi più o meno equamente.
Il legame metallico è tipico dei metalli: gli elettroni di valenza formano una "nuvola elettronica" mobile che tiene uniti gli ioni metallici positivi. Questo spiega perché i metalli conducono elettricità!
💡 Regola pratica: Metallo + Non metallo = Ionico, Non metallo + Non metallo = Covalente, Metallo + Metallo = Metallico.

Nel legame covalente polarizzato, la coppia di elettroni non è equidistante tra i due atomi. L'atomo più elettronegativo attira di più gli elettroni, creando cariche parziali .
Il legame covalente dativo è particolare: entrambi gli elettroni condivisi provengono dallo stesso atomo. È come prestare una coppia di elettroni a un atomo "povero".
Le forze di Van der Waals sono interazioni deboli tra molecole. Includono forze dipolo-dipolo, dipolo indotto, e forze di London (responsabili dell'attrazione tra molecole apolari).
L'interazione ione-dipolo spiega perché il sale si scioglie in acqua: gli ioni Na+ e Cl- vengono "circondati" e stabilizzati dalle molecole d'acqua polari, indebolendo il legame ionico del cristallo.
💡 Ricorda: Le forze intermolecolari sono più deboli dei legami chimici, ma determinano proprietà come punto di ebollizione e solubilità.

I legami a idrogeno sono forze intermolecolari particolarmente forti. Si formano quando l'idrogeno è legato a ossigeno, azoto o fluoro e interagisce con atomi elettronegativi di molecole vicine.
Il numero di ossidazione (n.o.) indica la carica che assumerebbe un atomo se tutti gli elettroni di legame andassero all'elemento più elettronegativo. È fondamentale per scrivere formule e bilanciare reazioni.
Regole base per il n.o.: elementi liberi = 0, ossigeno = -2 , idrogeno = +1 . La somma dei n.o. in un composto neutro deve essere zero.
I composti si classificano in binari (2 elementi), ternari (3 elementi) o quaternari (4 elementi). Nelle formule, l'elemento meno elettronegativo va sempre davanti al più elettronegativo.
💡 Trucco per il n.o.: Parti dagli elementi con n.o. fisso (O, H), poi calcola gli altri per fare tornare la somma a zero!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
elle tortelli
@elletortelli_oogm
La chimica è ovunque intorno a te! Studia la materia e le sue trasformazioni, partendo dall'unità più piccola: gli atomi. Capire questi concetti ti darà le basi per comprendere tutto quello che succede nel mondo microscopico.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Tutto quello che vedi è fatto di atomi - dalle gocce d'acqua al tuo smartphone. La materia si divide principalmente in due categorie: le sostanze pure (un solo tipo di componente) e le miscele (più sostanze mescolate insieme).
Le miscele possono essere omogenee (come l'acqua salata, dove non distingui i componenti) o eterogenee (come acqua e olio, che rimangono separati). Quando devi separare i componenti di una miscela, hai diversi trucchi a disposizione.
I metodi di separazione sfruttano le diverse proprietà delle sostanze. La filtrazione separa solidi da liquidi, la distillazione usa le diverse temperature di ebollizione, e la centrifugazione sfrutta la densità. La cromatografia è come una gara di velocità tra molecole!
💡 Ricorda: Ogni metodo di separazione sfrutta una proprietà fisica diversa - temperatura, dimensione, densità o velocità di movimento.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Le sostanze pure si dividono in elementi (come l'ossigeno O₂, che non puoi scomporre ulteriormente) e composti (come l'acqua H₂O, formata da idrogeno e ossigeno). Gli elementi sono i mattoncini base di tutto!
Dalton per primo immaginò gli atomi come palline indivisibili e indistruttibili. Secondo lui, tutti gli atomi dello stesso elemento sono identici e si combinano sempre in proporzioni fisse - un'idea geniale per l'epoca!
Rutherford scoprì che l'atomo non è pieno: c'è un nucleo centrale con protoni (+) e neutroni, mentre gli elettroni (-) girano intorno. Il numero di protoni ed elettroni è uguale, quindi l'atomo è neutro.
Ogni elemento ha un numero atomico (Z) che indica i protoni nel nucleo. Il numero di massa (A) conta protoni più neutroni. Questi numeri sono come la carta d'identità di ogni atomo!
💡 Trucco per ricordare: Z = Protoni = Elettroni (in un atomo neutro), A = Protoni + Neutroni

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Quando un atomo perde o acquista elettroni, diventa uno ione. Se perde elettroni diventa positivo (catione), se li acquista diventa negativo (anione). È come perdere o guadagnare soldi - cambia il tuo "saldo"!
Bohr migliorò il modello atomico introducendo le orbite stazionarie. Gli elettroni si muovono in orbite fisse senza perdere energia, come i pianeti intorno al Sole. Più l'orbita è lontana dal nucleo, più energia ha l'elettrone.
Il passaggio tra orbite avviene tramite assorbimento o emissione di fotoni. Quando un elettrone "salta" da un'orbita all'altra, l'atomo scambia energia con l'ambiente circostante.
Il modello ondulatorio moderno è più preciso: gli elettroni non seguono orbite fisse ma si comportano come nuvole elettroniche. Gli orbitali sono le regioni dove è più probabile trovarli.
💡 Pensaci così: Gli elettroni sono come api intorno all'alveare - sai dove è probabile trovarle, ma non la loro posizione esatta!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Heisenberg dimostrò che è impossibile conoscere contemporaneamente posizione e velocità di una particella. Per gli elettroni questo significa che possiamo solo calcolare la probabilità di trovarli in una certa zona.
Un orbitale è definito da una funzione d'onda che dipende da quattro numeri quantici. È come avere le coordinate GPS di una regione nello spazio atomico!
I numeri quantici sono: n (livello energetico principale), l (forma dell'orbitale), m (orientamento nello spazio) e s (spin dell'elettrone). Ogni orbitale può contenere massimo due elettroni con spin opposto.
Pensalo come un sistema di indirizzi: il numero quantico principale è la strada, quello angolare è il tipo di edificio, quello magnetico è l'orientamento, e lo spin indica se l'elettrone "gira" in senso orario o antiorario.
💡 Regola d'oro: Ogni orbitale ha un "indirizzo" unico dato da n, l, m e può ospitare al massimo 2 elettroni con spin opposto.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La configurazione elettronica descrive come gli elettroni si distribuiscono negli orbitali. Segue tre regole fondamentali che determinano l'"ordine di riempimento" degli orbitali.
Il Principio di Aufbau dice che gli elettroni occupano prima gli orbitali a energia più bassa (1s, 2s, 2p, 3s...). Il Principio di Esclusione di Pauli stabilisce che in ogni orbitale ci possono essere al massimo due elettroni con spin opposto.
La Regola di Hund è come trovare posto in autobus: negli orbitali della stessa energia, gli elettroni si siedono prima da soli, poi si accoppiano. Questo minimizza la repulsione elettronica.
Per scrivere la configurazione elettronica, prendi il numero atomico (numero di elettroni) e riempi gli orbitali seguendo lo schema energetico. È come compilare una lista in ordine di priorità!
💡 Schema da ricordare: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p... Segui sempre l'ordine crescente di energia!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La Tavola Periodica organizza tutti gli elementi in base alle loro proprietà. Le colonne verticali sono i gruppi (elementi con caratteristiche simili), le righe orizzontali sono i periodi (stesso numero di livelli elettronici).
La tavola si divide in tre zone principali: metalli a sinistra, non metalli a destra, e semimetalli lungo la linea di separazione. Ogni zona ha proprietà caratteristiche specifiche.
I metalli sono malleabili, duttili, conducono elettricità e calore, e tendono a perdere elettroni formando ioni positivi. I non metalli hanno proprietà opposte e tendono ad acquistare elettroni.
La tavola può essere divisa in blocchi (s, p, d, f) in base al tipo di orbitale che si sta riempiendo. Gli elettroni di valenza (quelli esterni) determinano le proprietà chimiche di ogni elemento.
💡 Trucco utile: Il numero del gruppo indica quanti elettroni di valenza ha l'elemento - è la sua "firma chimica"!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Le proprietà periodiche cambiano in modo prevedibile lungo i periodi e i gruppi. L'elettronegatività misura quanto un atomo attira gli elettroni di legame - cresce da sinistra a destra e dal basso verso l'alto.
Il potenziale di ionizzazione è l'energia necessaria per "strappare" un elettrone all'atomo. L'affinità elettronica è l'energia liberata quando un atomo acquista un elettrone. Entrambe seguono trend opposti al raggio atomico.
Il raggio atomico diminuisce lungo il periodo (più protoni attraggono più forte) e aumenta lungo il gruppo (più livelli elettronici). È come gonfiare o sgonfiare un palloncino!
Questi trend ti permettono di prevedere il comportamento chimico degli elementi. Conoscendo la posizione nella tavola periodica, puoi indovinare molte proprietà senza memorizzarle!
💡 Memoria visiva: Elettronegatività e potenziale di ionizzazione crescono verso l'angolo in alto a destra (fluoro), il raggio atomico verso il basso a sinistra (cesio).

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
I legami chimici sono le forze che tengono uniti gli atomi. Gli atomi si legano per raggiungere una configurazione elettronica stabile, di solito con 8 elettroni nello strato esterno (regola dell'ottetto).
Esistono tre tipi principali di legami forti. Il legame ionico nasce dal trasferimento di elettroni tra un metallo e un non metallo, formando ioni di carica opposta che si attraggono (differenza di elettronegatività > 1,7).
Il legame covalente si forma quando due non metalli condividono una coppia di elettroni. Se la differenza di elettronegatività è < 1,7, gli elettroni sono condivisi più o meno equamente.
Il legame metallico è tipico dei metalli: gli elettroni di valenza formano una "nuvola elettronica" mobile che tiene uniti gli ioni metallici positivi. Questo spiega perché i metalli conducono elettricità!
💡 Regola pratica: Metallo + Non metallo = Ionico, Non metallo + Non metallo = Covalente, Metallo + Metallo = Metallico.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Nel legame covalente polarizzato, la coppia di elettroni non è equidistante tra i due atomi. L'atomo più elettronegativo attira di più gli elettroni, creando cariche parziali .
Il legame covalente dativo è particolare: entrambi gli elettroni condivisi provengono dallo stesso atomo. È come prestare una coppia di elettroni a un atomo "povero".
Le forze di Van der Waals sono interazioni deboli tra molecole. Includono forze dipolo-dipolo, dipolo indotto, e forze di London (responsabili dell'attrazione tra molecole apolari).
L'interazione ione-dipolo spiega perché il sale si scioglie in acqua: gli ioni Na+ e Cl- vengono "circondati" e stabilizzati dalle molecole d'acqua polari, indebolendo il legame ionico del cristallo.
💡 Ricorda: Le forze intermolecolari sono più deboli dei legami chimici, ma determinano proprietà come punto di ebollizione e solubilità.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
I legami a idrogeno sono forze intermolecolari particolarmente forti. Si formano quando l'idrogeno è legato a ossigeno, azoto o fluoro e interagisce con atomi elettronegativi di molecole vicine.
Il numero di ossidazione (n.o.) indica la carica che assumerebbe un atomo se tutti gli elettroni di legame andassero all'elemento più elettronegativo. È fondamentale per scrivere formule e bilanciare reazioni.
Regole base per il n.o.: elementi liberi = 0, ossigeno = -2 , idrogeno = +1 . La somma dei n.o. in un composto neutro deve essere zero.
I composti si classificano in binari (2 elementi), ternari (3 elementi) o quaternari (4 elementi). Nelle formule, l'elemento meno elettronegativo va sempre davanti al più elettronegativo.
💡 Trucco per il n.o.: Parti dagli elementi con n.o. fisso (O, H), poi calcola gli altri per fare tornare la somma a zero!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
13
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS