configurazione elettronica, scaletta di riempimento e varie leggi.
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
7,624
•
Aggiornato Apr 19, 2026
•
configurazione elettronica, scaletta di riempimento e varie leggi.





Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
configurazione elettronica, scaletta di riempimento e varie leggi.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
185
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
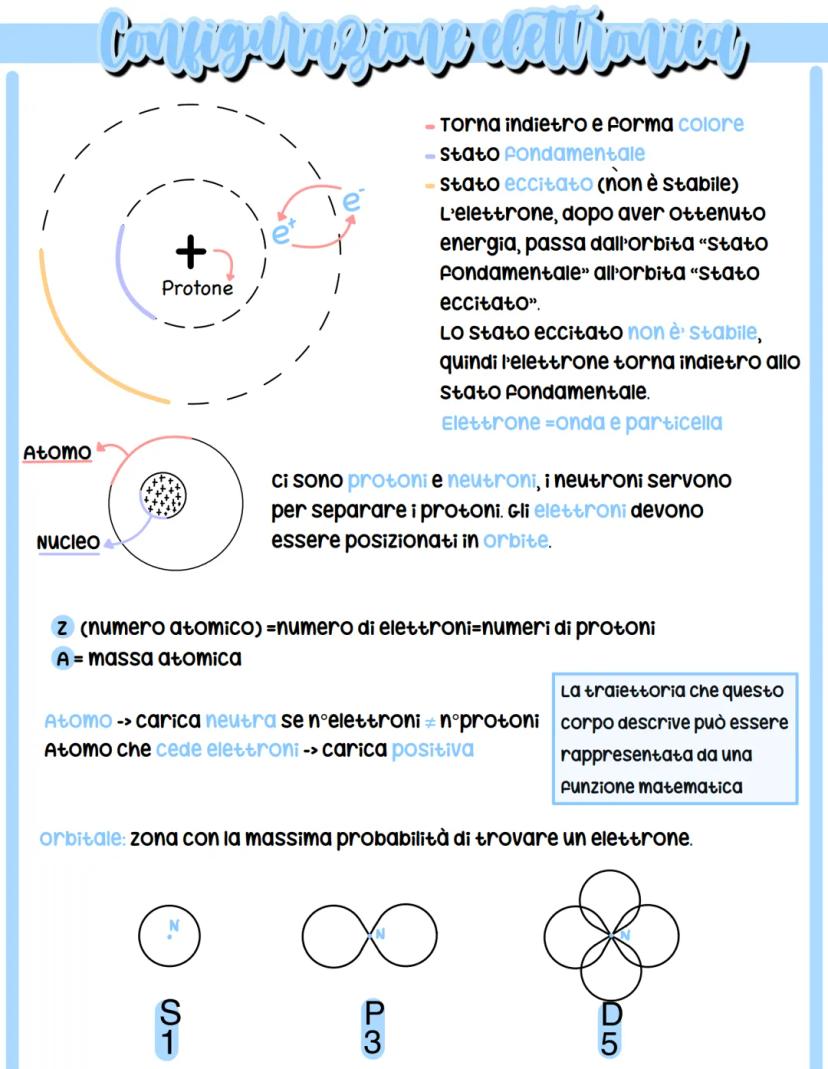
gli orbitali
È una mappa molto stilizzata. Spero possiate comprendere il testo. Se notate errori o avete altri suggerimenti, per favore fatemelo presente. Buono studio
Sintesi dell’argomento “Grandezze fisiche e misure”; definizione di: Grandezza Fisica, Sistema Internazionale, Unità di Misura, Notazione Scientifica, Massa, Peso, Temperatura, Calore, Lunghezza e Materia.
Legge di conservazione della massa; reazioni di sintesi, di combustione, di scambio semplice (o di spostamento); equazione ionica netta; resa di una reazione chimica; reazioni di ossidoriduzione
Reazioni chimiche e legami, numeri di ossidazione, composti dell'ossigeno (ossidi, anidridi, idrossidi, ossiacidi, ossoanioni, sali di ossiacidi), ossiacidi particolari, idracidi
Teorica dell’atomo di Dalton, Crookes, Thomson, Rutherford. Spettro elettromagnetico e teoria ondulatoria della luce
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS