Le reazioni redoxsono tra i processi chimici più importanti... Mostra di più
Reazioni Redox: Guida Completa con Esempi







Cos'è una reazione redox e il numero di ossidazione
Hai mai pensato a cosa succede quando accendi una candela o quando le piante fanno la fotosintesi? Sono tutte reazioni redox! Il nome viene da "riduzione" e "ossidazione", due processi che avvengono sempre insieme.
In una reazione redox, gli elettroni si spostano da un atomo all'altro. L'ossigeno è spesso il "colpevole" di questi spostamenti perché è molto elettronegativo (dopo il fluoro è il più "avido" di elettroni).
Il numero di ossidazione è come la "carta d'identità" di ogni atomo in un composto: ci dice che carica assume quando gli elettroni si spostano verso l'elemento più elettronegativo. Per esempio, nella combustione del carbonio: C(0) + O₂(0) → CO₂(+4)(-2), il carbonio passa da 0 a +4 perché perde elettroni.
💡 Ricorda: Tutti gli atomi neutri hanno numero di ossidazione 0, come punto di partenza!

Ossidazione e riduzione: chi fa cosa?
Prendiamo l'esempio della combustione del magnesio: 2Mg(0) + O₂(0) → 2MgO(+2)(-2). Qui succedono due cose simultanee che devi ricordare perfettamente.
L'ossidazione è quando un atomo perde elettroni e il suo numero di ossidazione aumenta. Il magnesio si ossida: Mg → Mg²⁺ + 2e⁻ .
La riduzione è quando un atomo acquista elettroni e il suo numero di ossidazione diminuisce. L'ossigeno si riduce: O + 2e⁻ → O²⁻ .
Quindi il magnesio è l'agente riducente (fa ridurre l'ossigeno) mentre l'ossigeno è l'agente ossidante (fa ossidare il magnesio). È come una danza: uno cede, l'altro riceve, sempre in coppia!
💡 Trucco: OIL RIG - Oxidation Involves Loss (of electrons), Reduction Involves Gain!

Come bilanciare le reazioni redox
Il bilanciamento delle reazioni redox può sembrare complicato, ma una volta capito il metodo diventa quasi automatico. L'importante è che il numero di elettroni persi sia uguale a quelli acquistati.
Il metodo della variazione del numero di ossidazione è il più semplice. Prendi la reazione: 2Na + 2H₂O → 2NaOH + H₂. Il sodio si ossida e l'idrogeno si riduce .
Per bilanciare, trova il minimo comune multiplo degli elettroni scambiati. Se uno perde 2 elettroni e l'altro ne acquista 1, dovrai mettere i coefficienti giusti per far coincidere tutto.
Nei casi particolari con più specie che si ossidano o riducono, somma tutti gli elettroni persi da una parte e tutti quelli acquistati dall'altra, poi bilancia come sempre.
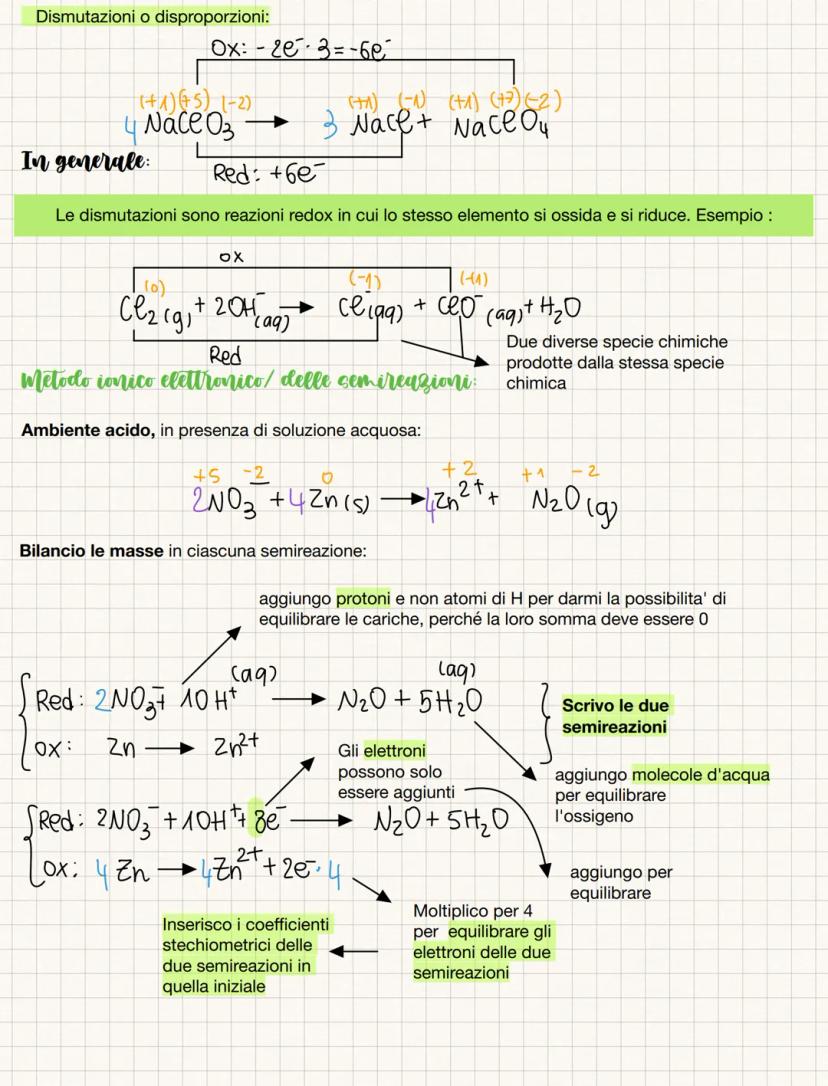
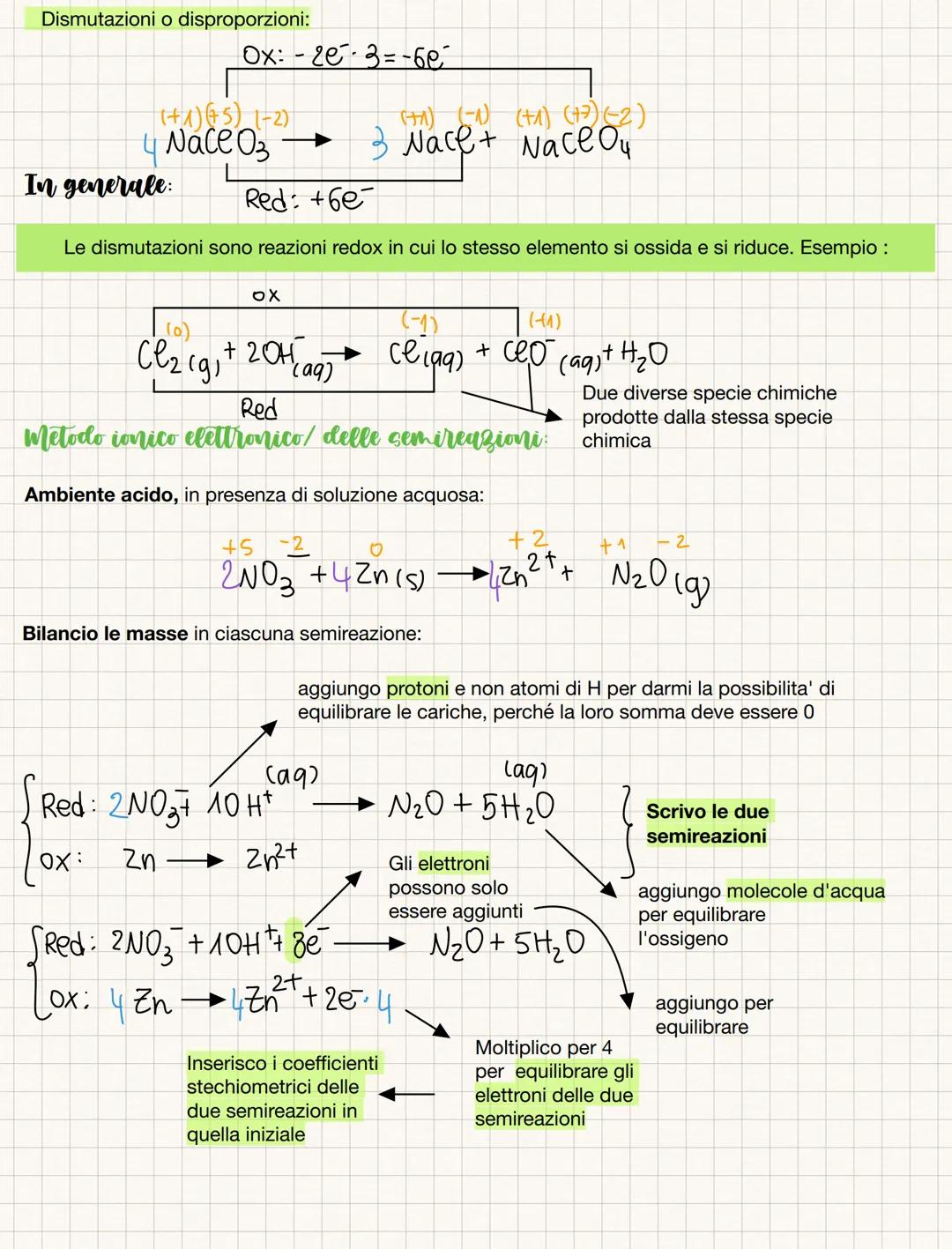
💡 Attenzione: Le dismutazioni sono reazioni speciali dove lo stesso elemento si ossida E si riduce contemporaneamente!

Il metodo ionico-elettronico
Quando lavori in soluzione acquosa, il metodo ionico-elettronico è più preciso perché considera la presenza di ioni. È perfetto per l'ambiente del laboratorio!
In ambiente acido, scrivi le due semireazioni separate. Per esempio: 2NO₃⁻ + 4Zn → 4Zn²⁺ + N₂O. Prima bilanci le masse aggiungendo H⁺ e H₂O dove serve, poi bilanci le cariche con gli elettroni.
La semireazione di riduzione: 2NO₃⁻ + 10H⁺ + 8e⁻ → N₂O + 5H₂O. La semireazione di ossidazione: 4Zn → 4Zn²⁺ + 8e⁻. Gli elettroni devono essere uguali nelle due semireazioni!
Infine, sommi tutto e semplifici le specie comuni. Il bello di questo metodo è che ti permette di gestire anche le reazioni più complesse con precisione.
💡 Suggerimento: Bilancia sempre prima le masse, poi le cariche con gli elettroni!
Ambiente basico e esempi pratici
Nell'ambiente basico il procedimento è simile a quello acido, ma alla fine aggiungi ioni OH⁻ per neutralizzare tutti gli H⁺ che hai usato, trasformandoli in H₂O.
Prendi l'esempio: 2ClO⁻ + Bi₂O₃ → 2Cl⁻ + 2BiO₃⁻. Dopo aver bilanciato come in ambiente acido, se hai 6H⁺, aggiungi 6OH⁻ da entrambe le parti per formare 6H₂O.
La regola d'oro è: il numero di ioni ossidrili che aggiungi deve essere uguale al numero più alto di protoni presenti. Poi semplifici le molecole d'acqua che si ripetono.
Ricorda che non devi per forza avere cariche neutre da entrambe le parti, basta che la somma delle cariche dei reagenti sia uguale a quella dei prodotti.
💡 Importante: In ambiente basico, aggiungi sempre OH⁻ da entrambe le parti della reazione!

Esercizi e applicazioni pratiche
Ora che conosci i metodi, è il momento di applicarli! Prendi l'esempio: MnO₄⁻ + SO₃²⁻ → SO₄²⁻ + Mn²⁺. Il manganese si riduce (+7 → +2) e lo zolfo si ossida (+4 → +6).
Le semireazioni sono: MnO₄⁻ + 8H⁺ + 5e⁻ → Mn²⁺ + 4H₂O e SO₃²⁻ + H₂O → SO₄²⁻ + 2H⁺ + 2e⁻. Per bilanciare gli elettroni, moltiplica la prima per 2 e la seconda per 5.
Il risultato finale è: 2MnO₄⁻ + 5SO₃²⁺ + 6H⁺ → 2Mn²⁺ + 5SO₄²⁻ + 3H₂O. Nota come alla fine hai semplificato gli H⁺ e le H₂O in eccesso.
La chiave del successo è fare sempre il controllo finale: verifica che gli atomi e le cariche siano bilanciati da entrambe le parti!
💡 Pro tip: Fai sempre la prova del nove controllando atomi e cariche alla fine!

Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: Ossidazione
9Chimica organica
Nomenclatura e proprietà di idrocarburi e alogenoderivati: ALCANI, ALCHENI, ALCHINI, IDROCARBURI AROMATICI, ALCOLI, FENOLI, ETERI, ALDEIDI, CHETONI, ACIDI CARBOSSILICI, SAPONI, ESTERI, AMMINE
I carboidrati
Monosaccaridi, disaccaridi e polisaccaridi
Idrocarburi alifatici e aliciclici: Alcani, cicloalcani, Alcheni, Alchini
Alcani, cicloalcani, Alcheni, Alchini con rispettive reazioni
Chimica, programma intero di quinto
Chimica Organica, Biomolecole, Matabolismo del glucosio, Ciclo di Krebs e Fosforilazione Ossidativa; Biochimica del corpo umano, accenni alla fotosintesi. Gli Acidi Nucleici e il DNA, Replicazione, Trascrizione e Traduzione.
Enzimi
Biochimica: gli enzimi - che cosa sono e funzione - specificità enzima - cofattori enzimatici - azione catalitica - attività enzimatica e regolazione
i carboidrati
appunti sui carboidrati: monosaccaridi, proiezioni di Fischer, proiezioni di Haworth, reazioni dei monosaccaridi, oligosaccaridi (lattosio, maltosio e saccarosio) e polisaccaridi (amido, glicogeno, cellulosa, chitina e eteropolisaccaridi)
Reazioni di ossido-riduzione (redox)
teoria + esercizi
I derivati degli idrocarburi
Appunti chimica
Alcoli, Eteri e Fenoli
Sintesi riguardo alcoli, eteri e fenoli con le reazioni e la nomenclatura
Contenuti più popolari di Scienze
9Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Apparato respiratorio
fai un quiz
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Apparato Digerente
Presentazione sull’apparato digerente, con questa presentazione un buono voto è assicurato
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Platone
Riassunto dettagliato su Platone
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Reazioni Redox: Guida Completa con Esempi
Le reazioni redoxsono tra i processi chimici più importanti che ci circondano ogni giorno: dalla respirazione alla fotosintesi, dalla combustione alla corrosione. Queste reazioni coinvolgono sempre uno scambio di elettroni tra le sostanze, dove alcuni atomi perdono elettroni (si... Mostra di più

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Cos'è una reazione redox e il numero di ossidazione
Hai mai pensato a cosa succede quando accendi una candela o quando le piante fanno la fotosintesi? Sono tutte reazioni redox! Il nome viene da "riduzione" e "ossidazione", due processi che avvengono sempre insieme.
In una reazione redox, gli elettroni si spostano da un atomo all'altro. L'ossigeno è spesso il "colpevole" di questi spostamenti perché è molto elettronegativo (dopo il fluoro è il più "avido" di elettroni).
Il numero di ossidazione è come la "carta d'identità" di ogni atomo in un composto: ci dice che carica assume quando gli elettroni si spostano verso l'elemento più elettronegativo. Per esempio, nella combustione del carbonio: C(0) + O₂(0) → CO₂(+4)(-2), il carbonio passa da 0 a +4 perché perde elettroni.
💡 Ricorda: Tutti gli atomi neutri hanno numero di ossidazione 0, come punto di partenza!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Ossidazione e riduzione: chi fa cosa?
Prendiamo l'esempio della combustione del magnesio: 2Mg(0) + O₂(0) → 2MgO(+2)(-2). Qui succedono due cose simultanee che devi ricordare perfettamente.
L'ossidazione è quando un atomo perde elettroni e il suo numero di ossidazione aumenta. Il magnesio si ossida: Mg → Mg²⁺ + 2e⁻ .
La riduzione è quando un atomo acquista elettroni e il suo numero di ossidazione diminuisce. L'ossigeno si riduce: O + 2e⁻ → O²⁻ .
Quindi il magnesio è l'agente riducente (fa ridurre l'ossigeno) mentre l'ossigeno è l'agente ossidante (fa ossidare il magnesio). È come una danza: uno cede, l'altro riceve, sempre in coppia!
💡 Trucco: OIL RIG - Oxidation Involves Loss (of electrons), Reduction Involves Gain!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Come bilanciare le reazioni redox
Il bilanciamento delle reazioni redox può sembrare complicato, ma una volta capito il metodo diventa quasi automatico. L'importante è che il numero di elettroni persi sia uguale a quelli acquistati.
Il metodo della variazione del numero di ossidazione è il più semplice. Prendi la reazione: 2Na + 2H₂O → 2NaOH + H₂. Il sodio si ossida e l'idrogeno si riduce .
Per bilanciare, trova il minimo comune multiplo degli elettroni scambiati. Se uno perde 2 elettroni e l'altro ne acquista 1, dovrai mettere i coefficienti giusti per far coincidere tutto.
Nei casi particolari con più specie che si ossidano o riducono, somma tutti gli elettroni persi da una parte e tutti quelli acquistati dall'altra, poi bilancia come sempre.
💡 Attenzione: Le dismutazioni sono reazioni speciali dove lo stesso elemento si ossida E si riduce contemporaneamente!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Il metodo ionico-elettronico
Quando lavori in soluzione acquosa, il metodo ionico-elettronico è più preciso perché considera la presenza di ioni. È perfetto per l'ambiente del laboratorio!
In ambiente acido, scrivi le due semireazioni separate. Per esempio: 2NO₃⁻ + 4Zn → 4Zn²⁺ + N₂O. Prima bilanci le masse aggiungendo H⁺ e H₂O dove serve, poi bilanci le cariche con gli elettroni.
La semireazione di riduzione: 2NO₃⁻ + 10H⁺ + 8e⁻ → N₂O + 5H₂O. La semireazione di ossidazione: 4Zn → 4Zn²⁺ + 8e⁻. Gli elettroni devono essere uguali nelle due semireazioni!
Infine, sommi tutto e semplifici le specie comuni. Il bello di questo metodo è che ti permette di gestire anche le reazioni più complesse con precisione.
💡 Suggerimento: Bilancia sempre prima le masse, poi le cariche con gli elettroni!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Ambiente basico e esempi pratici
Nell'ambiente basico il procedimento è simile a quello acido, ma alla fine aggiungi ioni OH⁻ per neutralizzare tutti gli H⁺ che hai usato, trasformandoli in H₂O.
Prendi l'esempio: 2ClO⁻ + Bi₂O₃ → 2Cl⁻ + 2BiO₃⁻. Dopo aver bilanciato come in ambiente acido, se hai 6H⁺, aggiungi 6OH⁻ da entrambe le parti per formare 6H₂O.
La regola d'oro è: il numero di ioni ossidrili che aggiungi deve essere uguale al numero più alto di protoni presenti. Poi semplifici le molecole d'acqua che si ripetono.
Ricorda che non devi per forza avere cariche neutre da entrambe le parti, basta che la somma delle cariche dei reagenti sia uguale a quella dei prodotti.
💡 Importante: In ambiente basico, aggiungi sempre OH⁻ da entrambe le parti della reazione!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Esercizi e applicazioni pratiche
Ora che conosci i metodi, è il momento di applicarli! Prendi l'esempio: MnO₄⁻ + SO₃²⁻ → SO₄²⁻ + Mn²⁺. Il manganese si riduce (+7 → +2) e lo zolfo si ossida (+4 → +6).
Le semireazioni sono: MnO₄⁻ + 8H⁺ + 5e⁻ → Mn²⁺ + 4H₂O e SO₃²⁻ + H₂O → SO₄²⁻ + 2H⁺ + 2e⁻. Per bilanciare gli elettroni, moltiplica la prima per 2 e la seconda per 5.
Il risultato finale è: 2MnO₄⁻ + 5SO₃²⁺ + 6H⁺ → 2Mn²⁺ + 5SO₄²⁻ + 3H₂O. Nota come alla fine hai semplificato gli H⁺ e le H₂O in eccesso.
La chiave del successo è fare sempre il controllo finale: verifica che gli atomi e le cariche siano bilanciati da entrambe le parti!
💡 Pro tip: Fai sempre la prova del nove controllando atomi e cariche alla fine!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: Ossidazione
9Chimica organica
Nomenclatura e proprietà di idrocarburi e alogenoderivati: ALCANI, ALCHENI, ALCHINI, IDROCARBURI AROMATICI, ALCOLI, FENOLI, ETERI, ALDEIDI, CHETONI, ACIDI CARBOSSILICI, SAPONI, ESTERI, AMMINE
I carboidrati
Monosaccaridi, disaccaridi e polisaccaridi
Idrocarburi alifatici e aliciclici: Alcani, cicloalcani, Alcheni, Alchini
Alcani, cicloalcani, Alcheni, Alchini con rispettive reazioni
Chimica, programma intero di quinto
Chimica Organica, Biomolecole, Matabolismo del glucosio, Ciclo di Krebs e Fosforilazione Ossidativa; Biochimica del corpo umano, accenni alla fotosintesi. Gli Acidi Nucleici e il DNA, Replicazione, Trascrizione e Traduzione.
Enzimi
Biochimica: gli enzimi - che cosa sono e funzione - specificità enzima - cofattori enzimatici - azione catalitica - attività enzimatica e regolazione
i carboidrati
appunti sui carboidrati: monosaccaridi, proiezioni di Fischer, proiezioni di Haworth, reazioni dei monosaccaridi, oligosaccaridi (lattosio, maltosio e saccarosio) e polisaccaridi (amido, glicogeno, cellulosa, chitina e eteropolisaccaridi)
Reazioni di ossido-riduzione (redox)
teoria + esercizi
I derivati degli idrocarburi
Appunti chimica
Alcoli, Eteri e Fenoli
Sintesi riguardo alcoli, eteri e fenoli con le reazioni e la nomenclatura
Contenuti più popolari di Scienze
9Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Apparato respiratorio
fai un quiz
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Apparato Digerente
Presentazione sull’apparato digerente, con questa presentazione un buono voto è assicurato
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Platone
Riassunto dettagliato su Platone
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.