Hai mai messo il sale nell'acqua per cucinare la pasta?... Mostra di più
Soluzioni e Colloidi: Proprietà e Applicazioni







Soluzioni e Proprietà Elettriche
Una soluzione è un miscuglio omogeneo formato da un solvente (la sostanza presente in maggiore quantità) e un soluto (quella in quantità minore). Quando il solvente è l'acqua, parliamo di soluzioni acquose.
Il processo di formazione avviene grazie all'agitazione termica delle particelle. Nelle soluzioni acquose succede qualcosa di particolare: le molecole d'acqua circondano il soluto attraverso l'idratazione, orientandosi con le cariche positive verso gli ioni negativi e viceversa.
La capacità di condurre elettricità divide i soluti in tre categorie. I non elettroliti (come lo zucchero) non conducono corrente perché rimangono come molecole neutre. Gli elettroliti forti (come il sale da cucina) si dissociano completamente e conducono bene l'elettricità. Gli elettroliti deboli (come l'acido acetico) si ionizzano solo parzialmente.
Tip pratico: Se vuoi sapere se una sostanza è un elettrolita, basta vedere se la sua soluzione in acqua conduce elettricità!
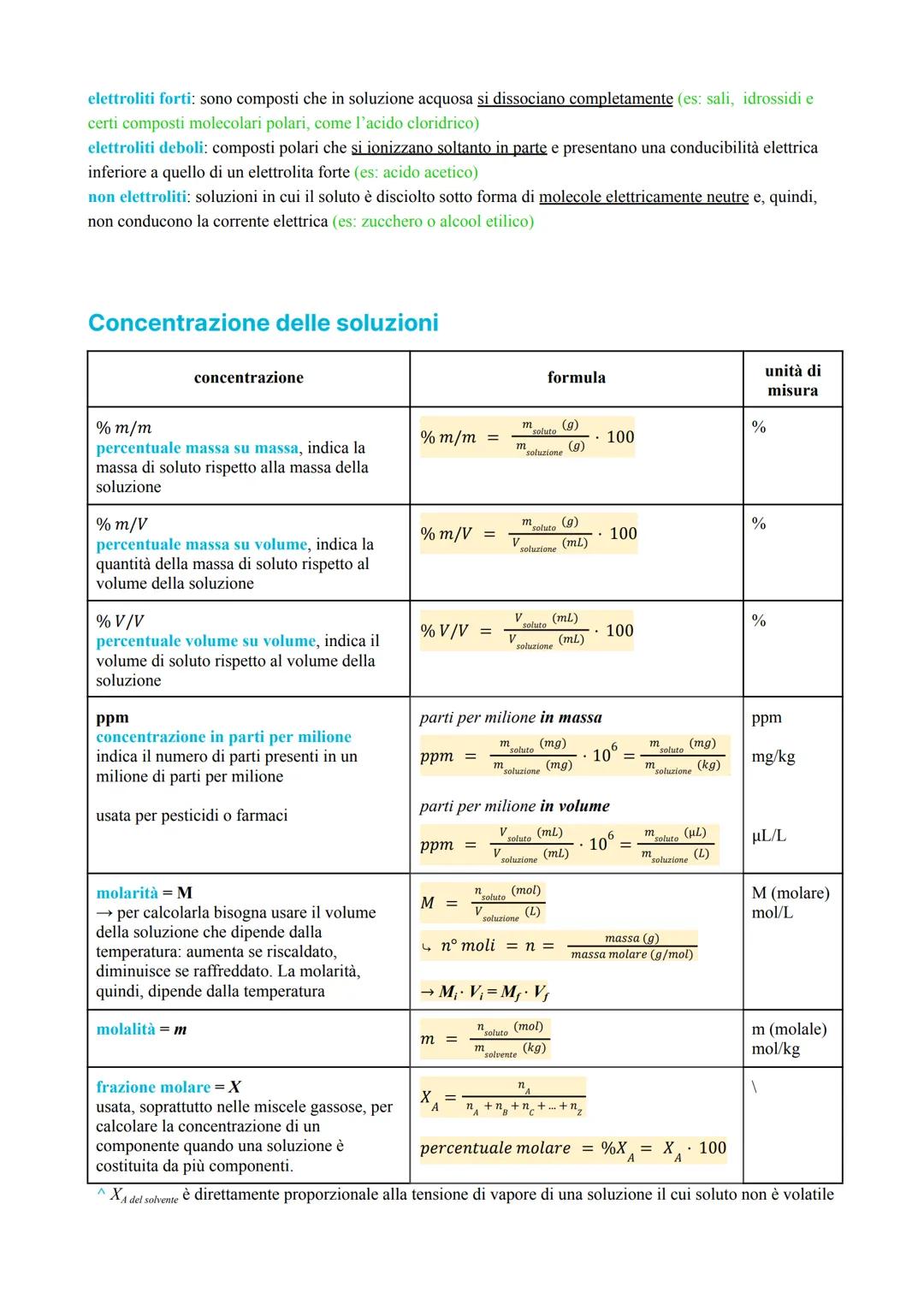
Concentrazione delle Soluzioni
Sapere quanta sostanza hai sciolto è fondamentale in chimica. La concentrazione ti dice esattamente questo e può essere espressa in diversi modi a seconda delle tue necessità.
La percentuale in peso è la più intuitiva: quanti grammi di soluto hai in 100 grammi di soluzione. La molarità è perfetta quando lavori con le reazioni chimiche. La molalità invece non cambia con la temperatura, rendendola ideale per certi calcoli.
Ogni unità di misura ha il suo utilizzo specifico. Per esempio, nei laboratori si usa spesso la molarità perché è facile da calcolare con i volumi, mentre per studiare le proprietà colligative preferisci la molalità.
Ricorda: La concentrazione è come una ricetta - ti dice esattamente quanto ingrediente mettere per ottenere il risultato desiderato!

Proprietà Colligative
Le proprietà colligative sono cambiamenti che dipendono solo dal numero di particelle di soluto, non da che tipo sono. È come se le particelle facessero "squadra" per modificare il comportamento della soluzione.
L'abbassamento crioscopico spiega perché si mette il sale sulle strade ghiacciate: il punto di congelamento si abbassa. L'innalzamento ebullioscopico invece fa bollire la soluzione a temperatura più alta del solvente puro.
La diminuzione della tensione di vapore segue la legge di Raoult: meno molecole di solvente possono "scappare" dalla soluzione. Le formule per calcolare questi effetti sono: Δt = k × m, dove k è una costante caratteristica del solvente e m è la molalità.
Curiosità: Gli iceberg sono ghiaccio puro perché quando l'acqua salata congela, solo l'acqua diventa solida!

Osmosi e Coefficiente di Van't Hoff
Quando hai elettroliti che si dissociano, devi usare il coefficiente di Van't Hoff (i) nelle formule delle proprietà colligative: Δt = k × m × i. Questo coefficiente rappresenta quante particelle produce una molecola di soluto.
L'osmosi è il movimento del solvente attraverso una membrana semipermeabile dalla soluzione meno concentrata a quella più concentrata. La pressione osmotica è la pressione necessaria per fermare questo processo: π = M × R × T.
Le soluzioni si classificano in base alla concentrazione: ipertonica (più concentrata), isotonica (uguale concentrazione) e ipotonica (meno concentrata). L'osmosi inversa permette di ottenere acqua dolce dal mare applicando pressione.
Applicazione pratica: L'osmosi è fondamentale nei processi biologici e nella depurazione dell'acqua!

Solubilità e Fattori che la Influenzano
La solubilità è la quantità massima di soluto che puoi sciogliere in una certa quantità di solvente a una data temperatura. Quando raggiungi questo limite, hai una soluzione satura in equilibrio dinamico.
La temperatura influenza moltissimo la solubilità. La maggior parte dei solidi si scioglie meglio in acqua calda, ma i gas fanno il contrario: più fa caldo, meno si sciolgono. Ecco perché nei laghi caldi i pesci possono morire per mancanza di ossigeno.
La pressione conta principalmente per i gas: più pressione = più gas disciolto nella soluzione. Le soluzioni soprassature contengono più soluto di quanto dovrebbero teoricamente e sono instabili.
Esempio interessante: Il fosfato di calcio è pochissimo solubile in acqua, ed è proprio questo che permette alle nostre ossa di essere resistenti!

Colloidi: Tra Soluzioni e Sospensioni
I colloidi hanno particelle di dimensioni intermedie tra le soluzioni vere e le sospensioni (tra 10⁻⁶ e 10⁻⁹ m). Sembrano omogenei ma non lo sono davvero - sono pseudosoluzioni.
L'effetto Tyndall ti permette di riconoscere un colloide: quando lo illumini appare torbido a causa del moto Browniano delle particelle. Questo movimento continuo e irregolare mantiene stabile il colloide.
Esistono diversi tipi di colloidi. I sol (come il latte di magnesia) si versano come liquidi, i gel (come la gelatina) hanno consistenza gelatinosa, le emulsioni (come la maionese) mescolano liquidi diversi, e gli aerosol hanno particelle in aria (come nebbia o fumo).
Curiosità medica: La dialisi sfrutta membrane semipermeabili per filtrare il sangue quando i reni non funzionano correttamente!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: elettrolita
8i legami chimici
breve sistesi sui legami chimici e sulla forma delle molecole
I Legami Chimici e Forze Intermolecolari
-Covalenti Singolo, Doppio, Triplo, Polare, Dativo -Legame Ionico e Caratteristiche -Forze Intermolecolari (Dipólo-Dipólo, Idrogeno, Wan der Waals/London) -Legame Metallico -Elettorliti e Non Elettroliti -Elettronegatività -Lunghezza e Energia Legame
I fenomeni elettrici
elettrizzazione per strofinio, contatto e induzione; isolanti e conduttori
atomi, molecole e ioni
atomi, molecole e ioni + come raggiungere l’ottetto, elettronegatività: legame covalente, polare, apolare, ionico
L'elettricità
.
Legami chimici
legame ionico e covalente
I legami chimici, cap. 11 chimica Zanichelli
I legami chimici, cap. 11 chimica Zanichelli
Scienze,atomi e molecole,secondo anno ITIS
Atomi, molecole e legami chimici in un semplice riassunto con immagini
Contenuti più popolari di Scienze
9ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Apparato respiratorio
fai un quiz
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Cellula procariote ed eucariote.
Descrizione delle diverse tipologie di microscopi ottici ed elettronici e la struttura della cellula procariote ed eucariote. Composizione delle cellule ed organuli cellulari.
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Soluzioni e Colloidi: Proprietà e Applicazioni
Hai mai messo il sale nell'acqua per cucinare la pasta? O aggiunto lo zucchero al caffè? Stai creando delle soluzionisenza neanche accorgertene! Le soluzioni sono miscugli omogenei che ci circondano ovunque e hanno proprietà affascinanti che influenzano la nostra... Mostra di più

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Soluzioni e Proprietà Elettriche
Una soluzione è un miscuglio omogeneo formato da un solvente (la sostanza presente in maggiore quantità) e un soluto (quella in quantità minore). Quando il solvente è l'acqua, parliamo di soluzioni acquose.
Il processo di formazione avviene grazie all'agitazione termica delle particelle. Nelle soluzioni acquose succede qualcosa di particolare: le molecole d'acqua circondano il soluto attraverso l'idratazione, orientandosi con le cariche positive verso gli ioni negativi e viceversa.
La capacità di condurre elettricità divide i soluti in tre categorie. I non elettroliti (come lo zucchero) non conducono corrente perché rimangono come molecole neutre. Gli elettroliti forti (come il sale da cucina) si dissociano completamente e conducono bene l'elettricità. Gli elettroliti deboli (come l'acido acetico) si ionizzano solo parzialmente.
Tip pratico: Se vuoi sapere se una sostanza è un elettrolita, basta vedere se la sua soluzione in acqua conduce elettricità!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Concentrazione delle Soluzioni
Sapere quanta sostanza hai sciolto è fondamentale in chimica. La concentrazione ti dice esattamente questo e può essere espressa in diversi modi a seconda delle tue necessità.
La percentuale in peso è la più intuitiva: quanti grammi di soluto hai in 100 grammi di soluzione. La molarità è perfetta quando lavori con le reazioni chimiche. La molalità invece non cambia con la temperatura, rendendola ideale per certi calcoli.
Ogni unità di misura ha il suo utilizzo specifico. Per esempio, nei laboratori si usa spesso la molarità perché è facile da calcolare con i volumi, mentre per studiare le proprietà colligative preferisci la molalità.
Ricorda: La concentrazione è come una ricetta - ti dice esattamente quanto ingrediente mettere per ottenere il risultato desiderato!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Proprietà Colligative
Le proprietà colligative sono cambiamenti che dipendono solo dal numero di particelle di soluto, non da che tipo sono. È come se le particelle facessero "squadra" per modificare il comportamento della soluzione.
L'abbassamento crioscopico spiega perché si mette il sale sulle strade ghiacciate: il punto di congelamento si abbassa. L'innalzamento ebullioscopico invece fa bollire la soluzione a temperatura più alta del solvente puro.
La diminuzione della tensione di vapore segue la legge di Raoult: meno molecole di solvente possono "scappare" dalla soluzione. Le formule per calcolare questi effetti sono: Δt = k × m, dove k è una costante caratteristica del solvente e m è la molalità.
Curiosità: Gli iceberg sono ghiaccio puro perché quando l'acqua salata congela, solo l'acqua diventa solida!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Osmosi e Coefficiente di Van't Hoff
Quando hai elettroliti che si dissociano, devi usare il coefficiente di Van't Hoff (i) nelle formule delle proprietà colligative: Δt = k × m × i. Questo coefficiente rappresenta quante particelle produce una molecola di soluto.
L'osmosi è il movimento del solvente attraverso una membrana semipermeabile dalla soluzione meno concentrata a quella più concentrata. La pressione osmotica è la pressione necessaria per fermare questo processo: π = M × R × T.
Le soluzioni si classificano in base alla concentrazione: ipertonica (più concentrata), isotonica (uguale concentrazione) e ipotonica (meno concentrata). L'osmosi inversa permette di ottenere acqua dolce dal mare applicando pressione.
Applicazione pratica: L'osmosi è fondamentale nei processi biologici e nella depurazione dell'acqua!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Solubilità e Fattori che la Influenzano
La solubilità è la quantità massima di soluto che puoi sciogliere in una certa quantità di solvente a una data temperatura. Quando raggiungi questo limite, hai una soluzione satura in equilibrio dinamico.
La temperatura influenza moltissimo la solubilità. La maggior parte dei solidi si scioglie meglio in acqua calda, ma i gas fanno il contrario: più fa caldo, meno si sciolgono. Ecco perché nei laghi caldi i pesci possono morire per mancanza di ossigeno.
La pressione conta principalmente per i gas: più pressione = più gas disciolto nella soluzione. Le soluzioni soprassature contengono più soluto di quanto dovrebbero teoricamente e sono instabili.
Esempio interessante: Il fosfato di calcio è pochissimo solubile in acqua, ed è proprio questo che permette alle nostre ossa di essere resistenti!

Iscriviti per mostrare il contenuto. È gratis!
- Accesso a tutti i documenti
- Migliora i tuoi voti
- Unisciti a milioni di studenti
Colloidi: Tra Soluzioni e Sospensioni
I colloidi hanno particelle di dimensioni intermedie tra le soluzioni vere e le sospensioni (tra 10⁻⁶ e 10⁻⁹ m). Sembrano omogenei ma non lo sono davvero - sono pseudosoluzioni.
L'effetto Tyndall ti permette di riconoscere un colloide: quando lo illumini appare torbido a causa del moto Browniano delle particelle. Questo movimento continuo e irregolare mantiene stabile il colloide.
Esistono diversi tipi di colloidi. I sol (come il latte di magnesia) si versano come liquidi, i gel (come la gelatina) hanno consistenza gelatinosa, le emulsioni (come la maionese) mescolano liquidi diversi, e gli aerosol hanno particelle in aria (come nebbia o fumo).
Curiosità medica: La dialisi sfrutta membrane semipermeabili per filtrare il sangue quando i reni non funzionano correttamente!
Pensavamo che non l'avreste mai chiesto....
Che cos'è l'assistente AI di Knowunity?
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
Dove posso scaricare l'applicazione Knowunity?
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Knowunity è davvero gratuita?
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
Contenuti più popolari: elettrolita
8i legami chimici
breve sistesi sui legami chimici e sulla forma delle molecole
I Legami Chimici e Forze Intermolecolari
-Covalenti Singolo, Doppio, Triplo, Polare, Dativo -Legame Ionico e Caratteristiche -Forze Intermolecolari (Dipólo-Dipólo, Idrogeno, Wan der Waals/London) -Legame Metallico -Elettorliti e Non Elettroliti -Elettronegatività -Lunghezza e Energia Legame
I fenomeni elettrici
elettrizzazione per strofinio, contatto e induzione; isolanti e conduttori
atomi, molecole e ioni
atomi, molecole e ioni + come raggiungere l’ottetto, elettronegatività: legame covalente, polare, apolare, ionico
L'elettricità
.
Legami chimici
legame ionico e covalente
I legami chimici, cap. 11 chimica Zanichelli
I legami chimici, cap. 11 chimica Zanichelli
Scienze,atomi e molecole,secondo anno ITIS
Atomi, molecole e legami chimici in un semplice riassunto con immagini
Contenuti più popolari di Scienze
9ripassa l'apparato digerente con queste sfide difficili!
10/10 prova questo quiz per ripassare l apparato digerente
Struttura della Cellula Eucariote
Ripasso delle componenti principali come nucleo, membrana e citoplasma per comprendere l'organizzazione di base della cellula.
Fondamenti dell'Apparato Circolatorio
Identifica gli organi principali dell'apparato circolatorio e le loro funzioni primarie nel corpo umano.
°• LA CELLULA •°
le cellule eucariote e procariote. Le cellule vegetali e animali
Anatomia dell'Apparato Digerente
Identifica i principali organi e le loro funzioni primarie all'interno del sistema digerente umano.
LA CELLULA EUCARIOTE
spiegazione della cellula eucariote, membrana cellulare e le due cellule ecucariotica vegetale ed animale
Apparato respiratorio
fai un quiz
Le biomolecole- Carboidrati, Lipidi, Proteine e Acidi Nucleici
Le biomolecole
Cellula procariote ed eucariote.
Descrizione delle diverse tipologie di microscopi ottici ed elettronici e la struttura della cellula procariote ed eucariote. Composizione delle cellule ed organuli cellulari.
Contenuti più popolari
9Riassunto patente B
Riassunto patente B - appunti presi a lezione
Teoria patente b
Tutti gli argomenti per la patente
I promessi sposi
Riassunti completi di tutti i 38 capitoli dei Promessi sposi.
Teoria patente di guida B: Segnali stradali
Segnali stradali di pericolo, luminosi, di prescrizione, di indicazione, temporanei, complementari, pannelli integrativi, segnaletica orizzontale, segnalazioni agenti del traffico, distanza di visibilità per l‘arresto, minima di sicurezza.
PATENTE
schemi per esame teorico della patente
promessi sposi (capitoli 1-18)
riassunto promessi sposi (capitoli da 1 a 18)
Sintesi finale di Analisi logica
Esercitazione completa di analisi logica su frasi articolate per consolidare la conoscenza di tutti i complementi.
I promessi sposi
Riassunti capitolo 1 - capitolo 26
Programma di italiano per la maturità
Decadentismo, Pascoli, D'Annunzio, la poesia e il romanzo di primo 900, il romanzo della crisi, le avanguardie storiche, Svevo, Pirandello, Ungaretti, l'ermetismo, Calvino (nel mio profilo trovate anche montale)
Non c'è niente di adatto? Esplorare altre aree tematiche.
Recensioni dei nostri utenti. Ci adorano - e anche tu, vedrai .
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.