La chimica studia la materia, la sua struttura e le... Mostra di più
Iscriviti per mostrare il contenutoÈ gratis!
Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Knowunity AI
Materie
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Mostra tutti gli argomenti
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Mostra tutti gli argomenti
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Mostra tutti gli argomenti
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Mostra tutti gli argomenti
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Mostra tutti gli argomenti
4,186
•
Aggiornato May 14, 2026
•
Laura
@_laurab
La chimica studia la materia, la sua struttura e le... Mostra di più










Benvenuti nel mondo della chimica! Questa scienza si occupa di capire come funziona la materia che ci circonda, studiando gli atomi e le loro trasformazioni.
La chimica è ovunque nella tua vita quotidiana: quando cuoci un uovo, quando una batteria si scarica o quando respiri. Imparare i suoi principi ti aiuterà a comprendere meglio il mondo che ti circonda.
💡 Lo sapevi che... Anche tu sei fatto di atomi! Il tuo corpo contiene miliardi di miliardi di atomi che lavorano insieme per farti vivere.

Tutto quello che puoi toccare e vedere è materia - ha una massa e occupa spazio. La materia può esistere in tre stati: solido, liquido e aeriforme (gas).
I solidi mantengono forma e volume propri perché le loro particelle sono molto vicine e non si muovono liberamente. I liquidi hanno volume fisso ma prendono la forma del contenitore, mentre i gas si espandono per riempire tutto lo spazio disponibile.
La materia può essere una miscela (più sostanze mescolate insieme) o una sostanza pura (un solo tipo di materia). Le miscele si dividono in omogenee (come l'acqua salata) ed eterogenee (come l'olio nell'acqua).
Per separare le miscele usi metodi fisici come la filtrazione, la distillazione o la cromatografia. Questi metodi sfruttano le diverse proprietà delle sostanze, come dimensione o temperatura di ebollizione.
⚗️ Esperimento mentale: Pensa al caffè: l'acqua calda estrae le sostanze dal caffè in polvere - questo è un esempio di estrazione con solventi!

Le sostanze pure hanno composizione uniforme e costante. Si dividono in elementi (come l'ossigeno) che non si possono scomporre, e composti (come l'acqua) formati da più elementi legati insieme.
L'atomo è il mattoncino fondamentale della materia. Democrito ne parlava già nel 400 a.C., ma la prima teoria scientifica è di Dalton (1802). Secondo Dalton, tutti gli elementi sono fatti di atomi indivisibili e uguali tra loro.
Due leggi importanti confermano l'esistenza degli atomi: la legge di conservazione della massa (la massa non si crea né si distrugge) e la legge delle proporzioni definite (nei composti gli elementi si combinano sempre nelle stesse proporzioni).
La legge delle proporzioni multiple spiega perché due elementi possono formare più composti diversi, come CO e CO₂.
🔬 Curiosità: Dalton era daltonico (non distingueva i colori) - da lui prende il nome questa condizione!

L'atomo non è indivisibile come pensava Dalton! Rutherford scoprì che ha un nucleo centrale con protoni (+) e neutroni (neutri), circondato da elettroni (-) che orbitano a grande distanza.
Il numero atomico (Z) indica quanti protoni ha un atomo, mentre il numero di massa (A) è la somma di protoni e neutroni. Gli isotopi sono atomi dello stesso elemento con diversi numeri di neutroni.
Bohr migliorò il modello introducendo le orbite stazionarie - gli elettroni possono stare solo in certe orbite specifiche, e quando saltano da un'orbita all'altra emettono o assorbono energia.
Il modello ondulatorio moderno descrive gli elettroni come "nuvole di probabilità" chiamate orbitali. Non possiamo sapere esattamente dove si trova un elettrone, ma solo la probabilità di trovarlo in una certa zona.
🌟 Pensaci così: Gli elettroni sono come api che volano intorno all'alveare - sai dove probabilmente si trovano, ma non la loro posizione esatta!

Gli elettroni si sistemano negli orbitali seguendo regole precise. La configurazione elettronica ti dice dove sono posizionati tutti gli elettroni di un atomo.
I numeri quantici descrivono ogni orbitale: n indica la dimensione e l'energia, l la forma, m l'orientamento nello spazio, e ms lo spin dell'elettrone.
Gli orbitali si chiamano s (sferici), p (a forma di manubrio), d e f (forme più complesse). Ogni orbitale s può contenere massimo 2 elettroni, p fino a 6, d fino a 10, f fino a 14.
Le tre regole fondamentali sono: principio di Aufbau (riempi prima gli orbitali a energia minore), principio di Pauli (massimo 2 elettroni per orbitale con spin opposti), regola di Hund (negli orbitali della stessa energia, metti prima un elettrone in ciascuno).
📝 Trucco per ricordare: Pensa agli orbitali come appartamenti: prima riempi quelli più economici (bassa energia), massimo 2 inquilini per appartamento!

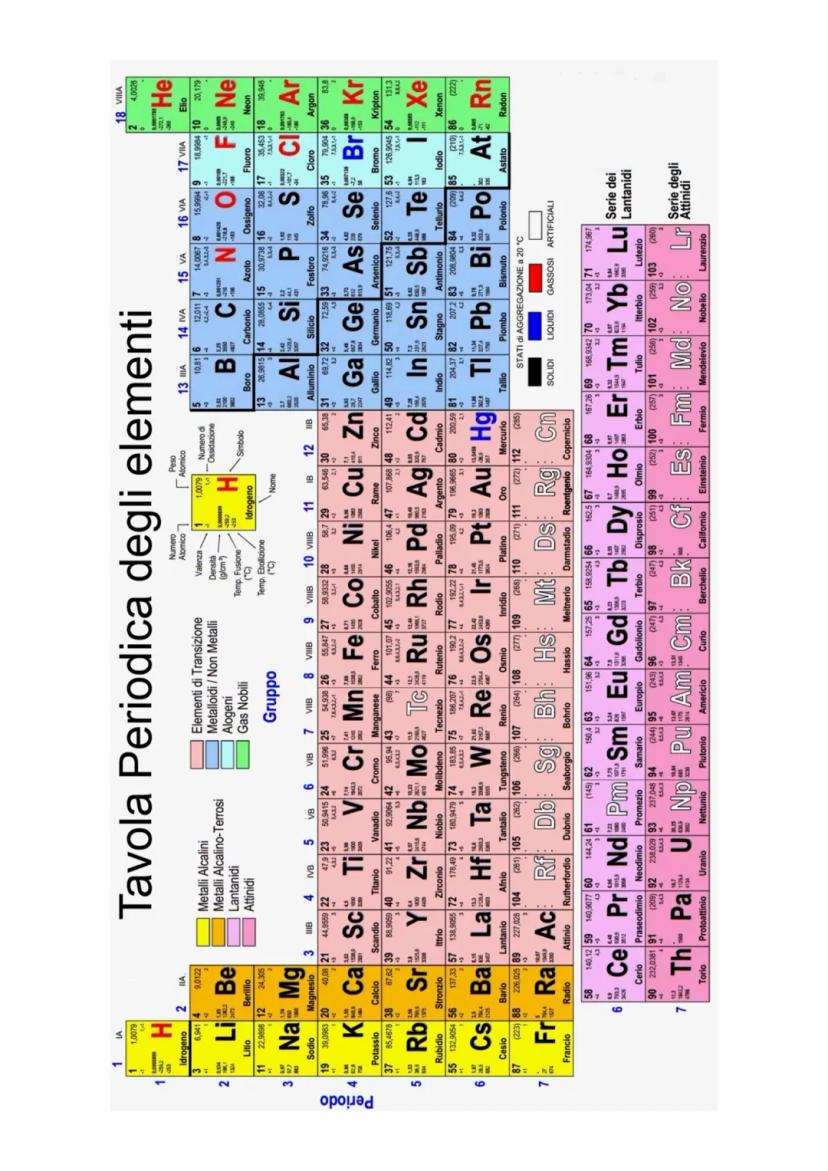
La tavola periodica organizza tutti gli elementi in righe (periodi) e colonne (gruppi). Gli elementi dello stesso gruppo hanno le stesse proprietà perché hanno lo stesso numero di elettroni di valenza (elettroni esterni).
Gli elementi si dividono in metalli (sinistra della tavola, conducono elettricità), non metalli (destra, isolanti) e semimetalli (proprietà intermedie).
Le proprietà periodiche cambiano in modo prevedibile: la dimensione atomica aumenta scendendo nei gruppi e diminuisce andando da sinistra a destra nei periodi.
Il potenziale di ionizzazione (energia per strappare un elettrone) e l'elettronegatività (capacità di attrarre elettroni) variano in modo opposto alla dimensione atomica.
🗺️ Mappa mentale: La tavola periodica è come una mappa: se sai leggere le coordinate (gruppo e periodo), puoi prevedere le proprietà di qualsiasi elemento!
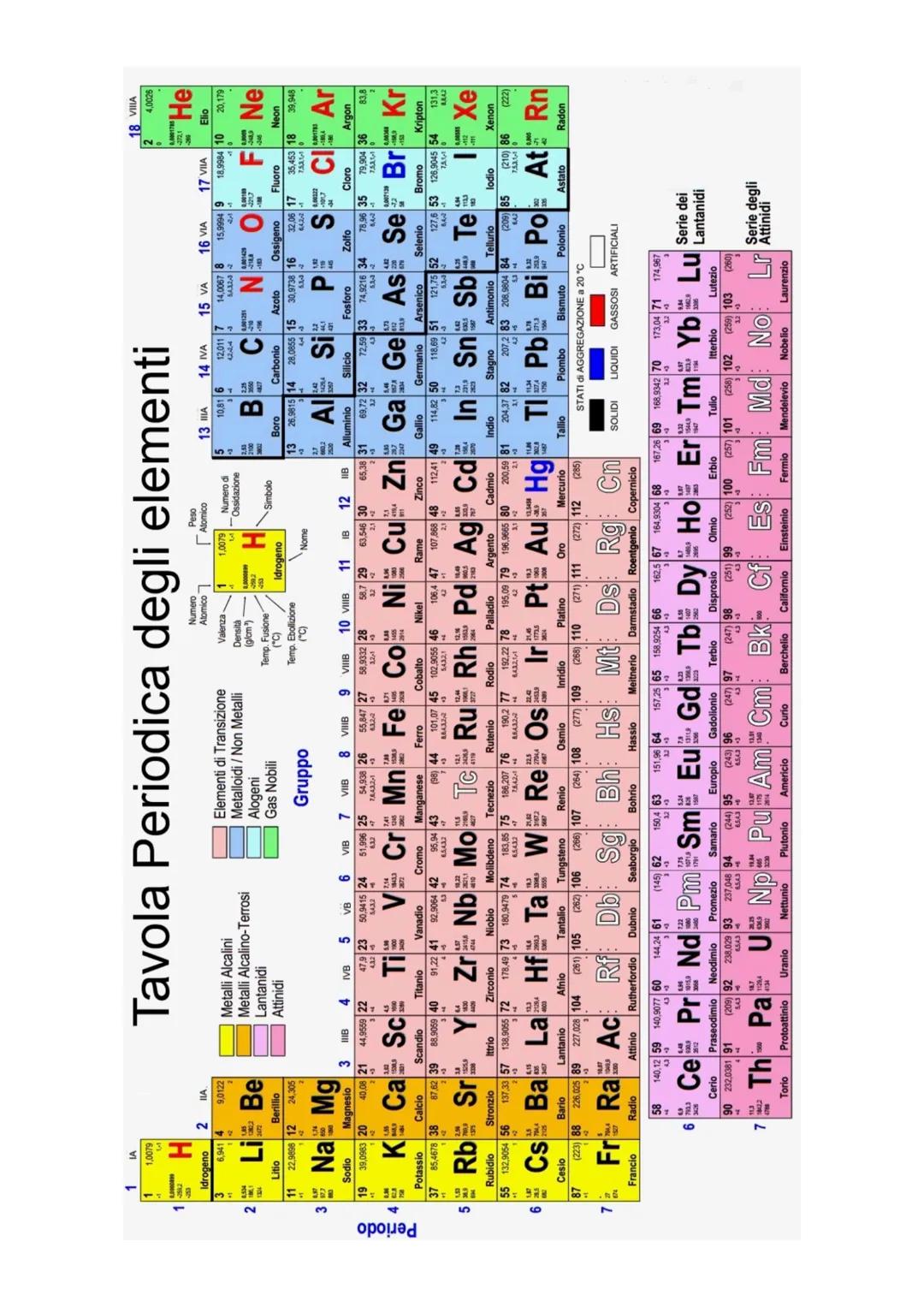
Questa è la tavola periodica completa che userai per tutta la tua carriera in chimica. Ogni casella contiene informazioni preziose: simbolo, numero atomico, massa atomica e altre proprietà.
I colori diversi indicano le famiglie di elementi: metalli alcalini (gruppo 1), alogeni (gruppo 17), gas nobili (gruppo 18), elementi di transizione (centro), lantanidi e attinidi (serie separate in basso).
La tavola ti permette di fare previsioni: se conosci le proprietà di un elemento, puoi immaginare quelle dei suoi "vicini". Gli elementi dello stesso gruppo si comportano in modo simile.
Memorizza almeno i primi 20 elementi - li userai continuamente! Noterai che alcuni hanno simboli "strani" perché derivano dai nomi latini (Na per sodio viene da "natrium").
🎯 Sfida: Prova a trovare un elemento per ogni lettera dell'alfabeto - scoprirai che alcune lettere sono più difficili di altre!

Gli isotopi sono "fratelli" dello stesso elemento: hanno lo stesso numero di protoni ma diversi neutroni. Per esempio, il carbonio-12 e il carbonio-14 sono isotopi del carbonio.
La massa atomica si misura in unità di massa atomica (u.m.a.), definita come 1/12 della massa del carbonio-12. Il peso molecolare è la somma delle masse atomiche di tutti gli atomi in una molecola.
La mole è l'unità fondamentale in chimica - contiene sempre 6,022 × 10²³ particelle (numero di Avogadro). Una mole di qualsiasi sostanza ha una massa in grammi pari numericamente al suo peso atomico/molecolare.
Per calcolare le moli usi la formula: n = m/PM . Questo ti permette di "contare" gli atomi e le molecole pesandoli!
💡 Analogia: Una mole è come una dozzina: così come 1 dozzina = 12 pezzi, 1 mole = 6,022 × 10²³ particelle, che sia di uova o di atomi!

I gas perfetti seguono leggi semplici: legge di Boyle , legge di Charles , legge di Gay-Lussac .
Tutte si riassumono nell'equazione di stato: PV = nRT, dove R = 0,082. La legge di Avogadro dice che una mole di qualsiasi gas occupa 22,4 litri a condizioni standard.
La chimica nucleare studia i nuclei atomici. Alcuni isotopi sono radioattivi e si trasformano emettendo radiazioni alfa, beta o gamma. Il tempo di dimezzamento indica quanto tempo serve perché metà degli atomi radioattivi si trasformi.
Fissione (scissione di nuclei pesanti) e fusione (unione di nuclei leggeri) liberano enormi quantità di energia - sono alla base delle centrali nucleari e del sole.
⚡ Fatto incredibile: Il sole "brucia" 4 milioni di tonnellate di idrogeno al secondo trasformandolo in elio attraverso la fusione nucleare!

Solo i gas nobili stanno da soli in natura - tutti gli altri atomi sono "socievoli" e si legano tra loro per diventare più stabili. I responsabili sono gli elettroni di valenza (quelli del guscio esterno).
La regola dell'ottetto spiega perché gli atomi si legano: vogliono tutti avere 8 elettroni esterni come i gas nobili, la configurazione più stabile in assoluto.
Il legame covalente si forma quando due atomi condividono elettroni. Più coppie condividono, più forte è il legame: legame semplice (1 coppia), doppio (2 coppie), triplo (3 coppie).
Quando due orbitali atomici si sovrappongono, formano un orbitale molecolare che circonda entrambi i nuclei. La lunghezza di legame dipende dall'equilibrio tra forze attrattive e repulsive.
🤝 Metafora: I legami chimici sono come amicizie: gli atomi "condividono" elettroni per stare meglio, proprio come gli amici condividono esperienze per essere più felici!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
Laura
@_laurab
La chimica studia la materia, la sua struttura e le trasformazioni che subisce. Tutto quello che ci circonda - dall'aria che respiriamo all'acqua che beviamo - è fatto di atomi che si combinano in modi diversi per formare sostanze e... Mostra di più

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Benvenuti nel mondo della chimica! Questa scienza si occupa di capire come funziona la materia che ci circonda, studiando gli atomi e le loro trasformazioni.
La chimica è ovunque nella tua vita quotidiana: quando cuoci un uovo, quando una batteria si scarica o quando respiri. Imparare i suoi principi ti aiuterà a comprendere meglio il mondo che ti circonda.
💡 Lo sapevi che... Anche tu sei fatto di atomi! Il tuo corpo contiene miliardi di miliardi di atomi che lavorano insieme per farti vivere.

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Tutto quello che puoi toccare e vedere è materia - ha una massa e occupa spazio. La materia può esistere in tre stati: solido, liquido e aeriforme (gas).
I solidi mantengono forma e volume propri perché le loro particelle sono molto vicine e non si muovono liberamente. I liquidi hanno volume fisso ma prendono la forma del contenitore, mentre i gas si espandono per riempire tutto lo spazio disponibile.
La materia può essere una miscela (più sostanze mescolate insieme) o una sostanza pura (un solo tipo di materia). Le miscele si dividono in omogenee (come l'acqua salata) ed eterogenee (come l'olio nell'acqua).
Per separare le miscele usi metodi fisici come la filtrazione, la distillazione o la cromatografia. Questi metodi sfruttano le diverse proprietà delle sostanze, come dimensione o temperatura di ebollizione.
⚗️ Esperimento mentale: Pensa al caffè: l'acqua calda estrae le sostanze dal caffè in polvere - questo è un esempio di estrazione con solventi!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Le sostanze pure hanno composizione uniforme e costante. Si dividono in elementi (come l'ossigeno) che non si possono scomporre, e composti (come l'acqua) formati da più elementi legati insieme.
L'atomo è il mattoncino fondamentale della materia. Democrito ne parlava già nel 400 a.C., ma la prima teoria scientifica è di Dalton (1802). Secondo Dalton, tutti gli elementi sono fatti di atomi indivisibili e uguali tra loro.
Due leggi importanti confermano l'esistenza degli atomi: la legge di conservazione della massa (la massa non si crea né si distrugge) e la legge delle proporzioni definite (nei composti gli elementi si combinano sempre nelle stesse proporzioni).
La legge delle proporzioni multiple spiega perché due elementi possono formare più composti diversi, come CO e CO₂.
🔬 Curiosità: Dalton era daltonico (non distingueva i colori) - da lui prende il nome questa condizione!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
L'atomo non è indivisibile come pensava Dalton! Rutherford scoprì che ha un nucleo centrale con protoni (+) e neutroni (neutri), circondato da elettroni (-) che orbitano a grande distanza.
Il numero atomico (Z) indica quanti protoni ha un atomo, mentre il numero di massa (A) è la somma di protoni e neutroni. Gli isotopi sono atomi dello stesso elemento con diversi numeri di neutroni.
Bohr migliorò il modello introducendo le orbite stazionarie - gli elettroni possono stare solo in certe orbite specifiche, e quando saltano da un'orbita all'altra emettono o assorbono energia.
Il modello ondulatorio moderno descrive gli elettroni come "nuvole di probabilità" chiamate orbitali. Non possiamo sapere esattamente dove si trova un elettrone, ma solo la probabilità di trovarlo in una certa zona.
🌟 Pensaci così: Gli elettroni sono come api che volano intorno all'alveare - sai dove probabilmente si trovano, ma non la loro posizione esatta!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Gli elettroni si sistemano negli orbitali seguendo regole precise. La configurazione elettronica ti dice dove sono posizionati tutti gli elettroni di un atomo.
I numeri quantici descrivono ogni orbitale: n indica la dimensione e l'energia, l la forma, m l'orientamento nello spazio, e ms lo spin dell'elettrone.
Gli orbitali si chiamano s (sferici), p (a forma di manubrio), d e f (forme più complesse). Ogni orbitale s può contenere massimo 2 elettroni, p fino a 6, d fino a 10, f fino a 14.
Le tre regole fondamentali sono: principio di Aufbau (riempi prima gli orbitali a energia minore), principio di Pauli (massimo 2 elettroni per orbitale con spin opposti), regola di Hund (negli orbitali della stessa energia, metti prima un elettrone in ciascuno).
📝 Trucco per ricordare: Pensa agli orbitali come appartamenti: prima riempi quelli più economici (bassa energia), massimo 2 inquilini per appartamento!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
La tavola periodica organizza tutti gli elementi in righe (periodi) e colonne (gruppi). Gli elementi dello stesso gruppo hanno le stesse proprietà perché hanno lo stesso numero di elettroni di valenza (elettroni esterni).
Gli elementi si dividono in metalli (sinistra della tavola, conducono elettricità), non metalli (destra, isolanti) e semimetalli (proprietà intermedie).
Le proprietà periodiche cambiano in modo prevedibile: la dimensione atomica aumenta scendendo nei gruppi e diminuisce andando da sinistra a destra nei periodi.
Il potenziale di ionizzazione (energia per strappare un elettrone) e l'elettronegatività (capacità di attrarre elettroni) variano in modo opposto alla dimensione atomica.
🗺️ Mappa mentale: La tavola periodica è come una mappa: se sai leggere le coordinate (gruppo e periodo), puoi prevedere le proprietà di qualsiasi elemento!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Questa è la tavola periodica completa che userai per tutta la tua carriera in chimica. Ogni casella contiene informazioni preziose: simbolo, numero atomico, massa atomica e altre proprietà.
I colori diversi indicano le famiglie di elementi: metalli alcalini (gruppo 1), alogeni (gruppo 17), gas nobili (gruppo 18), elementi di transizione (centro), lantanidi e attinidi (serie separate in basso).
La tavola ti permette di fare previsioni: se conosci le proprietà di un elemento, puoi immaginare quelle dei suoi "vicini". Gli elementi dello stesso gruppo si comportano in modo simile.
Memorizza almeno i primi 20 elementi - li userai continuamente! Noterai che alcuni hanno simboli "strani" perché derivano dai nomi latini (Na per sodio viene da "natrium").
🎯 Sfida: Prova a trovare un elemento per ogni lettera dell'alfabeto - scoprirai che alcune lettere sono più difficili di altre!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Gli isotopi sono "fratelli" dello stesso elemento: hanno lo stesso numero di protoni ma diversi neutroni. Per esempio, il carbonio-12 e il carbonio-14 sono isotopi del carbonio.
La massa atomica si misura in unità di massa atomica (u.m.a.), definita come 1/12 della massa del carbonio-12. Il peso molecolare è la somma delle masse atomiche di tutti gli atomi in una molecola.
La mole è l'unità fondamentale in chimica - contiene sempre 6,022 × 10²³ particelle (numero di Avogadro). Una mole di qualsiasi sostanza ha una massa in grammi pari numericamente al suo peso atomico/molecolare.
Per calcolare le moli usi la formula: n = m/PM . Questo ti permette di "contare" gli atomi e le molecole pesandoli!
💡 Analogia: Una mole è come una dozzina: così come 1 dozzina = 12 pezzi, 1 mole = 6,022 × 10²³ particelle, che sia di uova o di atomi!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
I gas perfetti seguono leggi semplici: legge di Boyle , legge di Charles , legge di Gay-Lussac .
Tutte si riassumono nell'equazione di stato: PV = nRT, dove R = 0,082. La legge di Avogadro dice che una mole di qualsiasi gas occupa 22,4 litri a condizioni standard.
La chimica nucleare studia i nuclei atomici. Alcuni isotopi sono radioattivi e si trasformano emettendo radiazioni alfa, beta o gamma. Il tempo di dimezzamento indica quanto tempo serve perché metà degli atomi radioattivi si trasformi.
Fissione (scissione di nuclei pesanti) e fusione (unione di nuclei leggeri) liberano enormi quantità di energia - sono alla base delle centrali nucleari e del sole.
⚡ Fatto incredibile: Il sole "brucia" 4 milioni di tonnellate di idrogeno al secondo trasformandolo in elio attraverso la fusione nucleare!

Accesso a tutti i documenti
Migliora i tuoi voti
Unisciti a milioni di studenti
Solo i gas nobili stanno da soli in natura - tutti gli altri atomi sono "socievoli" e si legano tra loro per diventare più stabili. I responsabili sono gli elettroni di valenza (quelli del guscio esterno).
La regola dell'ottetto spiega perché gli atomi si legano: vogliono tutti avere 8 elettroni esterni come i gas nobili, la configurazione più stabile in assoluto.
Il legame covalente si forma quando due atomi condividono elettroni. Più coppie condividono, più forte è il legame: legame semplice (1 coppia), doppio (2 coppie), triplo (3 coppie).
Quando due orbitali atomici si sovrappongono, formano un orbitale molecolare che circonda entrambi i nuclei. La lunghezza di legame dipende dall'equilibrio tra forze attrattive e repulsive.
🤝 Metafora: I legami chimici sono come amicizie: gli atomi "condividono" elettroni per stare meglio, proprio come gli amici condividono esperienze per essere più felici!
Il nostro assistente AI è costruito specificamente per le esigenze degli studenti. Sulla base dei milioni di contenuti presenti sulla piattaforma, possiamo fornire agli studenti risposte davvero significative e pertinenti. Ma non si tratta solo di risposte, l'assistente è in grado di guidare gli studenti attraverso le loro sfide quotidiane di studio, con piani di studio personalizzati, quiz o contenuti nella chat e una personalizzazione al 100% basata sulle competenze e sugli sviluppi degli studenti.
È possibile scaricare l'applicazione dal Google Play Store e dall'Apple App Store.
Sì, hai accesso completamente gratuito a tutti i contenuti nell'app e puoi chattare o seguire i Creatori in qualsiasi momento. Sbloccherai nuove funzioni crescendo il tuo numero di follower. Inoltre, offriamo Knowunity Premium, che consente di studiare senza alcun limite!!
127
Strumenti Intelligenti NUOVO
Trasforma questi appunti in: ✓ 50+ Domande di Pratica ✓ Flashcard Interattive ✓ Simulazione d'esame completa ✓ Schemi per Saggi
App Store
Google Play
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS
L'applicazione è molto facile da usare e ben progettata. Finora ho trovato tutto quello che cercavo e ho potuto imparare molto dalle presentazioni! Utilizzerò sicuramente l'app per i compiti in classe! È molto utile anche come fonte di ispirazione.
Stefano S
utente iOS
Questa applicazione è davvero grande! Ci sono tantissimi appunti e aiuti con lo studio [...]. La mia materia problematica, per esempio, è il francese e l'app ha così tante opzioni per aiutarmi. Grazie a questa app ho migliorato il mio francese. La consiglio a tutti.
Samantha Klich
utente Android
Wow, sono davvero stupita. Ho appena provato l'app perché l'ho vista pubblicizzata molte volte e sono rimasta assolutamente sbalordita. Questa app è L'AIUTO che cercate per la scuola e soprattutto offre tantissime cose, come allenamenti e schede, che a me personalmente sono state MOLTO utili.
Anna
utente iOS
È bellissima questa app, la adoro. È utilissima per lo studio e mi aiuta molto, anzi moltissimo, ma soprattutto mi aiutano molto i quiz, per memorizzare anche quello che non sapevo
Anastasia
utente Android
Fantastica per qualsiasi materia avere gli appunti anche di altre persone è molto utile perchè posso confrontarmi e vedere come migliorarmi. con i quiz riesco ad apprendere al meglio.
Francesca
utente Android
moooolto utile,gli appunti sono belli e funzionanti,schoolGPT da dei consigli formidabili!!
Marianna
utente Android
L'applicazione è semplicemente fantastica! Tutto ciò che devo fare è inserire l'argomento nella barra di ricerca e ottengo la risposta molto velocemente. Non devo guardare 10 video di YouTube per capire qualcosa, quindi risparmio tempo. Consigliatissima!
Sudenaz Ocak
utente Android
A scuola andavo malissimo in matematica, ma grazie a questa applicazione ora vado meglio. Vi sono molto grato per aver creato questa app.
Greenlight Bonnie
utente Android
Knowunity è un applicazione fantastica,considerando che ha degli schemi veramente molto carini e sfiziosi e che ci sono dei quiz,oltre al fatto che questa cosa dell intelligenza artificiale "school gpt" è almeno per me molto utile, perché a differenza di Chatgpt ti da le spiegazioni, ti spiega ciò che non è chiaro! Posso studiare più velocemente tramite gli schemi e che posso pubblicare io stessa gli schemi è una funzione utilissima per gli altri studenti. Knowunity è PERFETTA
Aurora
utente Android
L’app funziona benissimo e puoi trovare qualsiasi tipo di informazione. Non ho l’abbonamento ma la parte gratuita è sufficiente per uno studio approfondito.
Martina
utente iOS
I quiz E LE flashcard SONO COSÌ UTILI E ADORO Knowunity IA. È ANCHE LETTERALMENTE COME CHATGPT MA PIÙ INTELLIGENTE!! MI HA AIUTATO ANCHE COI MIEI PROBLEMI DI MASCARA!! E ANCHE CON LE MIE VERE MATERIE! OVVIO 😍😁😲🤑💗✨🎀😮
Chiara
utente IOS
Questa app è una delle migliori, nient’altro da dire.
Andrea
utente iOS